- Study on Adsorption Characteristics of Perfluorinated Compounds(PFCs) with Structural Properties
HyoJung Choi·Deok Hyun Kim·JongHyun Yoon·JongBeom Kwon·Moonsu Kim·Hyun-Koo Kim·Sun-Kyoung Shin·Sunhwa Park*
Soil and Groundwater Research Division, National Institute of Environmental Research, Incheon 22689, Korea
- 과불화화합물 구조적 속성에 따른 흡착 특성 연구
최효정·김덕현·윤종현·권종범·김문수·김현구·신선경·박선화*
국립환경과학원 토양지하수연구과
This article is an open access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/4.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Perfluorinated compounds(PFCs), an emerging environmental pollutant, are environmentally persistent and bioaccumulative organic compounds that possess a toxic impact on human health and ecosystems. PFCs are distributed widely in environment media including groundwater, surface water, soil and sediment. PFCs in contaminated solid can potentially leach into groundwater. Therefore, understanding PFCs partitioning between the aqueous phase and solid phase is important for the determination of their fate and transport in the environment. In this study, the sorption equilibrium batch and kinetic experiment of PFCs were carried out to estimated the sorption coefficient(Kd) and the fraction between aqueous-solid phase partition, respectively. Sorption branches of the PFDA(Perfluoro-n-decanoic acid), PFNA(Perfluoro-n-nonanoic acid), PFOA(Perfluoro-n-octanoic acid), PFOS(Perfluoro-1-octane sulfonic acid) and PFHxS(Perfluoro-1-hexane sulfonic acid) isotherms were nearly linear, and the estimated Kd was as follow: PFDA(1.50) > PFOS(1.49) > PFNA(0.81) > PFHxS(0.45) > PFOA(0.39). The sorption kinetics of PFDA, PFNA, PFOA, PFOS and PFHxS onto soil were described by a biexponential adsorption model, suggesting that a fast transport into the surface layer of soil, followed by two-step diffusion transport into the internal water and/or organic matter of soil. Shorter times(<20hr) were required to achieve equilibrium and fraction for adsorption on solid(F1, F2) increased with perfluorinated carbon chain length and sulfonate compounds in this study. Overall, our results suggested that not only the perfluorocarbon chain length, but also the terminal functional groups are important contributors to electrostatic and hydrophobic interactions between PFCs and soils, and organic matter in soils significantly affects adsorption maximum capacity than kinetic rate.
Keywords: PFCs, Adsorption, Batch test, Kinetics, Partitioning coefficient
PFOA(Perfluorooctanoic acid), PFOS(Perfluorooctane sur- fonate)와 같은 과불화화합물(perfluorinated compounds, PFCs)은 알킬(alkyl)사슬의 수소(hydrogen)원자가 불소(fluorine)로 치환된 소수성(hydrophobic)특성을 지니는 탄소사슬과 친수성(hydrophilic) 작용기가 결합되어 있는 구조를 지니고 있다(Du et al., 2014; Pereira et al., 2018; Oliver et al., 2019; Li et al., 2020). 유기화학결합 중에서 강한 결합 중 하나로 알려진 C-F의 결합(결합에너지 536 kJ/mol, Li et al., 2020)은 화학적으로 안정된 구조 형성과 물리, 생물학적 분해에 대한 저항력을 높이는데(Zhang et al., 2013; Li et al., 2018, 2019)기여하는 바가 크다. 이러한 특성으로 인해 과불화화합물은 난분해성 물질로 잔류성 유기오염물질(Persistence organic pollutants, POPs)과 유사하게 환경에 오랜 기간 머물며, 생물축적 등을 통해 인체 및 환경에 심각한 영향을 미칠 수 있어 국내·외적인 관심이 꾸준히 증가하고 있다(Du et al., 2014; Groffen et al., 2019).
과불화화합물은 폐수, 지표수, 지하수, 토양, 퇴적물을 포함한 대부분의 다양한 환경매질에서 검출되고 있다. 과불화화합물로 오염된 토양입자가 지하수 환경으로 직접적으로 흘러 들어가 잠재적 오염원이 될 수 있으며(Wei et al., 2017), 수체 내 잔류하고 있는 과불화화합물이 부유입자와 같은 고체상 매질에 흡착되어 이동(transport) 및 변환(transformation)의 과정을 거쳐 거동에 영향을 준다(Du et al., 2014). 과불화화합물의 환경 내 거동에 있어 서로 다른 과불화탄소 사슬의 길이와 작용기와 같은 해당 화합물의 물리·화학적 속성에 의해 영향을 받는 것으로 보고하고 있는데(Ahrens et al., 2011, 2014), 예를 들어 소수성을 나타내는 과불화탄소 사슬의 길이는 해당 화합물의 항목별 용해도를 결정하는 데에 기여하는 바가 크다고 설명하고 있다. 과불화탄소 사슬의 길이가 짧아 상대적으로 친수성이 강한 항목은 용해도가 증가하여 일반적으로 지하수 환경 내에서 용존상태로 존재하게 되고, 반면에 과불화탄소사슬의 길이가 길어 상대적으로 소수성이 강한 항목은 지하수 환경으로 유입되면 고체상 매질과 결합하여 이동하게 되며, 이로 인하여 생물체 내 생축적 가능성을 높이게 된다(Ahrens et al., 2014; Brendel et al., 2018).
과불화화합물과 같은 오염물질의 거동에 있어 고체상 입자 형태의 흡착제의 역할이 중요하다고 가정한다면 토양과 지하수 생태계 내에서의 과불화화합물의 이동과 거동을 파악하기 위해서는 고체상과 액체상 사이에서의 화합물의 흡착 및 분배(partitioning) 특성이 규명되어야 한다(Chen et al., 2016; Wei et al., 2017; Li et al., 2019). 과불화화합물의 토양으로 흡착에 관한 대부분의 연구(Milinovic et al., 2015; Miao et al., 2017; Wei et al., 2017; Groffen et al., 2019; Li et al., 2019)에서 보고한 바에 따르면 특정 단일 인자만의 영향으로 흡착 거동을 예측하기 어렵지만, 토양 내 유기물이 흡착능을 조절하는 중요한 인자라고 보고하고 있다(Wei et al., 2017; Groffen et al., 2019). 지하수 환경에서 토양의 유기물과 과불화화합물 사이에서의 흡착은 주로 소수성 상호작용(hydrophobic interaction)과 정전기적 상호작용(electrostatic interaction)에 의해 일어나는데(Du et al., 2014; Li et al., 2018; Oliver et al., 2019; Gagliano et al., 2020), 이는 음으로 하전된 과불화화합물의 작용기와 소수성의 과불화탄소사슬로 인하여 발생하는 흡착 기작이라고 설명하고 있다(Li et al., 2018).
본 연구에서는 과불화화합물 구조적 속성에 따른 흡착 거동특성 평가를 위하여 과불화화합물 14개 항목에 대한 흡착평형 배치(batch) 및 반응속도(kinetic analysis)실험을 수행하였다. 실험 결과로 도출한 고체상-액체상에서의 분배계수 및 흡착평형 도달시간 비교를 통하여 흡착 특성을 평가하였고, 유기물 함량이 다른 토양에서 실시한 국내ㆍ외 연구 결과와 유사성 검증ㆍ평가를 실시하였다.
2.1. 흡착 실험
2.1.1. PFCs 표준물질
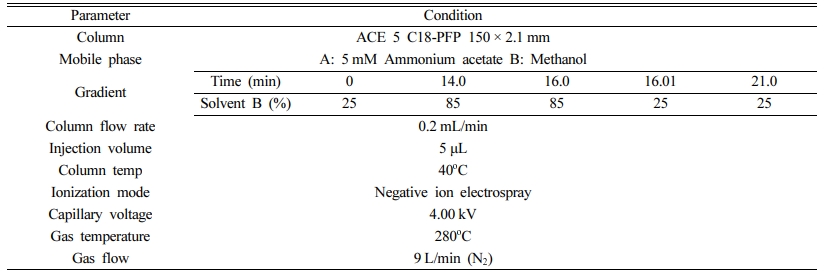
본 연구에서는 과불화화합물 14개 항목에 대해 동시 분석이 가능한 Wellington Laboratories(Ontario, Canada)사의 PFAC-MXB[Solution/Mixture of Native Perfluoroalkylcarboxylic Acids and Native Perfluoroalkylsufonates, 2000 mg/L in methanol/water(<1%)] 표준용액을 사용하였다. 내부표준물질 또한 같은 제조사의 EPA-737IS[Internal Standard Primary dilution standard, Perfluoro-n-[1,2-13C2]octanoic acid : 1000 mg/L, Sodium perfluoro-1-[1,2,3,4-13C2]octane- sulfonate : 3000 mg/L in methanol/water(<1%)]를 사용하였다. 과불화화합물 14개 항목 종류와 내부표준물질의 항목에 대한 정보는 Table 1에 나타내었다.
2.1.2. 회분식 흡착 실험
채취한 표토는 상온에서 풍건시킨 후 10 메쉬(< 2 mm)체로 걸러 균일하게 만든 후 흡착실험에 사용되었다. 회분식 흡착실험은 Chen(2016)의 방법을 참고하여 진행했으며, 폴리프로필렌 재질의 50 mL 코니컬 튜브(conical tube)에 토양 시료 5 g과 정제수(HPLC grade, J.T. Baker)를 40 mL을 첨가한 후 과불화화합물 표준 용액(PFCs MXB, 2000 mg/L)을 초기농도(C0)가 0, 0.5, 1, 2, 5, 10 μg/L가 되도록 처리하였다. 처리한 과불화화합물은 5일 간 상온에서 70 rpm의 속도로 교반시켜 평형상태에 도달하게 하였다. 이후 원심분리(4000 rpm, 15 min)하여 각 시료의 상등액을 분취하였고, 상등액의 잔여 입자는 실린지와 멤브레인 필터(cellulose acetate, <0.45 mm)를 이용하여 제거하였다. 이때 사용된 실린지와 필터는 모두 폴리프로필렌 재질이며, 여과 전 필터는 메탄올(HPLC grade, J.T. Baker)로 세척 한 후 HPLC grade 정제수로 흘려보내 주었다. 여과된 시료의 용출 및 농축, 분석은 2.2에 서술한 방법에 따른다.
2.1.3. 흡착 반응속도 실험
과불화화합물의 항목별 흡착 비율 및 속도상수 산정을 평가하기 위해 lab-scale 실험을 수행하였다. 배치실험 방법과 같은 방법으로 토양시료 2 g과 HPLC grade 정제수를 20 mL를 주입 후, 과불화화합물 표준용액을(PFCs MXB, 2000 mg/L)을 초기농도(C0)가 2 μg/L가 되도록 스파이킹(spiking) 하였다. 설정된 처리구에서 시간별로(0, 0.5, 1, 2, 4, 6, 24 hr) 시료를 채취하였으며, 배치실험과 동일한 방법으로 시료의 전처리 및 분석을 수행하였다.
2.2. PFCs 분석
여과된 상등액 내 과불화화합물 분석을 위한 추출은 카트리지 활성화, 시료 로딩(loading), 카트리지 건조, 시료 추출과정을 거쳐 진행하였다. 추출을 위해 Supelco사의 Visiprep Vacuum Manifold에 Waters사의 Oasis HLB 카트리지를 장착한 후, HPLC grade 메탄올과 정제수를 차례로 흘러 보내주며 카트리지를 활성화시킨다. 활성화된 카트리지에 여과된 상등액을 로딩시키는데, 이때 유속은 약 10-15 mL/min으로 한다. 시료가 카트리지에 로딩이 완료 되면, 카트리지를 진공상태로 한 후 약 15분가량 건조시킨다. 건조가 끝난 카트리지에 HPLC grade 8 mL (4 mL, 2회)를 흘려보내주어 카트리지에 로딩된 과불화화합물을 폴리프로필렌 재질의 바이알에 용출시킨다. 용출 한 후에는 질소농축기(Organomation Associates inc, N-EVAPTM112, USA)로 농축하였으며, 농축이 완료된 바이알에 HPLC grade 메탄올을 주입하여 최종 부피 0.4 mL가 되도록 한다.
과불화화합물은 HPLC-MS/MS(LCMS-8030, SHIMADZU)를 사용하여 분석하였으며, 정량은 ESI(Electrospray Ionization)모드와 전구 이온(precursor ion), 생성 이온(product ion) 값을 이용하여 실시하였으며, 각 항목에 대한 ion값은 Table 1와 같으며, 기기 분석 조건은 Table 2에 나타내었다.
2.3. 토양 내 과불화화합물 농도 및 흡착계수 산정
토양으로 흡착된 과불화화합물의 농도(Cs, mg/kg)는 식 (1)을 이용하여 산정하였다. 초기 농도(C0, mg/L)와 시간(t, hr)마다 채취한 시료의 농도(Ct)차이에서 주입한 증류수의 부피(L)를 통해 토양으로 흡착된 과불화화합물의 질량을 산정 후 토양시료의 무게(M, kg)로 나누어 계산하였다.

분배계수(Kd, water-solid partitioning coefficient)는 식 (2)을 이용하여 산출하였고, 시간(t, hr)에 해당하는 채취한 시료의 농도(Ct)와 흡착 후 토양농도(Cs)와의 비율로 계산한다. 토양농도는 식 (1)을 통해 산정한 농도 값을 이용한다.

2.4. 과불화화합물의 이중지수흡착모델(Biexponential adsorption model)
항목 별 카이네틱 특성 및 액체-고체상 분배 비율 평가·비교를 위해 과불화화합물 대상으로 한 흡착 특성 평가 연구(Zhang et al., 2013; Li et al., 2019)에서 적용한 이중지수흡착모델을 본 연구에서도 적용하였으며, 적용된 식은 아래와 같다(식 (3)). 흡착이중지수모델은 고체상 표면에 빠르게 흡착되는 (<1~2 hr) 반응과 고체상 내부로 느리게 확산되면서 흡착되는 반응(<48 hr)에 따른 속도상수와 속도에 따른 고체-액체상에서의 분배되는 비율을 산정할 수 있다.

Fw: 초기농도 대비 시간당(t) 채취한 액체상 PFCs의 농도
F0: 입자상으로 흡착될 수 없는 PFCs의 비율
F1: 속도상수(k1)에 따른 고체상 표면에 빠르게(<1~2 hr) 흡착되는 PFCs의 비율
F2: 속도상수(k2)에 따른 고체상 내부로 느리게(<48 hr) 흡착되는 PFCs의 비율
2.5. 토양의 물리·화학적 인자 분석
토양의 화학적 속성의 결정을 위한 분석은 토양화학분석법(NAAS, 2010)에 따라 유기물함량은 습식산화법(Walkley-Black)으로 분석하였으며, 토양 내 유기탄소의 함량을 식 (4))를 이용하여 유기물함량을 산정하였다.

pH와 EC는 건조된 토양과 증류수를 1:5(w/v)로 혼합하여 30분 진탕 후 pH는 HM-30R(DKK-TOA, Japan)를, EC는 CM-25R(DKK-TOA, Japan)을 이용하여 측정하였다. 양이온치환용량(Cation exchange capacity, CEC)은 ammonium acetate법으로 전처리하였고, 단백질/질소 자동분석기(Kieltec auto 2400/8400 system, Tecator AB, Swe- den)으로 분석하였다. 치환성양이온(Exchange-able cation, Ca, Na, Mg, K)은 ammonium acetate법으로 전처리 후 iCAPTM 7400 ICP-OES(Thermo ScientificTM, USA)으로 분석하였다.
토양의 물리적 속성은 토양 및 식물체 분석법(RDA, 2000)에 따라 토성 결정을 위한 입경분석은 침강속도의 차이를 이용한 pipet법으로 수행하였으며, 결과는 미국농무성법에 의해 입경 구분을 하였다. 가비중과 진비중은 10 메쉬(<2 mm) 체거름 한 시료를 Pycnometer법을 이용하여 산정하였다.
|
Table 1 Identities, carbon chain lengths and MRM conditions of measurement for PFCs |
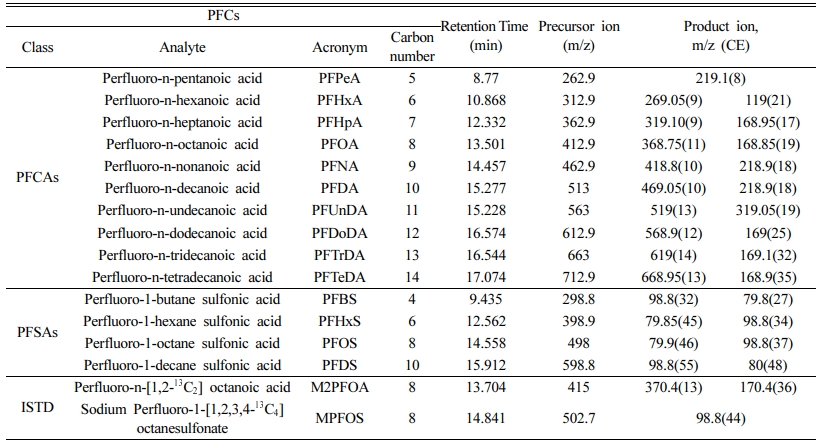
※ PFCAs : Perfluorocarboxylates |
3.1. 토양의 물리·화학적 속성
흡착 배치실험에 사용된 토양의 물리화학적 인자 정보는 Table 3과 같다. 토성은 양토(loam)이며, pH는 6.6으로 중성에 가깝게 측정되었다. 유기물 함량(Organic Matter, OM)은 약 1.8%인 것으로 나타났다. 이전 연구에서 언급한 유기탄소농도에 따른 과불화화합물 흡착 특성 결과와 본연구를 비교하기 위해 식 (4)(Mettingly et al., 1974)를 이용하여 유기탄소 농도를 유기물 함량으로 변환하여 비교·논의하였다.
3.2. 과불화화합물 흡착 등온식
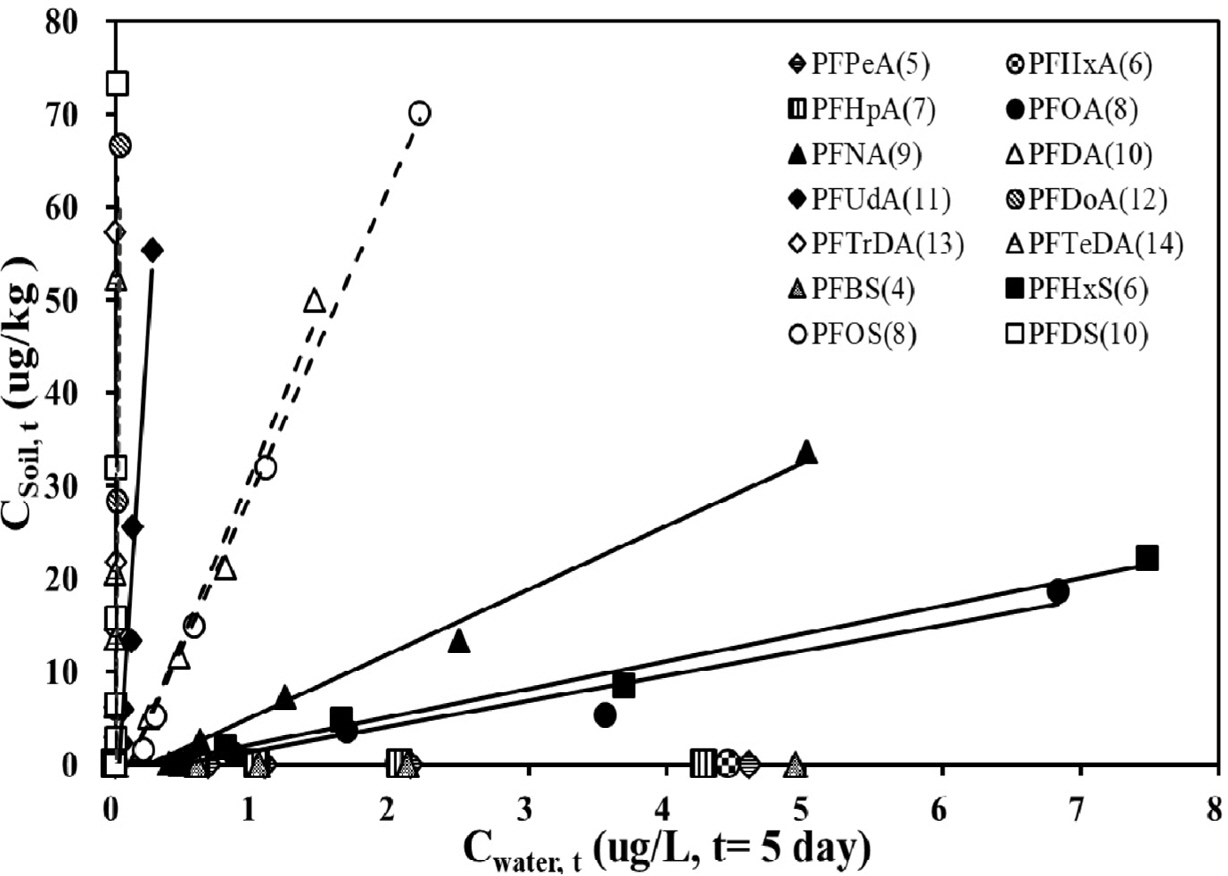
5일 동안 흡착이 진행된 시료의 상등액을 분취하여 과불화화합물 14개 항목에 대해 분석을 실시한 결과, 초기 농도(C0) 대비하여 평형상태 도달 후의 수용액 상 잔류 농도(C5days)와의 차이 수준이 과불화탄소사슬의 길이에 따라 3가지의 다른 양상을 보였다(Fig. 1). 검출된 14개 항목 중 상대적으로 과불화탄소사슬의 길이가 짧은 항목[PFBS(C:4), PFBA(C:4), PFPeA(C:5), PFHxA(C:6), PFHpA (C:7)]은 C0대비하여 C5days가 변화가 없는 반면, 과불화탄소사슬의 길이가 긴 항목[PFDS(C:10), PFUnDA(C:11), PFDoDA(C:12), PFTrDA(C:13), PFTeDA(C:13)]은 C5days가 MDL이하로 검출되었고, 나머지 5개 항목[PFDA(C:10), PFOS(C:8), PFNA(C:9), PFHxS(C:6), PFOA(C:8)]은 C0의 일부가 유의한 차이를 보이며 저감되는 양상을 보였다. 이렇듯, 전체적으로 C0 대비 평균 저감 비율[(C0-C5days)/C0]은 과불화탄소사슬의 길이가 길어짐에 따라 유의하게 증가하였다(r=0.89, p<0.05, Pearson’s correlation). 저감된 과불화화합물의 질량이 토양으로 완전한 흡착이 이루어졌다는 가정하에 고려해보면 각 항목이 지니는 탄소사슬의 길이가 길어질수록 토양으로의 흡착의 수준도 증가하는 것으로 해석할 수 있다.
본 연구에서는 주입농도 상관없이 흡착이 이루어지지 않았거나 흡착이 완벽하게 이루어진 두 분류에 속한 항목을 제외하고 수용액 상의 농도 일부가 토양에 흡착되어 분배계수 산정이 가능한 5개 항목에 관해서만 논의하고자 한다. 초기농도와 유의한 차이를 보이는 5개 항목은 수용액 상 잔류 농도 기준(C5days)으로 PFDA(C:10)항목이 가장 적은 농도[0.18 mg L-1(0.5 mg L-1); 0.24 mg L-1(1 mg L-1); 0.46 mg L-1(2 mg L-1); 0.80 mg L-1 (5 mg L-1); 1.4 mg L-1(10 mg L-1)]로 검출되었으며, 그 다음 순으로 PFOS (C:8), PFNA(C:9), PFHxS(C:6). PFOA(C:8)순으로 나타났다. 이 농도차이(C0-C5days)를 반영하여 식 (1)에 의해 산정된 토양의 농도(Cs)는 PFDA > PFOS > PFNA > PFHxS > PFOA순으로 나타났으며(Fig. 1), 흡착능의 세기의 순서와 같다고 판단한다.
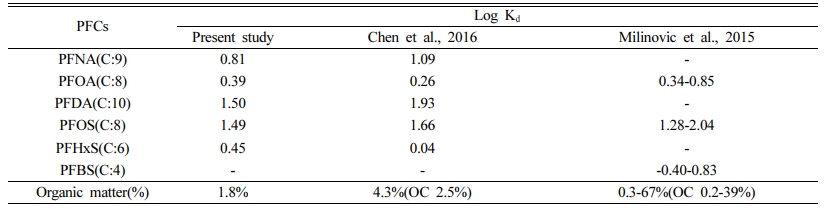
본 연구결과의 14개 항목에 대한 흡착 등온식은 Fig. 1에 나타냈으며, 등온곡선을 통해 산정한 Kd와 국외 문헌에서 발췌한 Kd는 Table 4에 언급하였다. 본 연구에서 실시한 흡착 등온식(adsorption isotherm)은 흡착이 평형으로 도달하는 동안 선형관계로(Fig. 1) 나타나 Kd(water-solid partitioning coefficient)로 분배계수를 산정하였다. 그런 다음 다른 연구 결과와의 비교를 위해 Kd상수는 log로 변환하였다. Log Kd의 크기는 흡착능의 세기의 순서와 같이 PFDA(C:10) > PFOS(C:8) > PFNA(C:9) > PFHxS(C:6) > PFOA(C:8)순으로 나타났다. 앞에서 언급한 흡착 후 산정된 토양농도의 결과와 같이 과불화탄소의 길이가 증가할수록 분배계수가 증가하는 경향을 보였다. 이 전 연구결과에서도 유사한 경향을 보였음을 확인하였다(Chen et al., 2016).
그러나 과불화탄소를 8개를 가진 PFOS의 Kd와 9개를 가진 PFNA의 Kd를 비교해보면 오히려 적은 탄소수를 가진 항목의 Kd가 높고, PFHxS(C:6)와 PFOA(C:8)의 Kd도 서로 다른 과불화탄소의 수로 구성되었음에도 유사하게 산정되었다. 그리고 과불화탄소길이가 같은 PFDS (C:10) vs PFDA(C:10)와 PFOS(C:8) vs PFOA(C:8)항목의 Kd도 비교해보면 PFDS와 PFOS의 Kd가 높게 나타났음을 확인 할 수 있었다. 이전 연구에서는 이러한 결과에 대해 과불화탄소사슬의 길이가 뿐만 아니라 과불화화합물에 구조화된 서로 다른 작용기 또한 흡착을 결정짓는 중요한 인자라고 언급하였고, 카르복실기(carboxylate)의 작용기를 가지는 항목보다 설폰기(sulfonate)를 가지는 항목일수록 흡착능이 강해진다고 보고하고 있다(Higgins and Luthy, 2006; Milinovic et al., 2015; Chen et al., 2016; Wei et al., 2017: Li et al., 2019).
3.3. 과불화화합물 흡착 반응속도
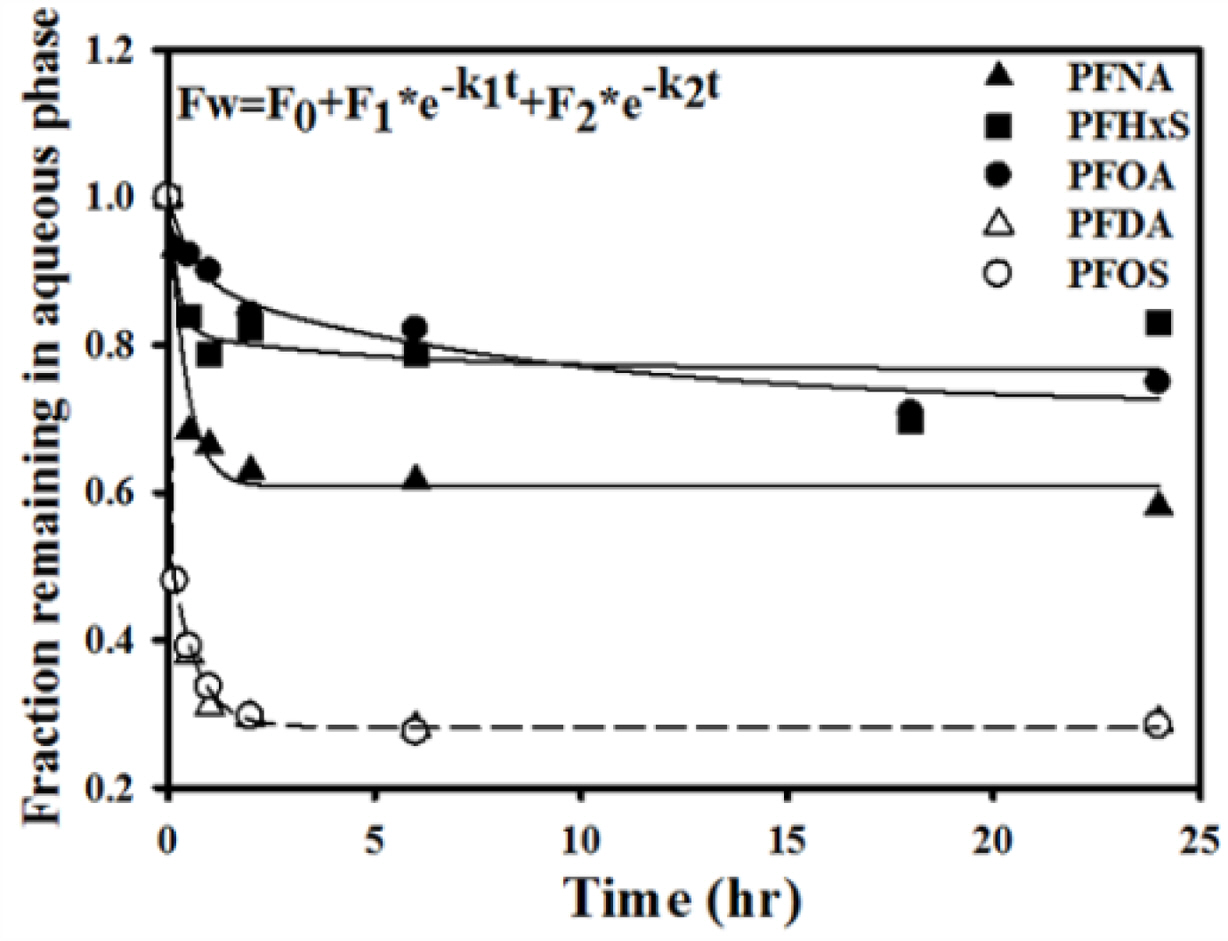
이전 연구들에서는 PFCs와 같은 오염물질이 고체상으로 확산이 이루어질 때 고체상 표면 경계층에서 빠른 속도로 흡착이 이루어진 후, 고체상 응집체 내부에 존재하는 수분이나 유기물로 흡착이 이루어지는 2단계 확산 거동(two-step diffusional transport) 기작을 따른다고 보고 하였으며, 2.4에 언급한 이중지수 흡착모델(Biexponential adsorption model)을 적용하여 반응속도 실험 결과를 해석하였다(Higgins and Luthy, 2006; Zhang et al., 2013; Li et al., 2019). 본 연구에서 실시한 실험 결과 또한 이중지수흡착모델을 적용하였으며, 1~2시간 이내에 고체상 표면에서 이루어지는 흡착반응과 상대적으로 느린 속도로(<48 hr) 고체상 내부에서 일어나는 흡착반응에 대한 분배비율 및 속도상수를 산정하였다.
토양시료에 표준용액을 스파이킹 후 30초의 볼텍싱(vortexing)과정을 거치는 동안에도 유의하게 흡착반응은 일어나고 있다고 보고하고 있다(Higgins and Luthy, 2006; Li et al., 2019). 이 흡착모델은 이러한 초기 흡착반응에 대해서는 고려하지 않았고, 초기 흡착반응 후의 농도를 초기값(t=0)으로 보고 비율을 산정하였기 때문에 Fw의 값이 모두 1 미만으로 나타났으나, 본 연구에서는 선행연구 결과에서 관찰할 수 없었던 과불화탄소사슬의 길이가 긴 항목의 흡착의 경향을 파악하기 위해 초기 흡착반응 전의 농도를 초기값으로 설정하여 비율을 산정하였다.
이전 실험 결과와 같이 흡착 속도상수와 액체-고체상 분배비율 평가가 가능한 항목은 PFDA, PFOS, PFNA, PFHxS, PFOA이며, 각 항목의 비율은 Fig. 2와 Table 5에 제시하였다. 5개 항목의 흡착이 평형상태에 도달하는데 <20 hr이 소요되었으며, 이는 이전 국외 연구에서 실시했던 결과와 비교하여 상대적으로 짧은 시간이 소요됐다(10 days, Higgins and Luthy, 2006; <48 hr, Zhang et al., 2013 and Li et al., 2019). Table 5에 제시한 결과를 보면 과불화탄소사슬 길이가 증가할수록 입자상으로 분포할 수 없는 과불화화합물의 비율(F0)은 감소하고, 토양으로 흡착된 과불화화합물의 비율(F1, F2)이 증가하는 경향을 나타냈다. 과불화탄소사슬의 길이가 긴 항목은 상대적으로 소수성이 강해 액체상으로 용존화 되기 어렵고 토양과 같은 고체상과의 흡착능이 높다고 설명하고 있다(Ahrens et al., 2011, 2014; Deng et al., 2012; Groffen et al., 2019).
같은 탄소사슬의 길이를 가지는 PFOA와 PFOS의 결과를 비교하면, 설폰기를 가지는 PFOS의 산정된 비율이 PFOA의 F0보다 낮고, 흡착 정도를 반영한 F1와 F2는 높은 경향을 보였다. 이는 설폰기로 구조화된 항목일수록 입자상으로 분배 될 가능성이 크다는 것을 의미하며, 3.2에서 언급한 연구결과와 같은 기작으로 설명이 가능하다. Pearson의 굳은(Hard)-무른(Soft)-산(Acid)/염기(Base)(HSAB theory) 이론에 따르면, 카르복실기-과불화화합물(PFCAs)는 상대적으로 무른 염기(Soft base)의 특성을 가지는 반면에 설폰기-과불화화합물(PFSAs)는 굳은 염기(Hard base)의 특성을 지니고 있어 굳은 산(Hard acid)의 산화물(oxide) 표면으로의 흡착이 용이하다고 해석한다. 그리고 이전 연구 결과에서도 PFSAs는 활성탄, 레진, 실리카, 제올라이트, 퇴적물, 슬러지와 같은 흡착제로의 흡착능이 같은 탄소사슬을 지니는 PFCAs보다 우세한 것으로 보고되고 있다(Waters et al., 1991; Wang et al., 2012; Du et al., 2014).
본 연구에서 나타난 흡착평형은 토양 내 유기물 함량이 더 높은 조건(5.64%)에서 실시한 Li(2019)의 연구에서 나타난 결과에 비하여 빠른 속도로 도달했지만, 흡착계수(Kd)와의 비교에서는 본 연구에서 도출한 흡착계수가 더 낮게 관찰되었다. 이는 토양 내 유기물의 함량에 따른 차이는 최대 흡착능(sorption capacity)을 결정짓는 요인이 되지만 흡착 속도를 반영하는 요인이 되지 않는 것으로 해석할 수 있다. 우리와는 다른 흡착모델을 적용한 이전 연구 결과에서도 흡착 속도를 반영한 상수를 조절하는 요인은 토양이 가지는 속성이며, 특히 토양 표면의 광물(minenal) 함량이 속도상수를 조절하는데 기여가 크다고 서술하였다(Miao et al., 2017). 그리고 토양의 형태 및 구조와 오염물질의 농도, 흡착제와의 친화성을 포함한 그 외 다양한 인자도 흡착 속도 결정에 관여한다고 보고하고 있다(Cheung et al., 2007; Miao et al., 2017).
3.4. 과불화화합물 흡착 기작
과불화화합물의 흡착반응은 정전기적 상호작용(Electrostatic interaction), 소수성 상호작용(Hydrophobic interaction), π-π 결합, 수소 결합(Hydrogen bond), 반데르발스 힘(Van der Waals force) 등 다양한 기작으로 설명이 가능하지만(Du et al., 2014; Wei et al., 2017; Li et al., 2018), 과불화화합물의 친양쪽성의 구조가 흡착반응 내 관여하는 주요 기작은 정전기적 상호작용과 소수성 상호작용이라고 언급하고 있다(Higgins and Luthy, 2006; Du et al., 2014; Li et al., 2018; Groffen et al., 2019; Gagliano et al., 2020).
과불화화합물은 낮은 pKa의 특성을 가지고 있어 일반적인 수환경 pH범위 내에서는 각 화합물에 구조화된 작용기로 인하여 음이온화 상태로 존재하게 되는데(Du et al., 2014; Li et al., 2019), 이온화된 과불화화합물과 전하를 뛰는 흡착제 표면 사이에서 정전기적 상호작용이 일어날 수 있다(Xaio et al., 2011; Du et al., 2014; Li et al., 2019; Gagliano et al., 2020). 추가적으로 과불화합물의 중심부는 양이온으로 하전되어 있어 과불화화합물의 외곽 셀(shell)은 음전하로 강하게 하전되기도 한다. 이는 정전기적 상호작용을 강하게 만드는 요인이다(Jonhnson et al., 2007; Du et al., 2014). 정전기적 흡착반응은 수환경의 pH와 이온강도(Ionic strength)에 의해 영향을 받게 된다. 이전 연구에 따르면 pH 변화는 흡착제 표면에 구조화된 작용기의 양성자화(protonation), 탈양성자화(deprotonation) 반응을 통해 흡착제 표면의 전하를 변이시킨다(Higgins and Luthy. 2006; Du et al., 2014; Gagliano et al., 2020). pH가 증가하면 대부분의 흡착제의 표면의 전하가 음으로 하전되거나 양으로 하전된 상태가 약하게 되어 제타 전위(zeta-tential)가 감소하게 되는데(Deng et al., 2012), 이는 과불화화합물과 흡착제 사이에서 강한 정전기적 반발(elcetrostatic repulsion)을 야기시킨다고 보고하고 있다(Du et al., 2014). 반면, 수용액 상의 이온강도는 증가할수록 흡착제의 전기이중층(electrical double layer)의 압축(compression)이 일어나 과불화화합물과 흡착제 사이의 상호작용을 촉진시킨다(Xaio et al., 2011; Du et al., 2014; Gagliano et al., 2020), 이는 pH에 의해 조절되는 정전기적 상호작용을 상쇄시키기도 한다고 보고하고있다(Yang et al., 2013; Du et al., 2014).
소수성 상호작용 또한 음이온으로 하전된 과불화화합물과 음이온상태의 흡착제 사이에서 일어나는 정전기적 반발을 상쇄시킨다고 보고하고 있다(Zhou et al., 2010; Wang et al., 2011; Xaio et al., 2011; Deng et al., 2012; Zhang et al., 2013; Du et al., 2014; Gagliano et al., 2020). 소수성 상호작용은 엔트로피 현상으로 물의 강한 응집력과 물에 의한 반발력으로 비극성 소수성기들이 서로 결합 하는 인력을 의미한다(Chandler et al., 2005; Du et al., 2014). 소수성 결합에 의한 흡착능은 과불화탄소 사슬의 길이에 의해 결정되며, 본 연구 결과에서도 과불화탄소사슬의 길이가 증가할수록 흡착의 세기가 증가한 것을 확인할 수 있었다. 그러나 실제적으로 과불화탄소 사슬은 전형적인 탄화수소와 다르게 소유성(oleophobic)과 친유성(oleophilic)을 함께 지니고 있는 양매-비친화성(amphiphobicity)이기 때문에(Du et al., 2014; Zaggia et al., 2016) 소수성 흡착 결합 반응 내에서 제어가 될 수 있다고 보고하고 있다(Du et al., 2014). 그러나 흡착제의 표면이 소수성 일 경우, 과불화화합물은 수체 내에 잔류하고 있는 것보다 고체상으로 흡착되려는 경향이 강하기 때문에 소수적 특성을 가진 유기물과의 결합은 물론 음으로 하전된 흡착제 표면과의 결합도 가능하다고 보고하였다(Du et al., 2014).
|
Fig. 1 Sorption isotherms of PFCs to soil. |
|
Fig. 2 Biexponential adsorption model for PFCs onto soil. |
|
Table 5 Fitting parameters of a biexponential adsorption model for the sorption of PFCs onto soil |
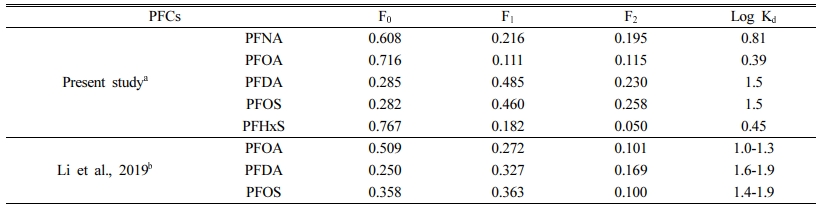
※ a) OM[1.8%], b) TOC[32.8 mg/g] |
본 연구에서는 과불화화합물의 흡착 거동 특성을 평가하기 위해 과불화화합물 14개 항목에 대한 흡착평형배치와 카이네틱 실험을 실시하였고, 14개 항목 중 분배계수를 도출할 수 있는 5개 항목(PFDA, PFNA, PFOA, PFOS, PFHxS)을 선정하여 국내·외 연구결과와 유사성을 비교·검증하였다. 본 연구결과에서는 이전 연구결과와 유사하게 과불화화합물의 탄소사슬의 길이가 증가할수록, 설폰기를 가진 항목일수록 흡착계수 및 평형도달시간이 증가하는 것을 확인하였다. 이는 과불화화합물의 화학적 구조 속성이 토양과 같은 고체상으로 흡착되는 과정에 중요한 요인으로 작용함을 의미한다. 토양 내 유기물은 과불화화합물 흡착 최대용량(capacity)을 결정하며, 이 전 연구결과와 비교를 통해 유기물 함량이 증가할수록 흡착분배비율 또한 증가하는 것을 확인하였다. 그러나 유기물이 흡착 속도를 조절하는 기작에 관해서는 유기물 함량뿐만 아니라 토양 내 유기물의 구조, 구성성분의 비율(휴믹, 펄빅 등), 표면의 광물(mineral)의 함량과 구성비율이 흡착속도를 결정짓는 요인이 될 것으로 사료되며, 추가적인 연구가 진행되어야 한다고 판단된다.
본 논문은 환경부의 재원으로 국립환경과학원의 지원을 받아 수행하였습니다(NIER-RP-2020-220).
- 1. Ahrens, L., 2011, Polyfluoroalkyl compounds in aquatic environment: A review of their occurrence and fate, J. Environ. Monit., 13(1), 20-31.
-

- 2. Ahrens, L. and Bundschuh, M., 2014, Fate and effects of poly- and perfluoroalkyl substances in the aquatic environment: A review, Environ. Toxicol. & Chem., 33(9), 1921-1929.
-

- 3. Brendel, S., Fetter, E., Staude, C., Vierke, L., and Biegel-Engler, A., 2018, Short-chain perfluoroalkyl acids: environmental concerns and a regulatory strategy under REACH, Environ. Sci. Eur., 30:9.
-

- 4. Chandler, D., 2005, Interfaces and the driving force of hydrophobic assembly, Nature, 437(7059), 640-647.
-

- 5. Chen, H., Reinhard, M., Nguyen, V.T., and Gin, K.Y-H., 2016, Reversible and irreversible sorption of perfluorinated compounds(PFCs) by sediments of an urban reservoir, Chemosphere, 144, 1747-1753.
-

- 6. Cheung, W.H., Szeto, Y.S., and McKay, G., 2007, Intraparticle diffusion processes during acid dye adsorption onto chitosan. Bioresour. Tehchnol., 98(15), 2897-2904.
-

- 7. Deng, S., Zhang, Q., Nie, Y., Wei, H., Wang, B., Huang, J., and Yu, G., and Xing, B., 2012, Sorption mechanisms of perfluorinated compounds on carbon nanotubes, Environ. pollut., 168, 138-144.
-

- 8. Du, Z., Deng, S., Bei, Y., Huang, Q., Wang, B., Huang, J., and Yu, G., 2014, Adsorption behavior and mechanisms of perfluorinated compounds on various adsorbents-A review, J. Hazard. Mater., 274, 443-454.
-

- 9. Gagliano, E., Sgroi, M., Falciglia, P.P., Vagliasindi, F.G.A., and Roccaro, P., 2020, Water Res., 171, 113851.
- 10. Groffen, T., Rijinders, J., Verbrigghe, N., Verbruggen, E., Prinsen, E., Eens, M., and Bervoets, L., 2019, Influence of soil physicochemical properties on the depth profiles of perfluoroalkylated acids(PFAAs) in soil along a distance gradient from a fluorochemical palnt and associations with soil microbial parameters, Chemosphere, 236, 124407.
-

- 11. Higgins, C.P. and Luthy, R.G., 2006, Sorption of perfluorinated surfactants on sediments, Environ. Sci. Technol., 40(23), 7251-7256.
-

- 12. Johnson, R.L., Anschutz, A.J., Smolen, J.M., Simcik, M.F., and Penn, R.L., 2007, The adsorption of perfluorooctane sulfonate onto sand, clay and iron oxide surfaces, J. Chem. Eng. DATA, 52, 1165-1170.
-

- 13. Li, F., Fang, X., Zhou, Z., Liao, X., Zou, J., Yuan, B., and Sun, W., 2019, Adsorption of perfluorinated acids onto soils: Kinetic, isotherms and influences of soil properties, Sci. The Environ., 649, 504-514.
-

- 14. Li, F., Duan, J., Tian, S., Ji, H., Zhu, Y., Wei, Z., and Zhao, D., 2020, Short-chain per- and polyfluoroalkyl substances in aquatic systems: Occurence, impacts and treatment, Chem. Eng. J., 380, 122506.
-

- 15. Li, Y., Oliver, D.P., and Kookana, R.S., 2018, A critical analysis of published data to discern the role of soil and sediment properties in determining sorption of per and polyfluoroalkyl substance(PFASs), Sci. The Environ., 628-629, 110-120.
-

- 16. Mattingly, G.E.G., 1974, The Woburn organic manuring experiment: ¥±. Soil analyses, 1964-1972, with special rereference to changes in carbon and nitrogen, Rothamsted Experimental Station Report for 1973, Part 2, pp. 134-151.
- 17. Miao, Y., Guo, X., Peng, D., Fan, T., and Yang, C., 2017, Rates and equilibria of perfluorooctanoate(PFOA) sorption on soils from different regions of China, Exotoxicol. Environ. Saf., 139, 102-108.
-

- 18. Milinovic, J., Lacorte, S., Vidal, M., and Rigol, A., 2015, Sorption behaviour of per-fluoroalkyl substances in soils, Sci. Total Environ., 511, 63-71.
-

- 19. NAAS (National Academy of Agriculture science), 2010, Analysis methods for soil chemical properties. NAAS. Suwon, Korea.
- 20. Oliver, D.P., Li, Y., Orr, R., Nelson, P., Barnes, M., McLaughlin, M.J., and Kookana, R.S., 2019, The role of surface charge and pH changes in tropical soils on sorption behaviour of per- and polyfluoroalkyl substances(PFASs), Sci. Total Environ., 673, 197-206.
-

- 21. Pereira, H.C., Ullberg, M., Kleja. D.B., Gustafsson, J.P., and Ahrens, L., 2018, Sorption of perfluoroalkyl substance(PFASs) to an organic soil horizon-Effect of cation compositiion and pH, Chemosphere, 207, 183-191.
-

- 22. RDA(Rural Development Administration), 2000, Anlytical methods of soil and plant. National Institute Agriculture Science and Technology. Suwon, Korea.
- 23. Walters, F.H., 1991, Design of corrosion inhibitors: use of the hard and soft acid base(HSHB) theory, J. Chem. Edu., 68(1), 29.
-

- 24. Wang, F. and Shih, K., 2011, Adsorption of perfluorooctanesulfonate(PFOS) and perlfuorooctanoate(PFOA) on alumina: Influence of solution pH and cations, Water Res. 45(9), 2925-2930.
-

- 25. Wang, F., Liu, C., and Shih, K., 2012, Adsorption behavior of perfluorooctanesulfonate(PFOS) and perfluooctanoate(PFOA) on boehmite, Chemosphere, 89(8), 1009-1014.
-

- 26. Wei, C., Song, X., Wang, Q., and Hu, Z., 2017, Sorption kinetics, isotherms and mechanisms of PFOS on soils with different physicochemical properties, Exotoxicol. Environ, Saf., 142, 40-50.
-

- 27. Xiao, F., Zhang, X., Penn, L., Gulliver, J.S., and Simcik, M.F., 2011, Effects of monovalent cations on the competitive adsorption of perfluoroalkyl acids by kaolinite: experimental studies and modeling, Environ. Sci. Technol., 45(23), 10028-10035.
-

- 28. Yang, S., Cheng, J., Sun, J., Hu, Y., and Liang, X., 2013, Defluorination of aqueous perfluorooctanesulfonate by activated persulfate oxidation, PLOS one, 8(10), e74877.
-

- 29. Zaggia, A., Conte, L., Falletti, L., Fant, M., and Chiorboli, A., 2016, Use of strong anion exchange resins for the removal of perfluoroalkylated substances from contaminated drinking water in batch and continous pilot plants. Water Res., 91, 137-146.
-

- 30. Zhang, C., Yan, H., Li, F., Hu, X., and Zhou, Q., 2013, Sorption of short- and long- chain perfluoroalkyl surfactants on sewage sludes. J. Hazard. Mater., 260, 689-699.
-

- 31. Zhou, Q., Deng, S., Yu, Q., Zhang, Q., Yu, G., Huang, H., and He, H., 2010, Sorption of perlfluooctane sulfonate on organo-montmorillonites, Chemosphere, 78(6), 688-694.
-

 This Article
This Article
-
2021; 26(5): 20-28
Published on Oct 31, 2021
- 10.7857/JSGE.2021.26.5.020
- Received on Jul 23, 2021
- Revised on Aug 3, 2021
- Accepted on Sep 28, 2021
 Services
Services
Shared
 Correspondence to
Correspondence to
- Sunhwa Park
-
Soil and Groundwater Research Division, National Institute of Environmental Research, Incheon 22689, Korea
- E-mail: parksu@korea.kr