- Stabilization of As and Heavy Metals in Farmland Soil using Iron Nanoparticles Impregnated Biochar
Il-Ha Koh1·Jung-Eun Kim1,2·So-Young Park1,2·Yu-Lim Choi3·Dong-Su Kim3·Deok Hyun Moon4·Yoon-Young Chang3*
1National Environment Lab. (NeLab), Seoul 02841, Korea
2Department of Energy & Climate Environment Fusion Technology, Graduate School, Hoseo University, Asan 31499, Korea
3Department of Environmental Engineering, Kwangwoon University, Seoul 01897, Korea
4Department of Environmental Engineering, Chosun University, Gwangju 61452, Korea- 비소 및 중금속의 식물체 전이감소를 위한 철 나노 입자가 담지된 바이오차의 농경지 토양 안정화제 적용성 평가
고일하1·김정은1,2·박소영1,2·최유림3·김동수3·문덕현4·장윤영3*
1환경기술정책연구원 (NeLab)
2호서대학교 일반대학원 에너지기후환경융합기술학과
3광운대학교 환경공학과
4조선대학교 환경공학과This article is an open access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/4.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
This study assessed the feasibility of iron oxide nanoparticles impregnated with biochar (INPBC), derived from woody biomass, as a stabilizing agent for the stabilization of farmland soil in the vicinity of an abandoned mine through pot experiments with 28 days of lettuce growth. The lettuce grown in the INPBC amended soils increased by more than 100% and the concentrations of inorganic elements (Cu, Ni, Zn) decreased by more than 40%. As, Cd and Pb were not transferred properly from the soils to the lettuce biomass. The bioavailability of arsenic and heavy metals in the INPBC amended soils were decreased by 26%~50%. It seems that the major mechanisms of stabilization were arsenic adsorption on iron oxides, heavy metal precipitation by soil pH increasing and heavy metal adsorption on organic matter. These results revealed that the lower bioavailability of the inorganic pollutants in the soils stabilized using INPBC induced lower transfer to the lettuce. Thus, INPBC could be used as an amendment material for the stabilization of farmland soils contaminated by arsenic and heavy metals. However, a pre-review of the chemical properties of the amended soil must be performed prior to applying INPBC in farmland soil because the concentration of the nutrients in the soil such as available phosphates and exchangeable cations (Ca, Mg, K) could be decreased due to adsorption on the surface of the iron oxides and organic matter
Keywords: Stabilization, Biochar, Iron nanoparticle, Arsenic, Heavy metal
바이오차는 무산소 조건에서 바이오매스를 열분해하여 얻어지는 탄소(C) 함량이 높은 물질이다. 농업이나 축산산업의 부산물과 하수슬러지와 같은 유기성 부산물 등이 열분해 대상 바이오매스가 된다(Lim et al., 2015). 바이오차를 토양에 주입하면 질소(N)나 인(P)과 같은 영양분과 수분의 손실 방지 및 미생물의 생존을 돕는 효과가 있어 농업 생산성 향상 측면에서 많은 관심이 있었다. 이외 기후변화 대응, 에너지 생산, 폐기물 관리측면의 연구와 활용 필요성 역시 제기된 바 있다(Woo, 2013).
최근에는 중금속 오염토양의 개량, 즉 오염토양 안정화를 위한 안정화제로서의 적용성에 대한 연구가 활발하게 이루어지고 있다. 안정화는 토양 내 존재하는 오염물질의 회수가 아닌 토양수분으로의 용출을 낮춰 자연계 내 이동성을 낮추는 공법이다(Kupiene et al., 2008). 안정화는 토양세척과는 달리 공법처리 전후 토양입자의 물리적 특성변화가 없다. 따라서 점토의 존재여부가 중요한 농경지 토양을 대상으로 하는 위해성 기반의 토양처리에 있어서 현실적으로 가장 타당한 방안이라 할 수 있다(Koh et al., 2015). 바이오차는 열분해 대상 바이오매스의 종류에 따라 그 특성에 차이가 있겠지만, 대체적으로 높은 pH, CEC, 풍부한 산소 함유 관능기와 비표면적을 가지고 있어 중금속을 효과적으로 흡착할 수 있다. 따라서 오염토양에 적용 시 구리(Cu), 납(Pb), 아연(Zn)과 같은 양이온 중금속의 이동성을 낮출 수 있다(Bessley et al., 2014; Enaime et al., 2020; Lehmann et al., 2011).
다만, 자연계에서 비산(H2AsO4-, HAsO42-)이나 아비산(H3AsO3, H2AsO3-) 등의 음이온으로 존재하는 비소(As)에 대해서는 안정화 효과에 대한 평가에 차이가 있다. Koh et al.(2016), Kumar et al.(2022), Kumar and Bhattacharya (2022) 등은 각각 단풍잎돼지풀, 오렌지 껍질, 밀짚(wheat straw) 기반의 바이오차로 토양 비소의 이동성을 저감시킬 수 있음을 확인하였다. 이에 반하여 Major et al.(2010), Abdelhafez et al.(2014), Bessley et al.(2014) 등은 비소의 이동성이 오히려 증가하는 결과를 얻었는데, 이는 철(Fe)‧망간(Mn) 산화물로부터의 탈착 또는 pH 및 유효인산의 증가에 기인한 것으로 판단하였다. 이에 비소의 효과적인 안정화 효과 발현을 위해 철산화물이나 영가철(ZVI)을 함유한 바이오차의 적용성을 연구한 바 있다(Choi et al., 2020; Zhou et al., 2014). 바이오차 내 철을 이용한 비소의 흡착 및 이를 통한 이동성 저감효과를 유도하는 것이다(Kim et al., 2014).
이에 본 연구에서는 나노 영가철 담지 바이오차의 비소 오염토양 안정화 가능성을 확인한 선행연구(Choi et al., 2020)의 후속으로 산화철이 함유된 바이오차의 적용성을 검토하였다. 금번 연구는 비소 오염토양 대상의 작물재배 실험을 통해 비소 및 양이온 중금속의 식물체 전이수준과 토양의 화학적 특성변화를 평가함으로써 해당 바이오차의 농경지 안정화제 적용가능성을 확인하는 것이 그 목적이었다. 이러한 연구결과는 향후 비소와 양이온 중금속으로 오염된 농경지를 대상으로 작물생산 관점의 안정화에 관한 참조자료로 활용될 수 있을 것이다.
본 연구에서는 철 나노 입자가 담지된 바이오차로 토양을 개량한 후 포트실험을 통해 오염물질의 식물체 전이와 토양특성 변화를 검토하고자 하였다. 실험은 크게 바이오차의 제조단계와 포트실험 단계로 구분하여 진행하였다.
2.1.바이오차 제조
2.2.1. 바이오매스 준비
바이오차의 주요 원료로 이용될 바이오매스는 경기도 고양시 인근의 폐목재 처리장에서 수급한 전정가지이었다. 전정가지 중 불필요한 협잡물을 제거하고 원통형 교반기를 이용해 3회 물세척한 후 1주일 동안 풍건하였다. 이후 목재용 파쇄기를 이용하여 3 cm 이내의 적절한 크기가 되도록 파쇄하였고, 이를 열분해 전까지 공기가 통하지 않는 용기에 보관하였다(Choi et al., 2020).
2.2.2. 철 나노입자가 담지된 바이오차 제조
전처리된 폐목재를 튜브형 강열기에서 열분해하였다. 열분해 중에는 온도를 상온에서 600oC까지 10oC/min의 속도로 상승시키고 온도가 600oC에 도달된 후 1시간 동안 유지하였다. 본 열분해 조건은 목질계 바이오매스 기반 바이오차에 대한 기존 연구(Yang et al., 2019)를 참고한 것이었다. 열분해 중 바이오매스가 산소와 반응하여 이산화탄소가 되는 것을 방지하고자 강열기 가동 30분 전부터 열분해 이후 온도가 다시 상온이 될 때 까지 질소 가스(N2)를 150 ml/min의 유량으로 강열기의 내부로 주입시켰다. 제조가 완료된 바이오차를 증류수로 수차례 세척하였고, 105oC에서 2시간 동안 건조하였다. 이후 건조된 바이오차(BC, biochar)를 철 산화물 담지 작업 전까지 공기가 통하지 않는 용기에 보관하였다.
바이오차 표면 및 공극에 나노 철산화물을 담지시키기 이전에 질산(HNO3)을 이용한 화학적 산화를 통해 제조된 바이오차의 표면을 활성화하였다(Gu et al., 2019; Jin et al., 2018; Ho et al., 2014). HNO3를 통한 화학적 산화는 바이오차의 표면에 카르복실(-COOH), 하이드록실(-OH) 그룹과 같은 산소함유 관능기를 형성시키고 유‧무기 오염물질에 대한 반응성을 향상시키는 것으로 알려져 있다(Gu et al., 2019; Jin et al., 2018). 바이오차 10 g을 300 mL의 25% HNO3 용액에 넣고 80oC에서 12시간 동안 교반하여 활성화된 바이오차(ABC, activated biochar)를 제조하였다.
상기의 ABC의 표면과 공극에 나노 철산화물이 담지된 Biochar/Fe3O4(INPBC, iron nanoparticles impregnated bio- char)를 제조하고자 하였다. ABC 10 g을 FeCl3와 FeSO4이 각각 24.07 g, 12.01 g(Fe3+:Fe2+=2:1)이 함유된 용액 500 mL에 주입하였다. Fe3+와 Fe2+가 ABC 표면과 공극에 흡착되도록 1시간 동안 80oC에서 교반하였다. 이후 질소 가스를 주입해 질소 분위기를 조성하고 2 M NaOH를 이용하여 pH를 10으로 조절한 후 1시간 동안 반응을 진행시켜 ABC 표면에 Fe3O4가 담지되도록 하였다. 이와 같이 제조된 물질을INPBC로 하였다. 일차적으로 완성된 INPBC의 세척을 위해 원심분리기(ST-16R, Thermo Scien- tific)를 이용해 5000 rpm에서 1시간 동안 원심분리한 후 상등액을 따라내고, 증류수를 넣고 흔든 후 다시 원심분리를 실시하였다. 이를 3회 이상 반복한 뒤 드라이 오븐을 통해 70oC에서 12시간 동안 건조한 후 실험용 분쇄기(IKA, A 11 Basic)을 통해 분쇄하였다. 최종적으로 제조가 완료된 INPBC를 다음 실험까지 공기가 통하지 않는 용기에 넣어 보관하였다.
2.2.3. 바이오차 특성분석
제조가 완료된 INPBC를 대상으로 표면 철 입자의 형태와 BC, ABC, INPBC의 비표면적 및 공극 특성을 분석하였다. 철 입자의 형태는 XRD(X-ray Diffractometer) (D8 Discover, Bruker AXS)을 이용한 결정성 분석으로 진행하였고, 비표면적 및 공극 특성은 ASAP 2420(Micro- meritics)를 이용하여 확인하였다.
2.2. 포트실험
2.2.1. 실험 대상 토양채취
실험 대상 토양은 충북 단양군 소재 폐광산 주변지역의 농경지에서 채취한 것이었다. 채취 시 현장에서 바로 5 mm 체질을 실시한 후 해당 크기 미만의 토양입자를 실험대상으로 하였다. 체질한 토양을 실험실 입고 후 균질하게 혼합하였고, 이후 9일 동안 자연건조하였다.
국내 토양오염공정시험기준(NIER, 2018)으로 분석한 대상 토양의 pH와 비소(As) 및 양이온 중금속(Cd, Cu, Ni, Pb, Zn) 농도를 다음의 Table 1에 나타내었다. 분석결과 실험 대상 토양은 pH 5.9의 산성이며, 비소가 28 mg/kg의 농도로 토양환경보전법에서 제시하는 농경지 우려기준(25 mg/kg)을 초과하였다. 이외 카드뮴, 구리, 니켈, 납, 아연 등의 중금속 항목은 불검출되었거나 우려기준 미만의 저농도로 존재하였다.
2.2.2. 포트조성
실험에 사용된 포트는 지름 10 cm, 높이 9 cm의 소형 크기로, 내부에 건조 토양 400 g을 적재하였다. 안정화 처리한 토양은 토양무게의 0.5%와 1%인 2 g과 4 g의 철 나노입자가 담지된 바이오차(INPBC)를 혼합한 것이었다. 각 처리조건별 3반복으로 구성하여 최종적으로는 대조구(control)를 포함해 총 9개의 포트를 배치하였다. 포트배치 직후 INPBC와 토양 간 안정화 반응을 위해 모든 포트를 대상으로 원토양의 포장용수량 수준을 유지하도록 4일간 1회/일 빈도로 증류수를 공급하였다.
농경지 토양 내 비소 및 중금속의 농작물 전이수준 확인을 위한 식물체로 춘토담적치마를 선정하였으며, 직파방식으로 포트당 60개 전후의 씨앗을 파종하였다. 이후 식물체 채취 시 까지 증류수를 관행살수 방식으로 1회/일 빈도로 공급하였다. 실험기간 동안 증류수 이외의 영양분은 공급되지 않았다.
2.2.3. 시료의 채취 및 분석
포트실험의 분석대상 검체는 식물체(상추) 및 토양이었다. 해당 시료를 상추 파종 후 28일 경과시점에서 채취하였다. 상추는 지표로부터 0.5 cm 이상 이격된 지상부를 시료로 하였다.
상추를 대상으로 비소 및 양이온 중금속 5개 항목(Cd, Cu, Ni, Pb, Zn)의 함량을 식품공전(KMFDS, 2021)에 따라 분석하였다. 현재 국내에서는 벼(쌀)를 제외한 농산물의 중금속 기준을 카드뮴(Cd)과 납(Pb)에 대해서만 제한하고 있다. 상추의 허용기준은 엽채류로서 카드뮴 0.2 mg/kg 이하, 납 0.3 mg/kg 이하이다.
상추 채취 후 포트 내 잔류토양을 대상으로 비소 및 양이온 중금속 5개 항목의 생물학적 유효도(bioavaila- bility)와 토양화학성 항목(pH, 유기물, 유효인산, 교환성 양이온)을 분석하였다. 생물학적 유효도는 1 M NH4NO3 추출법(KS I ISO 19730)을, 토양화학성 항목은 토양화학분석법(NIAST, 2010)에 따른 전처리를 준용하였다.
이상의 과정을 통해 전처리가 완료된 토양 및 식물체 내 무기원소 정량분석은 ICP-OES(model 8300, Perkin-Elmer Inc.)를 이용하였다. 특히, ICP-OES를 이용한 식물체 내 무기원소의 농도정량 시 불검출될 경우 저농도 영역에서 정량이 가능한 ICP-MS(model iCAPQ, Thermo SCIENTIFIC)를 추가 이용하였다. 교환성 양이온(Ca, Mg, K)이나 유효인산 등과 같은 무기원소와 관련한 토양화학성 분석 시 앞서 언급한 ICP-OES와 UV-VIS(model Lamda 25, Perkin-Elmer Inc.)를 이용하여 그 농도를 정량하였다.
|
Table 1 pH and the concentrations of inorganic contaminants of the studied soil |
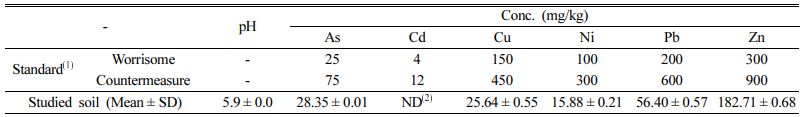
(1) Criteria for agricultural soil from soil environment conservation act of Korea |
3.1. 바이오차 특성
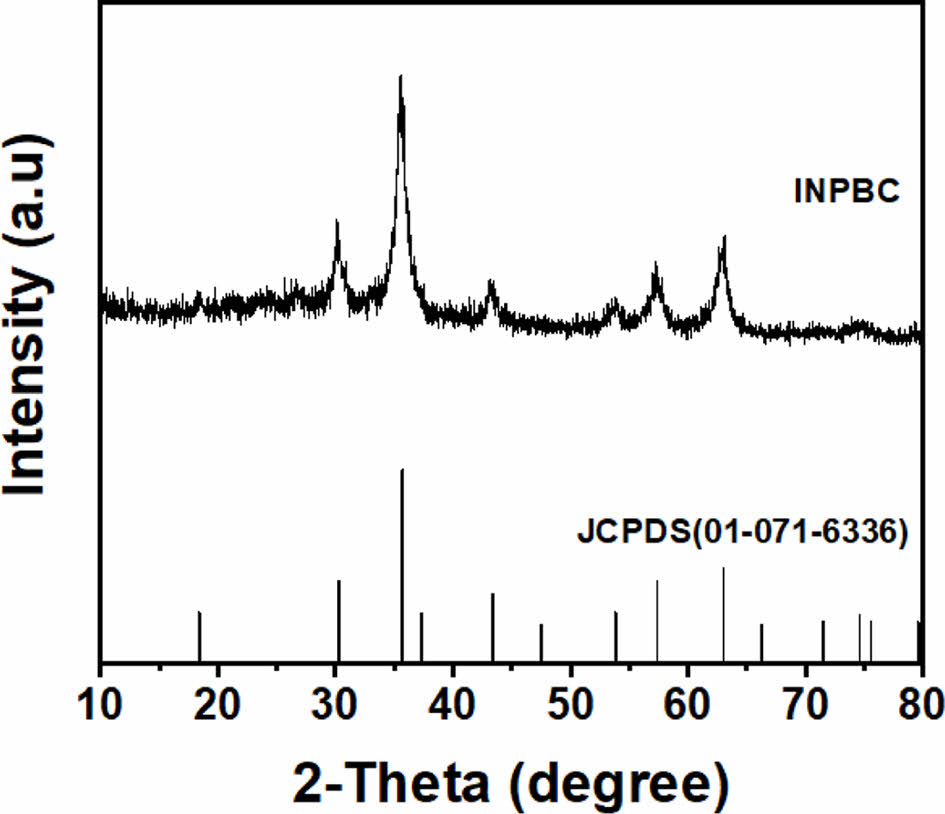
Fig. 1은 INPBC 표면 철 입자의 형태를 알아보기 위해 XRD를 이용한 결정성 분석결과이다. 그림에서 나타난 바와 같이 XRD 패턴은 2-theta 30.13, 35.51, 57.18, 62.98°에서 피크가 형성되는 것을 확인할 수 있다. 이는 JCPDS card(01-071-6366)의 패턴과 일치하며, 따라서 INPBC 표면에 존재하는 철의 형태는 Fe3O4임을 알 수 있다(Sun et al., 2020).
BC, ABC, INPBC의 비표면적 및 공극의 특성을 Table 2에 나타내었다. BC와 ABC를 비교하였을 때 BC의 HNO3에 의한 표면 활성화로 인해 표면적, 총 공극 부피, 평균 공극 크기가 증가한 것으로 나타났다. ABC 표면에 Fe3O4를 담지한 이후 비표면적은 감소하고 총 공극 부피와 평균 공극 크기는 증가하는 것으로 확인되었다. 이는 ABC의 표면에 Fe3O4가 형성되면서 Fe3O4의 비표면적 및 공극 특성의 영향을 받은 것으로 판단된다.
3.2. 포트실험
3.2.1. 식물체 분석
(1) 상추 성장현황
Fig. 2는 파종 후 28일 경과 시점의 상추 성장현황이다. 그림에서 볼 수 있듯이 대체적으로 INPBC 0.5%로 토양을 개량한 조건에서 성장률이 가장 높았고, 대조구(control)에서 가장 낮은 것으로 나타났다. 각 처리조건별 상추 지상부의 평균 무게는 대조구 2.04 ± 1.25 g, INPBC 0.5% 처리조건 6.05 ± 0.29 g, INPBC 1.0% 처리조건 4.14 ± 2.27 g으로 측정되었다. 즉, 토양무게의 0.5% 수준 이상의 철 나노입자 담지 바이오차 혼합처리로 2배에서 3배 가까운 생체량 증가효과를 확인한 것이다. 본 실험대상 바이오차와 같은 목질계 바이오차는 식물체 잎이나 퇴비를 기반으로 제조된 바이오차에 비해 탄소 함량만 높고 이외 질소나 인, 교환성 양이온(Ca, Mg, K)과 같은 영양물질 함량이 낮은 것으로 알려졌다(Singh et al., 2010). 그럼에도 본 실험에서 나타난 결과는 철 나노 입자가 담지된 목질계 바이오차 역시 농업생산성 증대 관점에서 충분한 효과를 가졌음을 나타낸 것으로 볼 수 있다.
다만, INPBC 처리조건별 비교에서는 1% 조건의 생체량이 0.5% 조건에 비해 32% 포인트 가까이 감소하는 결과를 보였다. 이는 분말상의 형태를 가진 바이오차의 특성상 상대적으로 높은 혼합비율에 따라서 배수나 공기의 통로역할을 하는 토양공극을 막아 식물체 생장에 영향을 미쳤던 것으로 판단된다. Yun et al.(2011)의 연구에서도 안정화제로 인한 토양공극 내 공기투과 및 배수조건의 불량화를 확인한 바 있다.
(2) 비소 및 중금속 함량
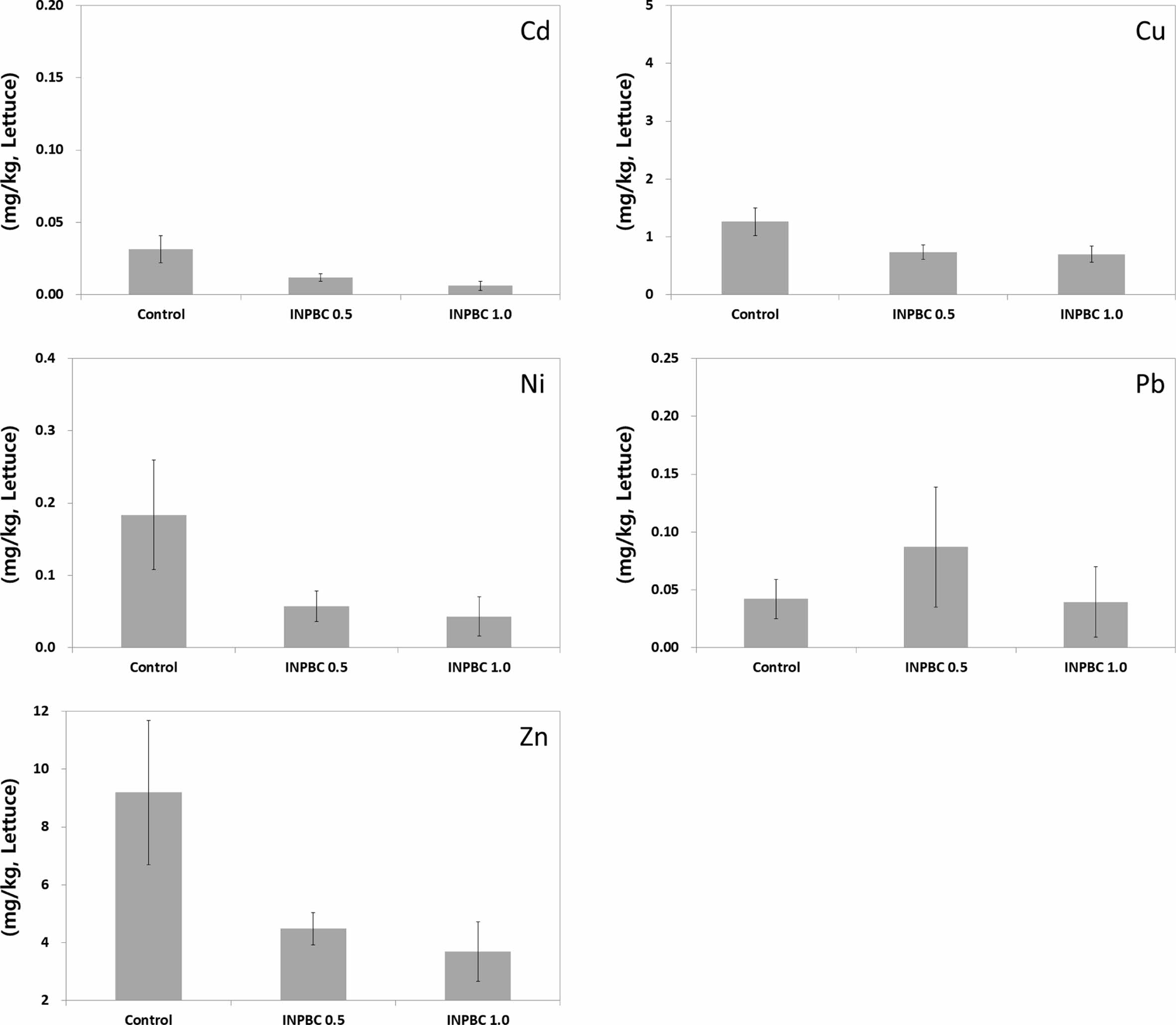
Fig. 3은 포트 상추의 중금속 함량을 나타낸 것이다. 토양 내 우려기준(25 mg/kg)을 다소 초과한 상태로 존재한 비소는 3개 처리조건(control, INPBC 0.5%, INPBC 1.0%)의 9개 포트에서 모두 검출되지 않았다. 이는 비소로 오염된 토양에서 재배된 농작물이라도 가식부의 비소농도는 일반적으로 낮게 나타나며, 분석기기의 검출한계에 가까운 저농도로 관측되는 빈도가 높다는 O’neill (1990)의 보고와 유사한 것이다.
국내 식품의약품안전처의 식품공전에서 허용기준이 설정된 오염물질인 카드뮴과 납은 카드뮴의 경우에만 철 나노입자 담지 바이오차 처리조건에서 대조구 대비 낮은 농도를 나타내었다. 앞선 Table 1에서 확인했듯이 실험대상 토양의 카드뮴 농도는 모두 불검출이었다. 그럼에도 상추에서 카드뮴의 존재를 확인할 수 있었는데, 이는 토양 내에 분석기기(ICP-OES) 검출한계 미만의 저농도으로 존재하는 카드뮴을 식물체 뿌리가 지속적으로 흡수했기 때문으로 보인다. 상추의 카드뮴 농도는 대조구에서 0.032 mg/kg이었으며, 바이오차 처리조건에서 각각 63% 포인트(INPBC 0.5%), 80% 포인트(INPBC 1.0%) 감소한 결과를 나타내었다. 납의 경우엔 바이오차 처리 시 대조구(0.042 mg/kg)와 유사하거나 두 배 이상 증가한 결과를 보였는데, 이때의 농도는 각각 0.087 mg/kg(INPBC 0.5%), 0.039 mg/kg(INPBC 1.0%)이었다. 다만, 본 항목들, 즉 카드뮴과 납의 식물체 농도는 토양의 바이오차 처리에 따른 전이감소 효과를 직접적으로 반영한 결과는 아닌 것으로 판단된다. 앞서 언급했듯이 식품공전에서 설정한 상추와 같은 엽채류의 허용가능 섭취수준은 카드뮴 0.2 mg/kg 이하, 납 0.3 mg/kg 이하이다. 본 실험결과 분석된 상추의 카드뮴과 납 농도는 이에 비하면 10배 가까이 낮은 수준이다. 따라서 해당 시료는 충분히 섭취가능한 수준의 카드뮴과 납을 함유하고 있으며, 토양안정화에 따른 전이감소 효과를 판단하기 위한 전이수준에는 못 미친 것으로 보인다. 아울러 식물체 뿌리가 아닌 지상부 납의 농도로 식물체 전이감소 효과를 판단하기엔 다소 어려움이 있을 수 있다. 이는 일반적으로 토양 납의 대부분이 식물체 지상부에 유효하지 않으며, 뿌리에 집적된 Pb2+의 매우 작은 양만이 지상부로 이행되기 때문이다(Steinnes, 2013).
이외 구리와 아연, 니켈은 바이오차 처리조건에서 모두 대조구 대비 낮은 농도를 보였으며, 바이오차의 투입비율이 높으면 그만큼 전이수준도 낮게 나타났다. 구리와 아연은 식물체 성장의 필수원소이다(Gwak and Yoon, 2011). 따라서 상추 내 농도 역시 다른 어느 항목보다도 높은 보였으나, 바이오차 처리조건에서는 그 농도가 낮게 나타났다. 구리는 대조구(1.259 mg/kg) 대비 40% 포인트(INPBC 0.5%) ~ 45% 포인트(INPBC 1.0%), 아연은 대조구(9.196 mg/kg) 대비 51% 포인트(INPBC 0.5%) ~ 60% 포인트(INPBC 1.0%)의 전이감소효율을 보여 안정화 처리 전 토양 내 농도가 높을수록 전이감소 효과가 더 큰 것으로 확인되었다.
실험대상 토양의 니켈 평균농도는 16 mg/kg로 비소 28 mg/kg보다 낮았음에도 대조구에서 최고 0.184 mg/kg의 수준을 보였다. 바이오차 처리조건에서는 대조구 대비 69% 포인트(INPBC 0.5%), 77% 포인트(INPBC 1.0%) 감소된 농도로 안정화에 의한 식물체 전이감소 효과를 확인할 수 있었다.
3.2.2. 포트 잔류토양 분석
(1) 비소 및 중금속의 생물학적 유효도
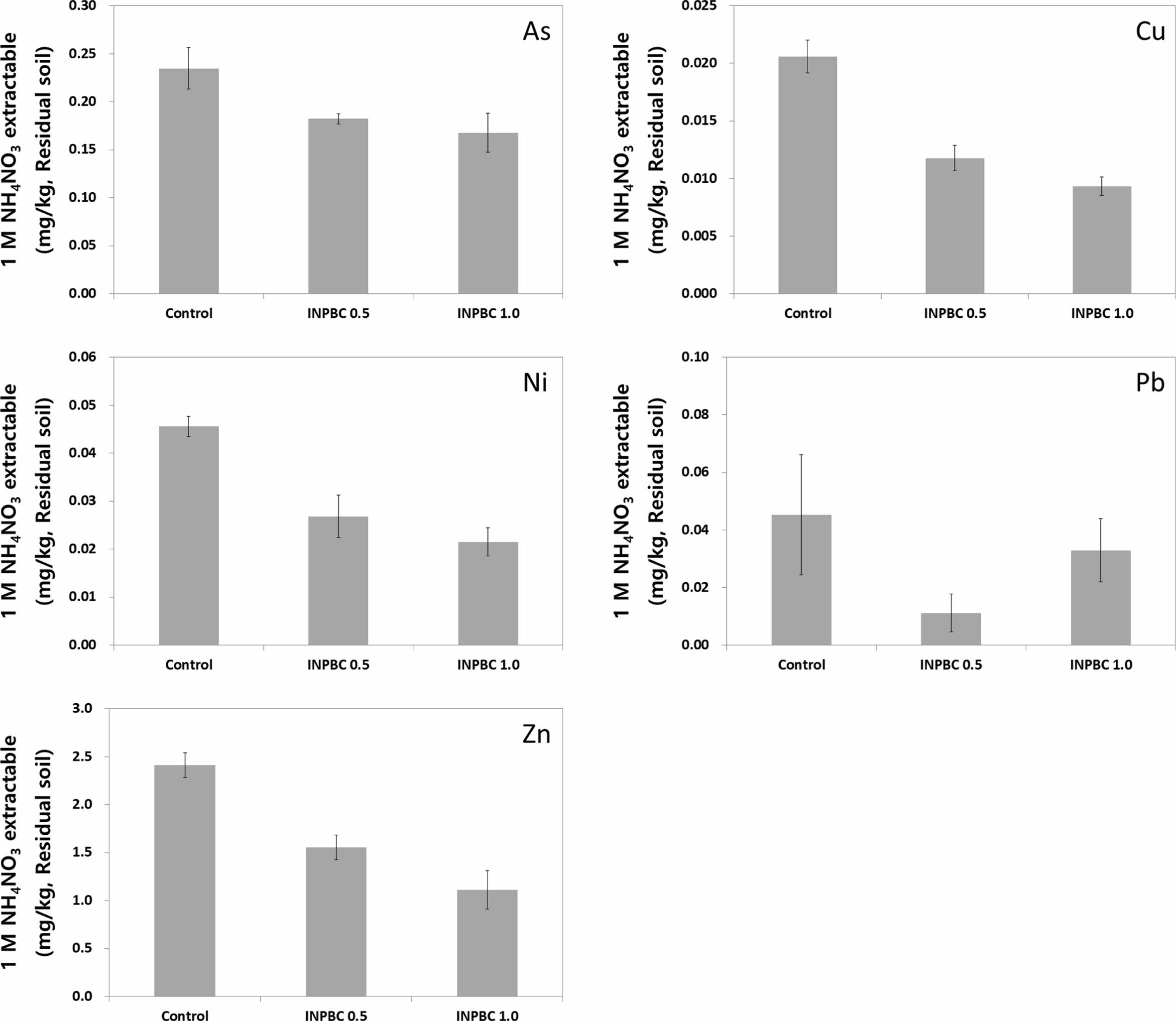
Fig. 4는 실험 종료시점 즉, 상추채취 직후 채취한 포트 내 잔류 토양을 1 M NH4NO3로 추출하여 분석한 비소 및 양이온 중금속의 생물학적 유효도 분석결과이다. Table 1의 실험대상 토양의 오염도 분석결과(왕수추출에 따른 전함량)와 마찬가지로 카드뮴은 모든 시료에서 검출되지 않았다.
비소 및 양이온 중금속의 생물학적 유효도는 그림에서 볼 수 있듯이 철 나노입자가 담지된 바이오차 처리조건에서 대조구 대비 낮게 나타났다. 이러한 결과는 바이오차 적용에 따라 해당 무기원소의 이동성이 낮아진 것으로 풀이할 수 있다. 아울러 앞선 Fig. 2의 상추 내 구리, 니켈, 아연 함량과 비교하면 토양 내 이동성 저감에 따라 식물체로의 전이감소 효과가 있었음을 확연하게 판단할 수 있다. INPBC 0.5% 처리조건에서 가장 낮은 수준을 보인 납을 제외하면 비소 및 중금속의 생물학적 유효도의 수준은 대조구 > INPBC 0.5% > INPBC 1.0%으로 나타났다. 즉, 바이오차 처리량을 높일수록 무기 오염물질의 이동성은 그만큼 낮아지는 결과를 보인 것이다. 따라서 비소 및 양이온 중금속으로 오염된 토양의 안정화 처리 시 철 나노입자 담지 바이오차의 안정화제로서의 적용성은 충분할 것으로 판단된다.
실험대상 토양의 주요 오염물질인 비소의 유효도는 INPBC 처리 시 대조구 대비 26% 포인트 전후(INPBC 0.5% 처리조건 23% 포인트, INPBC 1.0% 처리조건 29% 포인트)로 감소하였다. 이 같은 유효도 감소는 비소가 INPBC 내 철 나노입자 표면으로의 화학적 흡착이 주요 원인 중 하나일 것이다(Wenzel, 2013; Kumpiene et al., 2008). 철산화물의 영전하점(PZC, the point of zero charge)은 pH 6~8로 다양하며, 이중 INPBC 내 철산화물(Fe3O4)의 영전하점은 pH 6.5이다(Evangelou,1998; Fard and Pourghobadi, 2018). 뒤에서 언급하겠지만 실험종료 시점에 측정한 INPBC 0.5%로 처리한 토양의 pH는 6.2이었다. 즉, 영전하점 아래의 토양pH 환경으로 인해 철 나노입자의 표면은 양하전(+)된 상태로 존재했었을 것이다. 따라서 본 실험이 산화상태의 밭토양을 모사한 것임을 고려할 때 토양 내 비산(H2AsO4-, HAsO42-)의 형태로 존재하는 비소를 철 나노입자가 흡착했던 것 역시 주요 원인 중 하나로 판단된다(Zhou et al., 2014).
양이온 중금속인 구리, 니켈, 납, 아연은 철 나노입자 담지 바이오차 처리 시 대조구 대비 50% 포인트 전후의 유효도 감소가 확인되었다. 이는 바이오차 적용으로 인한 토양 pH와 유기물 함량의 증가가 주요 원인으로, 알칼리도 증가로 인한 양이온 중금속의 침전과 음하전된 유기물 표면으로 흡착이 주요 제어기작이었던 것으로 판단된다. 토양 pH와 유기물 함량은 양이온 중금속과 같은 토양 내 미량독성 원소의 식물체 전이에 영향을 미치는 인자로 알려져 있다(Park et al., 2018). 각 항목별 INPBC 처리 시 생물학적 유효도의 대조구 대비 감소율은 구리 43% 포인트 전후(INPBC 0.5% 처리조건 43% 포인트, INPBC 1.0% 처리조건 57% 포인트), 니켈 47% 포인트 전후(INPBC 0.5% 처리조건 41% 포인트, INPBC 1.0% 처리조건 52% 포인트), 납 52% 포인트 전후(INPBC 0.5% 처리조건 76% 포인트, INPBC 1.0% 처리조건 27% 포인트), 아연 45% 포인트 전후(INPBC 0.5% 처리조건 36% 포인트, INPBC 1.0% 처리조건 54% 포인트)로 확인되었다.
(2) 이화학특성
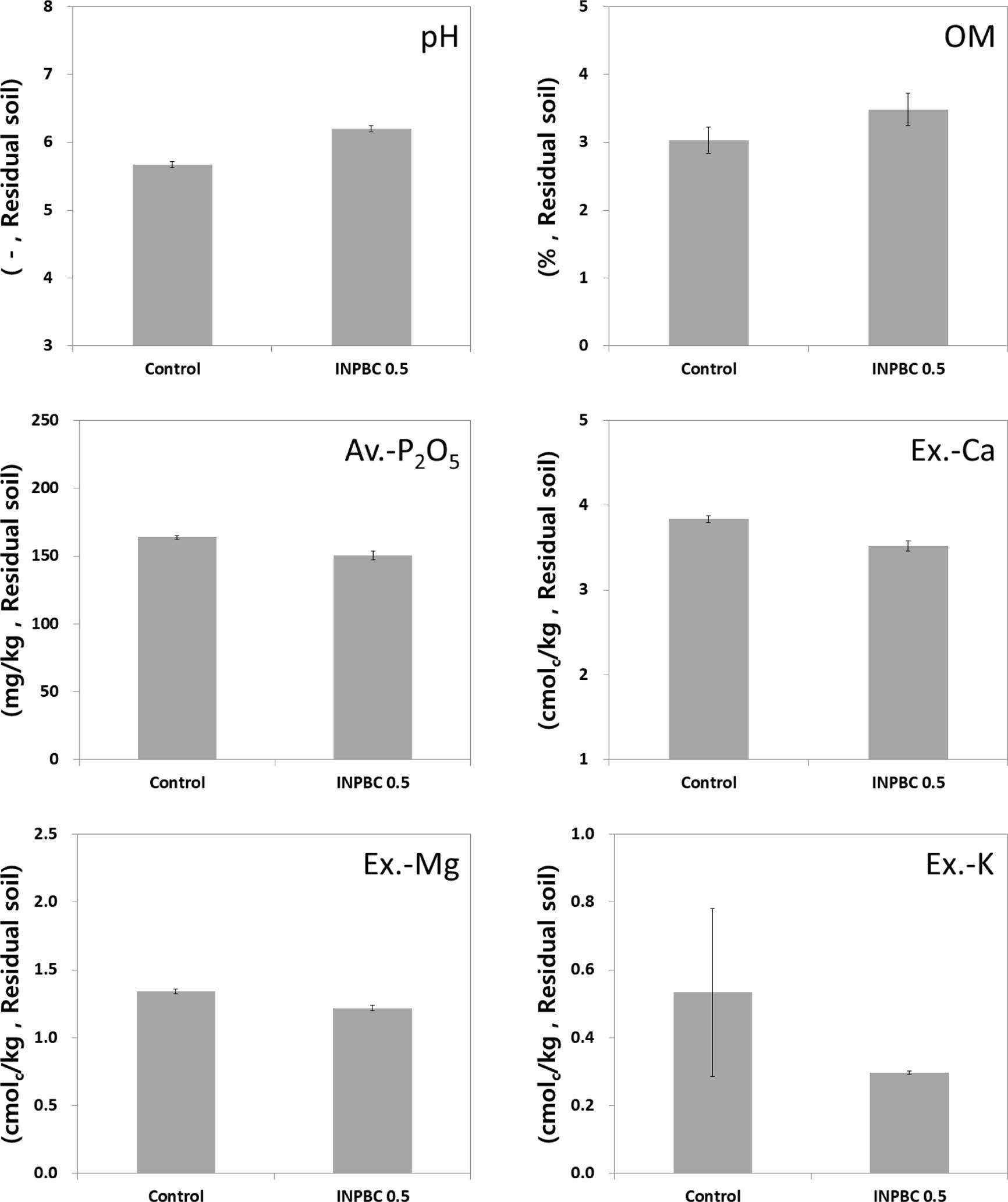
실험종료 시점에서 채취한 포트 잔류토양의 화학적 특성 분석결과를 Fig. 5에 나타내었다. 바이오차를 혼합한 토양의 화학적 특성 검토항목의 분석은 Fig. 2에서 확인했듯이 상추의 성장율이 높았던 INPBC 0.5% 처리조건만을 대상으로 하였다.
앞서 언급한 바와 같이 pH와 유기물 함량은 바이오차 처리 시 증가하는 것으로 나타났는데, 이때의 pH는 대조구 5.7, INPBC 처리조건 6.2, 유기물 함량은 대조구 3.03%, INPBC 처리조건 3.48%이었다. 이 같은 증가양상은 일반적으로 알려진 바이오차의 높은 탄소함량과 알칼리 특성에 기인한 것으로 볼 수 있다. 아울러, 바이오차 표면의 음하전(-)된 관능기(phenolic group, carboxylic group, hyrodxyl group)가 토양 내 수소이온(H+)과 결합해 토양의 pH를 증가시키기도 한다(Gul et al., 2015; Masud et al., 2014). 따라서 양이온 중금속의 토양 내 수산화물 침전이나 유기물 흡착을 통해 생물학적 유효도 저감 및 이로 인한 식물체 전이감소에 긍정적인 영향을 미친 것으로 보인다(Beesley et al., 2014).
유효인산(available P2O5)은 바이오차 처리 시 대조구에 비해 8% 포인트 가까이 감소하는 것으로 나타났다. 인산은 철이온(Fe3+)이나 알루미늄이온(Al3+), 망간이온(Mn2+), 칼슘이온(Ca2+)과 반응하여 침전하는 것으로 알려졌다. 본 실험결과 INPBC 처리조건에서 교환성 칼슘이온이 감소했음을 고려할 때, 바이오차 내부의 철 나노 입자와 반응해 그 유효성이 감소했던 것으로 판단된다(Brady and Weil, 2014). 유효인산은 식물체 성장에 필수적인 영양물질이다. 바이오차 적용에 따른 유효인산 감소효과는 단풍잎돼지풀 기반 바이오차의 연구(Koh et al., 2016)에서도 확인된 바 있는 만큼 향후 농경지 대상의 안정화제로 활용할 경우 식물체 영향에 대한 면밀한 검토가 사전에 수행되어져야 할 것이다.
교환성 양이온 3개 항목(Ca, Mg, K)의 농도는 일반적으로 알려진 바와 다르게 바이오차 처리 시 오히려 감소하는 것으로 나타났다. 이는 본 실험에서 사용한 목질계 바이오차의 특성에 기반한 결과로 판단된다. 앞서 언급했듯이 본 실험대상 바이오차와 같은 목질계 바이오차는 다른 바이오차에 비해 탄소 함량만 높고 이외 질소나 인, 교환성 양이온(Ca, Mg, K)과 같은 영양물질 함량이 낮다(Singh et al., 2010). 따라서 교환성 양이온의 공급량이 높지 않았고, 오히려 기존 토양에 존재한 칼슘 등의 염기 양이온이 음하전(-)된 유기물의 표면에 흡착되었던 것으로 판단된다(Hailegnaw et al., 2019).
|
Fig. 1 X-ray diffraction pattern of INPBC. |

|
Fig. 2 Photograph of lettuce growth at the end of pot experiment ((A) control; (B) INPBC 0.5% amended; (C) INPBC 1.0% amended). |
|
Fig. 3 Concentration of heavy metals in the lettuce plant (As was not detected in all samples). |
|
Fig. 4 Concentration of bioavailable As and heavy metals in the pot soils extracted with 1 M NH4NO3 (Cd was not detected in all samples). |
|
Fig. 5 Chemical properties of the residual soils. |
|
Table 2 BET surface area, total pore volume and average pore width of BC, ABC and INPBC |

본 연구에서는 광산지역 농경지 비소오염 토양의 안정화를 위해 전정가지를 열분해하여 제조한 바이오차에 철 산화물을 주입한 철 나노입자 담지 바이오차의 안정화제 적용성을 28일간의 작물재배를 포함하는 포트실험을 통해 검토하였다. 포트실험 결과 토양 안정화에 따른 비소 및 중금속의 토양 내 유효도 저감 및 식물체 전이감소에 관한 유의한 결과를 확인할 수 있었다.
대상 토양무게의 0.5%와 1.0% 수준의 바이오차를 적용하여 식물체(상추)을 재배한 결과 대조구 대비 2배 이상의 작물 생체량 증가를 확인하였다. 아울러 상추의 비소 및 중금속 함량 분석결과 모든 시료에서 불검출되었던 비소와 식물체로의 충분한 전이가 이루어지지 않았던 카드뮴, 납을 제외한 나머지 구리, 니켈, 아연 항목에서 대조구 대비 40% 이상의 전이감소 효과가 확인되었다. 이 같은 결과는 철 나노입자가 담지된 목질계 바이오차 역시 농업생산성 증대와 오염물질의 작물 전이감소 관점에서 충분한 효과를 가지는 것으로 볼 수 있다.
포트 잔류토양 내 비소 및 중금속의 생물학적 유효도를 1 M NH4NO3로 추출하여 분석한 결과 모든 시료에서 불검출되었던 카드뮴을 제외하면 대체적으로 바이오차의 주입량이 증가할수록 토양 내 유효도가 감소하는 결과를 얻었다. 대조구 대비 바이오차 처리조건의 감소율은 비소 26% 전후, 구리, 니켈, 납, 아연 등의 양이온 중금속은 50% 전후를 보였다. 오염물질의 주요 제어기작은 양하전(+)된 철 나노입자의 표면으로의 비산(H2AsO4-, HAsO42-) 흡착 등을 포함하는 화학적 흡착, 양이온 중금속의 토양 pH 증가로 인한 침전 및 음하전(-)된 유기물 표면으로의 흡착으로 판단되었다. 철 나노 담지 바이오차 0.5% 처리조건 토양의 화학적 특성 검토에서는 대조구 대비 pH와 유기물 함량의 증가, 유효인산과 교환성 양이온(Ca, Mg, K)의 감소가 확인되었다. 교환성 양이온의 감소는 목질계 바이오매스의 특성상 토양에 공급되는 영양물질(N, P, Ca, Mg, K 등) 함량이 낮고, 기존 토양의 교환성 양이온이 음하전(-)된 유기물 표면에 흡착된 것에 기인하였다. 유효인산 역시 바이오차 표면의 양하전(+)된 산화철에 흡착되어 그 유효도가 감소한 것으로 나타났다.
이상의 결과를 통해 철 나노입자가 담지된 바이오차는 비소오염 농경지 안정화 처리 시 작물성장의 위해가 없는 안정화제로서의 적용성이 있음을 확인하였다. 다만, 산화철이 함유된 목질계 바이오차의 특성상 향후 농경지에 적용하기 위해서는 영양물질 유효도 저감에 따른 적정 토양질 유지여부에 대한 사전검토가 필요할 것이다.
본 연구는 중소기업기술정보진흥원의 산학연 Collabo R&D사업인 “양이온 및 음이온계 복합 오염토양의 위해성 확산 방지를 위한 IOHC(Iron Oxide nanoparticles impregnated HydroChar) 기반 조기 안정화 기술 개발(기관과제번호:SS2910834)” 연구의 지원으로 수행되었음
- 1. Abdelhafez, A.A., Li, J., and Abbas, M.H.H., 2014, Feasibility of biochar manufactured from organic wastes on the stabilization of heavy metals in a metal smelter contaminated soil, Chemosphere, 117, 66-71.
-

- 2. Beesley, L., Inneh, O.S., Norton, G.J., Moreno-Jimenez, E., Pardo, T., Clemente, R., and Dawson, J.J.C., 2014, Assessing the influence of compost and biochar amendments on the mobility and toxicity of metals and arsenic in a naturally contaminated mine soil, Environ. Pollut., 186, 195-202.
-

- 3. Brady, N.C. and Weil, R.R., 2014, Elements of the Nature and Properties of Soils, Pearson Education Limited, 490 p., 624 p.
- 4. Choi, Y.L., Angaru, G.K.R., Ahn, H.Y., Park, K.J., Joo, W.H., Yang, J.K., and Chang, Y.Y., 2020, Application of nano Fe0-impregnated biochar for the stabilization of As-contaminated soil, J. Environ. Impact Assess., 29(5), 350-362.
- 5. Enaime, G., Bacaoui, A., Yaacoubi, A., and Lübken, M., 2020, Biochar for wastewater treatment-Conversion technologies and applications, Appl. Sci., 10, 1-29.
-

- 6. Evangelou, V.P., 1998, Environmental Soil and Water Chemistry, John Wiley & Sons, Inc., New York, Chichester, Weinheim, Brisbane, Singapore, Toronto, 151 p.
- 7. Fard, M.R. and Pourghobadi, Z., 2018, The spectrophotometric determination of nystatin in real samples using solid phase extraction based on sodium dodecyl sulphate-coated magnetite nanoparticles, Anal. Bioanal. Chem. Res., 5(2), 249-259.
- 8. Gwak, B.H. and Yoon, K.E., 2011, Plant Physiology, Hyangmunsa, 93 p.
- 9. Gul, S., Whalen, J.K., Thomas, B.W., Sachdeva, V., and Deng, H., 2015, Physicochemical properties and microbial responses in biochar-amended soils: mechanisms and future directions, Agric. Ecosyst. Environ., 206, 46-59.
-

- 10. Gu, S.Y., Hsieh, C.T., Gandomi, Y.A., Yang, Z.F., Li, L., Fu, C.C., and Juang, R.S., 2019, Functionalization of activated carbons with magnetic iron oxide nanoparticles for removal of copper ions from aqueous solution, J. Mol. Loq., 277, 499-505.
-

- 11. Hailegnaw, N.S., Merd, F., Pračke, K., Száková, J., and Tlustoš, P., 2019, Mutual relationships of biochar and soil pH, CEC, and exchangeable base cations in a model laboratory experiment, J. Soil Sediment, 19, 2405-2416.
-

- 12. Ho, P.H., Lee, S.Y., Lee, D.H., and Woo, H.C., 2014, Selective adsorption of tert-butylmercaptan and tetrahydrothiophene on modified activated carbons for fuel processing in fuel cell applications, Int. J. Hydrogen Energ., 39(12), 6737-6745.
-

- 13. Jin, J., Li, S., Peng, X., Liu, W., Zhang, C., Yang, Y., Han, L., Du, Z., Sun, K., and Wang, X., 2018, HNO3 modified biochars for uranium (VI) removal from aqueous solution, Bioresource Technol., 256, 247-253.
-

- 14. Kim, M.S., Min, H.G., Lee, B.J., Chang, S.I., Kim, J.G., Koo, N.I., Park, J.S., and Bak, G.I., 2014, The applicability of the acid mine drainage sludge in the heavy metal stabilization in soils, Korean J Environ Agric., 33(2), 78-85.
-

- 15. KMFDS (Korea Mistry of Food and Drug Safety), 2021, Korean Food Standard Codex.
- 16. Koh, I.H., Kim, E.Y., Ji, W.H., Yoon, D.G., and Chang, Y.Y., 2015, The fate of As and heavy metals in the flooded paddy soil stabilized by limestone and steelmaking slag, J. Soil Groundw. Environ., 20(1), 7-18.
-

- 17. Koh, I.H., Kim, J.E., Kim, G.S., Park, M.S., Kang, D.M., and Ji, W.H., 2016, Stabilization of agricultural soil contaminated by arsenic and heavy metals using biochar derived from buffalo weed, J. Soil Groundw. Environ., 21(6), 87-100.
-

- 18. KS I ISO 19730:2009, Soil quality – extraction of trace elements from soil using ammonium nitrate solution.
- 19. Kumar, A. and Bhattacharya, T., 2022, Removal of arsenic by wheat straw biochar from soil, B. Environ. Contam. Tox., 108, 415-422.
-

- 20. Kumar, A., Bhattacharya, T., Shaikh, W.A., Chakraborty, S., Owens, G., and Naushad, M., 2022, Valorization of fruit waste-based biochar for arsenic removal in soils, Environ. Res., 213, 113710.
-

- 21. Kumpiene, J., Lagerkvist, A., and Maurice, C., 2008, Stabilization of As, Cr, Cu, Pb and Zn in soil using amendments – A review, Waste Manage., 28(1), 215-225.
-

- 22. Lehmann, J., Rillig, M.C., Thies, J., Masiello, C.A., Hockaday, W.C., and Crowley, D., 2011, Biochar effects on soil biota – A review, Soil Biol. Biochem., 43(9), 1812-1836.
-

- 23. Lim, J.E., Lee, S.S., and Ok, Y.S., 2015, Efficiency of poultry manure biochar for stabilization of metals in contaminated soil, J Appl Biol Chem, 58(1), 39-50.
-

- 24. Major, J., Lehmann, J., Rondon, M., and Goodale, C., 2010, Fate of soil-applied black carbon: downward migration, leaching and soil respiration, Global Change Biol., 16(4), 1366-1379.
-

- 25. Masud, M.M., Li, J.Y., Xu, R.K., 2014, Use of alkaline slag and crop residue biochars to promote base saturation and reduce acidity of an acidic ultisol, Pedosphere, 24(6), 791-798.
-

- 26. NIER (National Institute of Environmental Research), 2018, Korea standard methods for soil analysis.
- 27. NIAST (National Institute of Agricultural Science and Technology), 2010, Chemical methods for soil analysis.
- 28. O¡¯neill, P., 1990, Arsenic, In: B.J. Alloway(ed.), Heavy Metals in Soils, John Wiley & Sons, Inc., New York, 93 p.
- 29. Park, M.J., Ji, W.H., Koh, I.H., and Lee, S.H., 2018, Effect of soil factors on crop uptake of toxic trace elements, J. Soil Groundwater Environ., 23(5), 37-44.
-

- 30. Singh, B., Singh, B.P., and Cowie, A.L., 2010, Characterisation and evaluation of biochars for their application as a soil amendment, Aust. J. Soil res., 48(7), 516-525.
-

- 31. Sun, X., Xu, L., Jiang, W., Xuan, Y., Lu, W., Li, Z., Yang, S., and Gu, Z., Adsorption mechanism of rhein-coated Fe3O4 as magnetic adsorbent based on low-field NMR, 2020, Environ. Sci. Pollut. R., 28, 1052-1060.
-

- 32. Steinnes, E., 2013, Lead, In: B.J. Alloway(ed.), Heavy Metals in Soils, Springer, Dordrecht, Heidelberg, New York, London, 402-403 p.
- 33. Wenzel, W.W., 2013, Arsenic, In: B.J. Alloway(ed.), Heavy Metals in Soils, Springer, Dordrecht, Heidelberg, New York, London, 255-258 p.
- 34. Woo, S.H., 2013, Biochar for soil carbon sequestration, Clean Technol., 19(3), 201-211.
-

- 35. Yang, X., Zhang, S., Ju, M., and Liu, L., 2019, Preparation and modification of biochar materials and their application in soil Remediation, Appl. Sci., 9(7), 1365.
-

- 36. Yun, S.W., Kang, S.I., Jin, H.G., and Yu, C., 2011, Leaching characteristics of arsenic and heavy metals and stabilization effects of limestone and steel refining slag in a reducing environment of flooded paddy soil, J. Agric. Life Sci., 45(6), 251-263.
-

- 37. Zhou, Y., Gao, B., Zimmerman, A.R., Chen, H., Zhang, M., and Cao, X., 2014, Biochar-supported zerovalent iron for removal of various contaminants from aqueous solutions, Bioresource Technol., 152, 538-542.
-

 This Article
This Article
-
2022; 27(6): 1-10
Published on Dec 31, 2022
- 10.7857/JSGE..2022.27.6.001
- Received on Oct 14, 2022
- Revised on Oct 24, 2022
- Accepted on Nov 18, 2022
 Services
Services
Shared
 Correspondence to
Correspondence to
- Yoon-Young Chang
-
Department of Environmental Engineering, Kwangwoon University, Seoul 01897, Korea
- E-mail: yychang@kw.ac.kr





