- Review of Analytical and Assessment Techniques of Terminal Electron Accepting Processes (TEAPs) for Site Characterization and Natural Attenuation in Contaminated Subsurface Environments
Yun Sun Song1 ∙ Han-Suk Kim1 ∙ Man Jae Kwon1*
1Department of Earth and Environment Sciences, Korea University, Seoul 02841, Korea
- 오염 지중환경 특성화와 자연저감평가를 위한 말단전자수용과정(TEAPs) 분석 및 평가기술 소개
송윤선1·김한석1·권만재1*
1고려대학교 지구환경과학과
Monitoring and assessing terminal electron accepting processes (TEAPs)
are one of the most important steps to remediate contaminated sites via various
in-situ techniques. TEAPs are a part of the microbial respiration reactions.
Microorganisms gain energy from these reactions and reduces pollutants.
Monitoring TEAPs enables us to predict degradability of contaminants and degradation
rates. In many countries, TEAPs have been used for characterization of field
sites and management of groundwater wells. For instance, US Environmental
Protection Agency (EPA) provided strategies for groundwater quality and well
management by applying TEAPs monitoring. Denmark has also constructed TEAPs map
of local unit area to develop effective groundwater managing system,
particularly to predict and assess nitrogen contamination. In case of Korea,
although detailed soil survey and groundwater contamination assessment have
been employed, site investigation guidelines using TEAPs have not been
established yet. To better define TEAPs in subsurface environments, multiple
indicators including ion concentrations, isotope compositions and contaminant
degradation byproducts must be assessed. Furthermore, dissolved hydrogen
concentrations are regarded as significant evidence of TEAPs occurring in
subsurface environment. This review study introduces optimal sampling
techniques of groundwater and dissolved hydrogen, and further discuss how to
assess TEAPs in contaminated subsurface environments according to several
contamination scenarios.
Keywords: TEAPs, In-situ remediation, Redox reaction, Monitoring, Soil and groundwater
1.1. 지중환경 미생물과 산화환원반응
지중환경은 토양, 지하수 암석 등의 매체가 존재하고 인간이 활용하는 지하시설 및 공간이 다수 존재하는 동시에 다양한 환경적 기능을 같이
수행하고 있다. 토양은 자정작용, 자원 저장 및 이산화탄소 저감 기능 등을 가지고 있으며, 지하수는 없어서는 안 될 수자원이며 수생태계에 중요한
역할을 담당하고 있다. 그러나, 지중환경은 대규모 토목공사와 부적절한 폐기물 매립, 오염유발시설, 폐수배출시설에 의한 오염 등에 의해 지속적으로
오염 및 훼손되고 있다. 지중환경에서 중요한 역할을 하는 미생물은 세균, 방선균, 사상균, 조류, 원생동물을 말하는 것으로, 토양 내 영양물질
순환에 큰 역할을 하고 있다. 토양의 탄소순환에 50% 정도, 분해과정에는 100% 정도 관여할 수 있으며 질소순환의 탈질과정에 60%, 인순환에
90%까지 미생물이 기여할 수 있다고 보고되고 있다(Van der Heijden et al., 2008). 토양 1 g 안에 포함된 미생물 개체
수는 107~109 마리에 육박하며, 미생물의 생체 무게는 토양 유기물 양의 수 %에 달하기도 한다. 생물학적
정화 방식은 지중환경의 풍부한 미생물을 활용하여, 이들이 자발적으로 오염을 분해하도록 유도한다(Kwon et al., 2011; Raynaud
and Nunan, 2014).
산화 환원 반응(redox,
reduction-oxidation)은 원자의 산화수가 달라지는 화학반응이다. 두 반응은 서로 반대작용으로, 한쪽 물질에서 산화가 일어나면 반대쪽에서는
환원이 일어나게 된다. 호흡(respiration)은 산화환원반응의 대표적인 예로서 NO3- 나 Fe3+, SO42- 등 다양한 화학성분을 이용하여
호흡하기도 하는데, 이처럼 산소 외 물질을 사용하여 호흡하는 혐기성 미생물과 산소를 사용하여 호흡하는 호기성 미생물로 구분할 수 있다. 모든 미생물은
전자를
전자공여체(electron donor)에서 전자수용체(electron acceptor)로 전달시켜 에너지를 얻는다. 전자전달계를 통해
전자가 전달되는 과정 동안 전자공여체는 산화되고, 전자수용체는 환원된다. 탄화수소, 토양의 유기물, 환원된 무기물들은 모두 전자공여체로
작용될 수 있는 화합물이다. 전자수용체의 예로는 산소, 질산염, 철(III), 망간(IV), 황산염, 이산화탄소 또는 일부 미생물에서
테트라클로로에틸렌, 트라이클로로에틸렌, 다이클로로에테인, 염화 비닐과 같은 염소계 용매가 사용된다. 이러한 반응은 생물이 에너지를 얻을 수 있도록
할 뿐만 아니라 유기 오염물의 자연적인 생분해에 관여하기 때문에 중요하다(Cozzarelli and Weiss, 2007).
앞서 설명한 바와 같이 미생물마다 사용하는 전자수용체가 다른데, O2를 사용하는 미생물을 ‘호기성 미생물’이라 부르고, NO3-를 사용하는 미생물을 ‘탈질화 미생물’이라고 부른다. Fe3+을 사용하면
‘철환원 미생물’, SO42-를 사용하면 ‘황산염 환원 미생물’, CO2를 사용하여 메탄을 생성하면 ‘메탄
생성 미생물’이라고 한다. 호기성 미생물과 탈질화 미생물은 개체 수도 많고, 밀도도 높으며 활동성이 크지만, 황산염 환원균과 메탄 생성 혐기성
균은 상대적으로 개체 수가 적고 드물다(박용하, 1988). 특정 지중 환경 조건에 따라 주된 호흡 기작에 관여하는 미생물이 달라질 수 있다.
예를 들면, 표토를 포함한 심도가 얕은 대부분의 지역은 호기성 미생물이 가장 활발하고 다양한 반면, 심도가 깊어질수록 질산염 환원 미생물과 철
환원 미생물 그리고 황산염 환원 미생물들이 각각 특정 심도에서 역할을 달리할 수 있고 가장 심도가 깊은 지역에서는 메탄 생성 미생물이 주된 역할을
하는 것으로 보고되고 있다. 이러한 차이는 지중 환경의 수리지질학적 특성과 다양한 전자수용체 분포에 기인하게 된다(Cozzarelli and Weiss, 2007).
또한, 미생물 대사과정 중 널리 알려진 발효(fermenta- tion) 반응의 경우, 산소나 전자전달계를 필요로 하지
않으며 최종 전자수용체로 유기물을 사용한다. 발효의 생성물은 유기산, 가스 또는 알코올이다. 미생물에서 발효는 유기 영양소를 혐기적으로 분해하여
ATP를 생산하는 주요 수단이 된다. 이처럼 발효를 포함한 혐기성 조건에서, 미생물에 의한 유기물(carbohydrates, amino
acids, fatty acids, aromatics) 분해 과정 시 수소 가스가 발생하게 된다. 수소는 환원된 물질로서 전자공여체로 역할을 할
수 있고, 중요한 중간산물(intermediate)로서 말단전자수용과정 단계를 나타낼 수 있는 indicator로서 연구되고 있다(Lovley and Goodwin, 1988).
1.2. TEAPs의 정의, 분석 필요성 및
국내외 활용현황
지중환경에는 전자수용체는 상대적으로 높은 농도로 분포하는 데 반해, 전자공여체는 현저하게 부족하다. 즉, 지중환경은 유기물질 농도가
희박하여 탄소 농도가 매우 낮아지게 되기 때문이다. 석탄층이나 퇴적분지로부터 탄소가 흘러 들어올 수는 있으나 소량에 불과하다. 지중환경은 전자공여체가
제한된 환경(electron donor limited)으로 유지된다(Cozzarelli
and Weiss, 2007).
매립지 내 침출수나 폐기물 저장시설의 오염물 유출로 인해 용존상 유기물질(DOC, dissolved organic carbon)이 지중오염을
일으킬 경우, 전자공여체로 DOC가 공급됨에 따라, 반대로 환경 내 전자수용체가 줄어들게 되어 제한환경(electron acceptor
limited)으로 바뀌게 된다. 유출 초기에는, 가장 개체 수가 많고 왕성한 호기성 미생물이 먼저 오염물질을 차지하여 호흡한다. 호기성 미생물이
번성함에 따라, 곧 지중환경내 산소가 빠르게 고갈된다. 산소 농도가 감소하면 호기성 미생물은 쇠약해지고, 그 이후 혐기성 미생물이 발효나 호흡을
통해 잔류 오염물질을 분해하게 된다(Cozzarelli
and Weiss, 2007; Hwang et al., 2014).
말단전자수용과정(terminal electron accepting process, TEAPs)은 지중환경에서 자연적 또는 인위적으로 발생하는 일련의 미생물 호흡반응(respiration)으로 호기성
호흡, 질산염환원 반응, 철환원 황산염 환원 반응 등에서 에너지를 얻고, 그 과정에서 다양한 오염 물질을 저감시킬 수 있다. TEAPs는 오염지역에서
발생할 수 있는 생지구화학적 반응 종류를 구분하는 데 유리하다(Kwon et al., 2014).
자연적으로 지중환경 내 지하수(deep pristine ground- water)의 경우, TEAPs에 따라 구분할 수 있으며,
나눠진 구역은 일정한 규칙을 나타낸다: Aerobic respiration - Nitrate reduction - Fe/Mn reduction - Sulfate reduction - Methanogenesis(Chapelle, 2001; Cozzarelli and Weiss,
2007; Lovley et al., 1996). 지중환경 내 자연상태의 용존
유기물이 전자공여체가 되고 그로 인해 호기성 미생물이 활발한 대사작용을 통해 개체 수가 증가하여 분해과정에 필요한 산소가 고갈된다. 시간이 경과하고
하부로 내려갈수록 지중환경은 점차 혐기성 환경으로 전환하게 된다. 그때부터 혐기성 미생물이 번성하기 시작하며, 자유에너지가 낮은 화학종부터 호흡
반응이 활성화되어 NO3-, Fe3+, SO42-, CO2 순서로 TEAPs가 나타나게 되는 것이다.
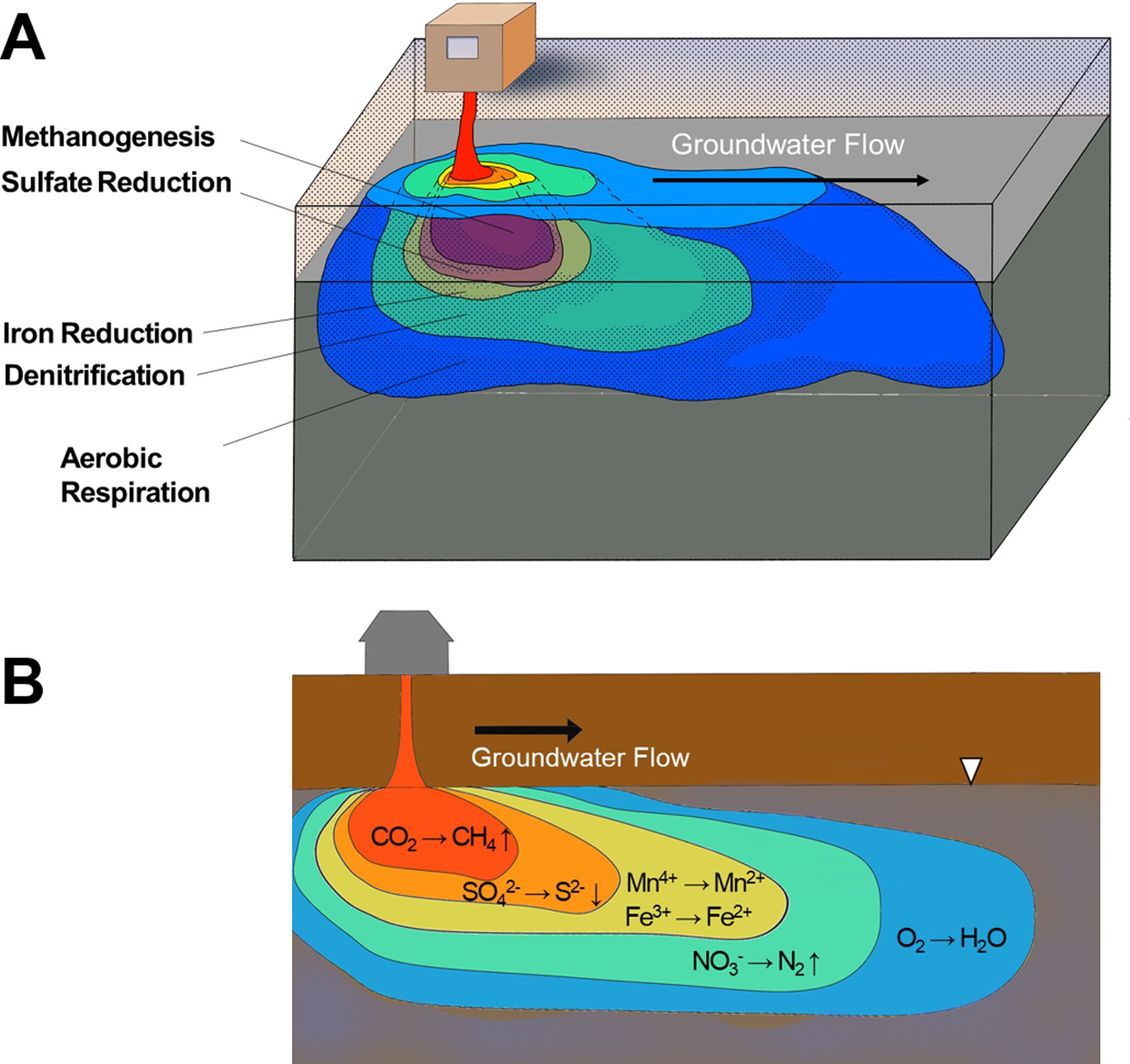
어떠한 해당 지역에서 인위적으로 오염이 유출됐을 때, 자연상태와 반대의 순서로 구역화가 진행된다. 예를 들어 침출수나
기타 유기오염물이 장기간 유출되었을 경우, 지중환경 내 TEAPs는 다음과 같이 특정 순서를 따라 구역화 된다; Methanogenesis →
Sulfate reduction → Fe/Mn reduction → Nitrate reduction → Aerobic respira- tion(Fig. 1A)
(Chapelle, 2001).
침출수 같은 오염물질이 장기간 지하수와 함께 대수층으로 이동하게 될 경우, 오염 유출 지점은 가장 오랫동안 호흡이 일어났으므로 O2를 비롯한 NO3-, Fe3+,
SO42- 등 대다수의 전자수용체가
고갈된 상태가 된다. 따라서 오염 농도가 가장 높은 오염원 중심 부분에서는 CO2를 이용한 메탄 생성반응이
일어난다. 중심 부분의 바로 바깥쪽 부분엔 아직 SO42-가 고갈되기 전이므로 황산염환원
반응이 진행되고, 점차 지하수확산 방향과 함께 철환원 반응구역과 그 다음으로 질산염환원 반응구역이 나타나게 된다(Fig. 1B)
(Chapelle, 2001; Cozzarelli and Weiss, 2007).
TEAPs는 오염물질의 거동과 밀접한 관련이 있는데 확산, 희석, 흡착, 분해 등에 따라 센티미터에서 킬로미터 범위로 나타날 수 있다.
각 지역에서 어떤 반응이 일어나는지 구분함으로써 오염의 분해 여부를 평가할 수 있다. 위에서 언급한 오염물질 거동에 따라 단계별로 TEAPs가
진행되어, 전자 수용체를 이용하는 특정 미생물에 의해 오염 물질 분해가 이루어지기 때문에, 특이적 미생물 모니터링을 통해 오염 저감 수준을 평가할
수 있게 된다(Azadpour-Keeley, 1999).
미국의 오염정화 현장에서의 TEAPs 조사와 평가 사례의 경우, TCE가 주요
오염원이고 석유계탄화수소가 부 오염원인 OO부지의 두 오염물질의 농도는 TCE와 cis-DCE가 최대 300 mg/L과 석유계탄화수소가
수 mg/l 수준으로 심각하게 오염되어 있었다. 초기에 화학적 산화법과 고분자 지질을 이용한 전자공유체 투여를 통한 생물학적 원위치 정화공법이
제안되었으나 화학적 산화의 경우 오염량과 오염범위가 너무 넓어 효과적이지 않아 제외되었다. 생물학적 오염정화를 위해 2011년 고분자량을 가진
전자공여체를 투여했으며, 오염운의 하류 가장자리(downgradient fringes)에서는 완전한 탈염소화(dechlori-
nation)가 되었으나, 전자공여체가 투여된 곳에서는 탈염소화가 전혀 이루어지지 않았다. 이는 오염현장이 고농도 탄화수소류로 오염된
곳이기 때문에 전자공여체(i.e., acetate 3-4 mM)가 이미 충분하였고, TEAPs가 메탄생성반응(i.e.,
dissolved hydrogen 18 nM)까지 진행하여 오히려
탈염소화를 저해하기 때문이었다.
한편, 초기 지중환경조사를 통해 하류지역의 지하수 오염운 가장자리의 경우 트라이클로로에틸렌(trichloroethylene, TCE), 다이클로로에테인(dichloroethylene,
cis-DCE), 염화 비닐(vinyl chloride, VC) 농도가 매우 낮고, 에텐(ethene)의 경우 80%(VC 화학양론 기준)를 차지하는
결과를 보여 완전한 탈염소화가 진행되고 있음을 확인할 수 있었다. 이때 지하수는 저농도의 전자공여체(i.e., acetate
100-200 μM)와 용존수소(1.8 nM) 범위를 보였다. 이러한
사실을 바탕으로 오염원 지역내 비수용상액체(Non-aqueous phase liquids, NAPL)의 양수추출(Pump &
Treat)을 통해 전자공여체 농도를 저감시키는 정화전략이 세워졌다. 정화실행 후 NAPL 질량의 90%를 추출하여 제거하였고, 용존수소 농도를
철(III), 망간(IV), 완전한 TCE 탈염소화를 위한 최적의 범위인 2-4 nM로 감소시켰다. 이후
자연저감을 통해 탈염소화가 성공적으로 이루어지고 있음을 확인하였다(Finneran, 2019). 따라서 이러한 결과는 TEAPs가 오염정화 전략수립과
오염저감 예측에 매우 중요한 판단 근거가 될 수 있음을 시사해준다.
이외에도 지중환경에서 TEAPs 조사가 필요한 경우는 심부에 위치한 관정과 하수관/배수관 등에서 나타나는 문제들에서 찾을 수 있다.
특히, 관정을 부식시키고 막히게 하는 여러 원인이 있는데, 이를테면 오래된 관정이 부식될 경우, 용존 이가철(Fe2+)이 용해되고
산화 작용에 민감하여 악취를 발생시키게 되고 침전물이 형성되기 때문에 배관을 막히게 한다. 혐기성 상태의 유기물로부터 발생하는 황화수소(H2S)도
마찬가지로 역겨운 냄새와 유해가스를 발생시키며, 다양한 화학반응을 거쳐 관정을 부식시켜 수질을 저해할 수 있다(Kwon et al.,
2014). 외국의 경우, TEAPs를 지중환경 조사와 지하수 수질관리에 효율적으로 운영하고 있다. 미국 EPA는 TEAPs 변화를
모니터링하여 지하수 관리 방안을 마련하였으며, TEAPs를 오염 부지의 중요한 특성 중 하나로 보고, 관리항목을 나타내는 indicator로서
분석 연구를 하고 있다(AFCEE et al, 2004). 또한 원위치 생물학적 환경정화(In-situ bioreme- diation),
MNA(monitored natural attenuation) 등 여러 오염정화 기술에서 TEAPs를 분석하고 미생물과의 상호관련성을 평가함으로써,
주요 평가 인자로 연구하고 있다(EPA, 2013). 덴마크는 지하수 내 질소 오염 평가, 예측을 위한 지역 단위 TEAPs 지도를 작성하고 있다(Geological
Survey of Denmark and Greenland, 2019). 지도가 완성되면 덴마크에는 효율적인 지하수 관리체계가 구축될 것으로 보인다.
우리나라의 경우 지중환경을 고려한 오염부지 특성 조사와 방법이 체계적이지 않고, 오염도 측정항목 위주로 조사와 정화설계를 대부분 진행하고
있기 때문에, 지중 정화 효율성이 떨어진다. 그리고 사업 기간이 제한되어 있어서 반출하여 처리하는 비원위치 처리를 선호하기 때문에 충분한 부지특성
조사가 뒷받침되지 못하고 있는 실정이다. 따라서 지중환경을 고려한 원위치(in situ) 정화를 불가피하게 수행하게 될 경우, 조사와 정화설계의
기술 부족으로 인해 정화가 지연되거나, 정화 하자 문제 사례가 적지 않다.
국내의 경우, 최근에는 심부 지중환경 오염 및 지하수 오염 조사와 정화를 위한 기술개발의 중요성을 인지하여 연구개발에 집중하고 있다.
아쉽게도 현재 우리나라는 오염부지 특성화조사를 위한 TEAPs에 대한 이해가 부족한 상황으로 파악된다. 해외의 다양한 TEAPs 분석 사례를 토대로
시료 채취방법과 다양한 TEAPs 지표들을 활용한 종합적인 해석기법이 필요한 상황이다. 따라서 본 논문에서는 TEAPs 샘플링, 분석과 해석방법
등을 체계적으로 정리하여 오염부지 특성조사를 강화하고 지중환경 내 자연 저감과 생물학적 정화설계 인자를 파악하고자 한다. 이를 바탕으로 상세한
지중환경 조사를 통해, 효율적인 지중정화 공법 설계가 가능하게 되고 정화 효율을 향상시킬 수 있다. 또한, 지하수 관정 막힘과 부식 현상을 감소시키고,
유해가스 발생 원인을 규명하고 현상을 예측하여 조기에 예방하는 것도 가능할 것으로 판단된다.
|
Fig. 1 Major terminal electron accepting processes (TEAPs) (A) and their reaction products (B) in contaminated aquifer. |
2.1. TEAPs를 구분하는 데 쓰이는 지표
및 방법
지중환경 내 TEAPs를 분석하기 위해 토양 및 지하수 내 존재하는 다양한 지표들을 활용할 수 있다(Smith and Harris, 2007).
2.1.1. TEAPs 구분 지표
· 탈질화 반응: 탈질화 반응은 질소 기체를 생성한다. 하지만 질소 기체는
쉽게 손실되어 측정하는 데 어려움이 있다. 그래서 반응물인 NO3-를 측정한다.
· 철환원 반응: 반응물인 Fe3+가 광물 형태로
존재하여 샘플링이 불가능하다. 반면에 생성물 Fe2+는 지하수에 용해되어 샘플링이 가능하다. 따라서 Fe2+를
측정한다.
· 황산염 환원 반응: 생성물인 S2-는 철 이온과
침전하는 경향이 있어 샘플링이 거의 불가능하다. 그래서 지하수에 용해되는 반응물인 SO42-이온을 측정한다.
· 메탄 생성 반응: 지하수에 용해된 메탄가스를 측정한다. 정확도를 위해
지중환경의 헨리 상수를 함께 측정한다. 아주 작은 값이지만, 다른 유기 물질에 비하면 메탄의 용해도는 십만 배 정도나 큰 편이다.
· 수소 농도: 수소 농도 수치를 통해 지중환경 환원 반응을 알 수 있다.
현재까지 가장 명확한 기준으로 사료된다. 단, TEAPs를 구역화 할 때 ‘경계 지역’에서는 구분이 어려울 수 있다.
· 유기 탄소의 질량 감소: 분해된 유기 탄소 양을 알 수 있다면, 반응한
양과 반응 속도를 알 수 있다. MTBE, 페놀 물질, CH4 등의 분해를 조사할 때 사용하는
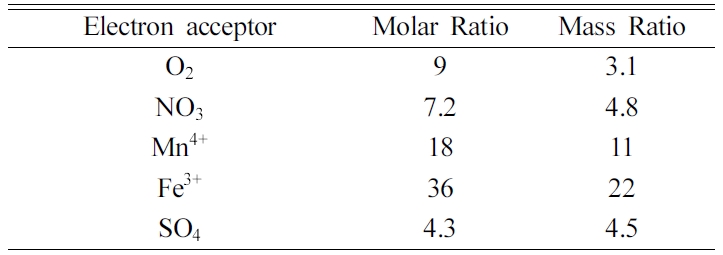
방법이다. 이를 통해 오염운의 이동 속도와 희석 정도를 알 수 있다. 예를 들면, BTEX 고분자 한 개를 완전히 분해하는 데 필요한 전자수용체
비율은 Table 1과 같다.
· BTEX를 완전히 분해하기 위해 필요한 O2, NO3, Fe3+,
SO42-의 비율은 정해져 있다. 그러므로 감소한 전자수용체를 측정하면, 분해된 BTEX의 양도 알 수
있을 것이다. 물론 오염물질의 흡착, 탈착 작용에 의해 오차가 발생하기도 한다.
· 대사작용시 발생하는 부산물 조사: 미생물에 의해 대사작용이 일어나게
되면 부산물도 함께 발생한다. 따라서, 부산물이 존재한다는 것은 생물학적 반응에 의한 분해가 일어났다는 것을 지시한다. 주로 혐기성 미생물 분해반응을
조사하는 데 쓰이는데, 예를 들면, 석유계 화합물로 오염된 대수층 내에서 발견되는 알킬벤젠은 분해되면서 벤조익산, 알킬벤젠산 등의 대사산물로 변하게
된다. 그러므로 하류(downstream)로 갈수록 원래 물질인 알킬 벤젠은 감소하고, 벤조익산, 알킬벤젠산 같은 부산물이 증가할 것이다. 이와
유사하게, 지중내 미생물에 의해 염화 유기용제(chlorinated solvents)의 분해 변환과정을 지시하는 근거로 분해 산물인 ‘딸 생성물(daughter
products)’을 조사하는 방법이 있다.
· 유기물질의 동위원소 비율: 미생물은 가벼운 분자를 먼저 소모하는 경향이
있다. 그래서 분해가 가벼운 분자가 더 빨리 고갈된다. 따라서 반응물에서 가벼운 동위원소가 먼저 감소한다. 이렇듯 물질의 동위원소 비율을 조사하는 것을
CSIA(compound specific isotope analysis)라고 한다. 호기성, 혐기성 반응 모두 적용할 수 있는 조사 방법으로, 탄소뿐만
아니라 다른 전자수용체, DIC(dissolved inorganic carbon) 등을 사용할 수도 있다. 대표적으로 조사하는 동위원소로는 13C/12C,
15N/14N, 34S/32S가 있다.
2.1.2. TEAPs 구분을 위한 현장모사 실험
위의 지표들을 활용하여, 지중 환경과 유사한 조건에서 다양한 현장 및 실내 실험이 가능하다. 어떤 오염 물질의 분해 가능 여부와 촉진제
여부에 따른 진행 양상 등을 관찰하여 복원 프로젝트 방향을 결정할 수 있다.
· Flow-through column: 실험실에서 컬럼 유출액에서 전자수용체,
전자공여체 농도 등 화학 변화를 측정한다. 토양 퇴적물을 Column에 넣고 토양 샘플과 지하수 샘플 둘 다 조사할 수도 있다. 이 데이터를 바탕으로
지중환경에서 일어나는 반응의 종류를 추정할 수 있다.
· 추적자실험: 실험 용액을 대수층에 주입하고 시간, 공간에 따른 변화를
관찰한다. 타겟 물질이 분해되는지 실험한다. 식별용 방사성 동위원소 추적자(radiolabeled tracer)를 사용하면 탈질화
반응 속도를 측정하기 쉽다. 그러나, 수리지질학적 바탕 조사가 시행되어야 하며, 박테리아 분석이 어렵다는 단점이 있다.
· 푸시 풀 시험(single well push pull test):
수리지질학적 정보가 없다면 단일 관정을 이용한 푸시 풀 시험을 수행할 수 있다. 푸시 풀 시험은 추적자시험을 간소화한 것이다. 실험 용액에 분해되는
성분과 보존되는 성분 두 가지를 모두 섞은 후 대수층으로 pulse type 주입한다. 몇 시간~며칠이 지난 후, 시험 용액을 다시 뽑아낸다.
단, 천천히 일어나는 반응과 지하수 흐름이 빠른 곳에서는 측정이 어려우므로 이를 고려해야 한다.
· 원위치 마이크로코즘(in-situ microcosm)테스트: 2 L 정도의 부피가 들어가는
실린더를 대수층 내부에 설치하여 관심 대상 반응 물질을 넣고 미생물, 화학물질 등의 변화를 모니터링할 수 있다. 이 방법의 장점은 실제 대수층
내에서 실험할 수 있다는 것으로 실내 column 실험과는 달리, 현장의 조건을 보다 잘 반영한 데이터를 산출할 수 있다. 또한 추적자시험(tracer
test)과 달리 실험 통제가 용이하다는 장점을 갖고 있다.
위의 네 가지 방법 중에서 flow-through column만 실험실에서 진행하는 방법이고, 나머지 세 방법은 현장에서 진행하는 방법이다.
실험실 진행 방법은 상대적으로 샘플링 하는 과정에서 다른 성분이 섞이게 되거나, 실험실로 옮기면서 시간이 지체될 경우, 미생물 활성이 변하기 때문에
상대적으로 신뢰도가 낮아지게 된다. 이 네 가지 방법 외에도 multiple push pull test를 비롯한 다양한 방법을 고려해 볼 수 있다(Smith and Harris, 2007).
2.2. TEAPs 분석을 위한 지하수 샘플링
기법
지하환경 샘플링은 비용이 많이 들고 고난도 기술이 필요하므로 사전에 철저히 계획을 세워 효율성을 극대화해야 한다. 첫 번째로, 언제,
어디에서 샘플링을 할지 정하고, 제한된 시간과 예산, 연구 목적, 지중 시스템의 복잡도에 따라 절차서를 작성한다. 해당 지형에 대해 기초적인 조사를
진행하고 지질학적, 수리지질학적, 오염의 존재 여부 등 지역의 기초적인 정보를 얻는다. 둘째, 샘플링 스케일을 정할 경우, 환원 반응 구역 분포를
고려하여 간격을 1~10 m 단위로 설정한다. 시간에 따른 분포 변화를 알아보기 위해, 샘플링 빈도를 시간, 주, 월
단위로 설정하고, 지중환경내 심도를 고려하여 샘플 깊이를 설정할 수 있다. 메탄 생성 미생물의 경우엔 깊이 1 m 사이에서도 급격한 변동이
있다(Smith and Harris, 2007).
어떤 샘플을 채취할 것인지도 중요하다. 샘플에는 두 가지 종류가 있는데, 바로 지하수 샘플과 토양 샘플이다. 국내의 경우 지하수 샘플만
채취하는 경우가 대부분이었는데, 지층 샘플은 채취하기가 굉장히 까다롭고 도중에 샘플이 오염될 가능성이 높기 때문이다.
지하수 샘플의 경우 지하수공에서 지하수를 채수한다. 물에 존재하는 박테리아의 종류와 수, 활성도를 알 수 있다. 그러나 여기서 채취된
박테리아는 지하수를 타고 유동적으로 이동하는 자유상 비부착미생물(unattached bacteria)이다. 이러한 자유상 미생물은 지중환경 박테리아
중 10%에 불과하고 90%의 박테리아는 부착미생물(attached bacteria)로서 토양 등 고체 표면에 붙어있다. 그래서 지하수 샘플만으로는
토착미생물에 대한 정보를 얻지 못한다. 반면, 토양샘플에는 토착미생물이 충분히 포함되어있다. 따라서 지중 미생물 분포를 정확히 알기 위해서는 둘 다 샘플링해야
한다(Flynn et al., 2008; Kwon et al., 2018). 최근에는 토양과 지하수 둘 다 샘플링하는 추세이지만, 지하수는
관정에서 샘플링하고, 토양샘플은 코어(core)에서 샘플링을 하게 된다. 하지만 이 방법으로는 각 샘플이 채취된 장소가 다르기 때문에 동일한 환경을
대표할 수 없으므로 조사 및 평가 시 이를 고려해야 한다(Smith and
Harris, 2007).
한편, 지하수 내 TEAPs 분석을 위한 샘플링 시 여러 가지 주의가 필요하다. 지하수 샘플은 민감해서 대기에 노출되거나 금속 물질에
닿으면 쉽게 변한다. 따라서 산소와의 접촉을 피하고, 금속 파이프 등, 금속 물질과 닿지 않게 조심해야 한다. 금속과 닿을 경우, 황산염과 수소
농도가 변할 수 있다. 우선 지하수 관정에 고인 물을 제거해야 한다. 펌핑을 통해 지하수 부피의 최소 3배를 미리 채수하여 버린다. 그리고 부풀어
오르는 패커(inflatable packer)를 관정 내부에 설치하여 펌프(down well pump)를 통해 대기와 관정, 샘플을
효과적으로 격리할 수 있다. Grab 샘플러는 지중환경 압력을 보존하는 기능이 있어 심부 샘플링과 가스 포집(gas laden)샘플에
유리하다. 다심도(small bore multilevel) 샘플러는 정량펌프를 이용하여 산소가 새지 않는 튜브를 통해 가스 누출을 방지해야 하며,
이때 펌핑 속도는 아주 낮게 해야 한다. 또한, 관정에서 직접 샘플링하게 될 경우, 난류가 발생하게 되어 외부 산소가 섞일 수 있으니 주의해야
한다. Table 2에 다양한 샘플링 기술들의 장단점을 정리하였다(Smith
and Harris, 2007).
2.3. TEAPs 분석을 위한 수소 가스 샘플링
기법
지하수의 용존 가스는 Bubble Stripping 기법으로 샘플링 할 수 있다. Bubble Stripping은 수소 가스 샘플링을
포함하여 메탄가스 등 다른 여타 용존 가스에 모두 적용할 수 있다. Bubble Stripping은 헨리 법칙을 바탕에 두고 있다. 기체 상태
수소 농도가 주어지면, 액체 용존 수소 농도를 계산해낼 수 있다. Bubble Stripping에서 가장 많이 쓰이는 두 가지 방법은
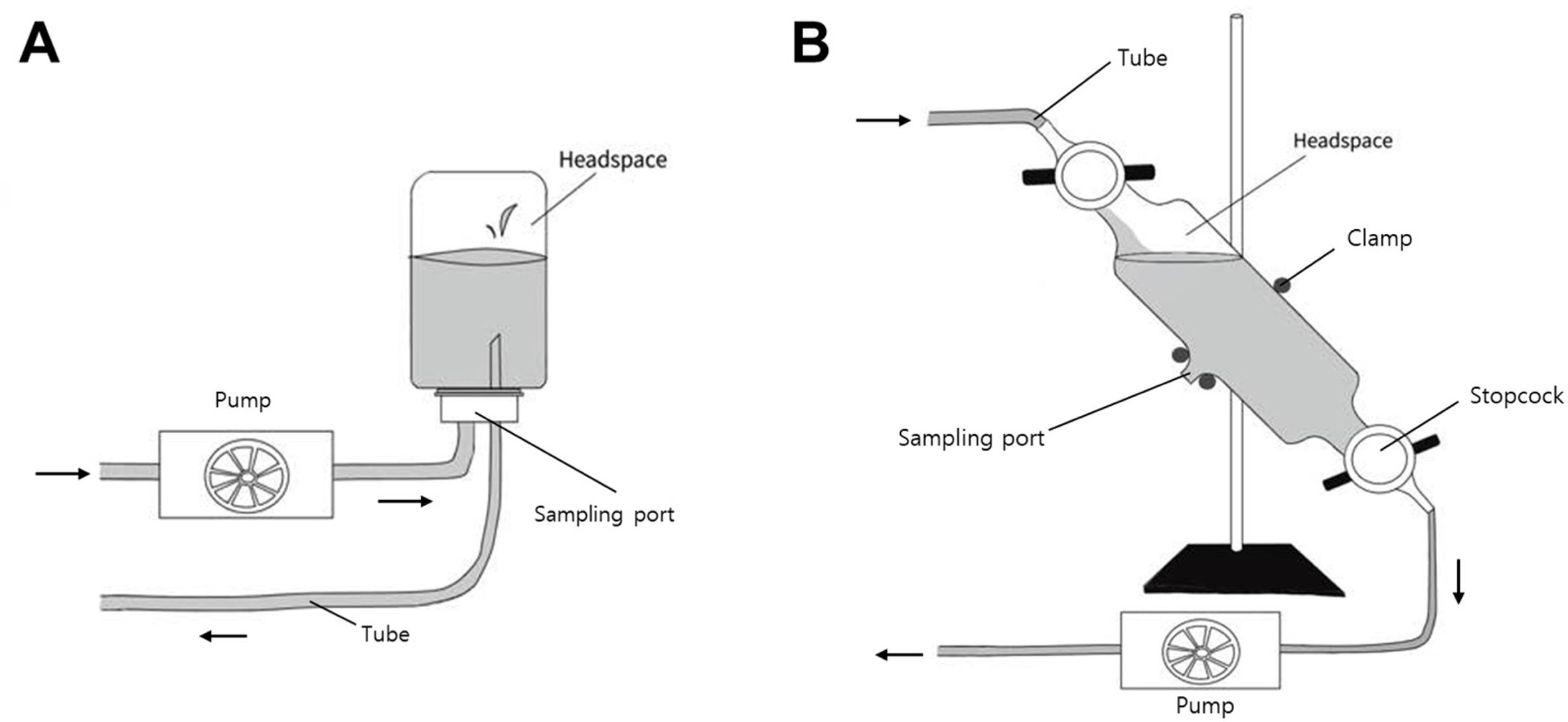
Microseeps cell과 Chapelle cell 이다(Fig. 2A and 2B). Microseeps cell은 간단하고 효율적인 데
반해 Chapelle cell은 다소 복잡하여 Microseeps cell을 많이 사용하고 있다. Microseeps cell과
Chapelle cell 방식은 유리 용기 크기와 펌프 위치에 차이가 있다.
Microseeps cell 설치법은 다음과 같다; 1) 70 ml의 유리용기를 고무마개로
막고, 구멍을 2개 뚫는다, 2) 두 개 구멍에 튜브를 꽂는다, 3) 펌프 하류(downstream)에 유리용기를 설치한다, 4) 유리용기를 스크류
클램프로 링 스탠드에 고정한다, 5) 평형에 도달할 때까지 적절한 시간 동안 펌핑하고 펌프를 끈다, 6) 샘플링은 그때그때 고무마개에 주사기를
꽂아 샘플링 한다.
Chapelle cell 설치는 다음과 같은 순서로 진행한다; 1) 250 ml 유리용기를 준비한다,
2) 정량펌프 상류(upstream)에 유리용기를 설치한다, 3) 유리 용기를 가로로 45o로 기울여 고정하여 스트리핑한다, 4) 평형에 도달할 때까지 적절한 시간동안 펌핑하고 펌프를 끈다, 5)
샘플링 시, 셀을 가로로 눕혀 sampling port가 위를 향하게 한 다음 샘플링한다.
Chapelle cell에서 유리용기를 펌프 상류에 설치하는 이유는, 하류에 설치하면 유리용기 내부가 불안정해지기 때문이다.
Chapelle cell에서는 스탑코크가 어긋나 오류가 생길 가능성이 높다. 장치가 복잡해서 압력이 미세하게 달라지기도 한다.
Microseeps cell이 평형에 더 빨리 도달하고 정확하므로 Microseeps cell을 쓰는 것이 유리하다(Mclnnes and
Kampbell, 2000).
두 가지 Bubble Stripping 방법을 사용할 때 cell 제작 시 재료와 stripping 시간, 유속, 온도 등 다양한 실험
조건을 고려해야 한다. 튜브는 수소 손실이 작을수록 바람직하다. 실리콘이나 폴리에틸렌, 폴리염화비닐(PVC) 튜브는 손실이 거의 없다.
Passive sampling의 경우는 테프론 튜브를 쓸 수도 있다. Passive sampling 시에는 평형을 맞추려면 8시간 걸린다.
PA(polyamide) 튜브는 60% 정도가 손실될 정도로 가스 샘이 매우 심하므로 추천하지 않는다. 튜브는 공극이 적은 재질을 추천한다(Heimann
et al., 2003; Mclnnes and Kampbell, 2000).
수조와 유리 용기의 압력, 대기압은 디지털 마노미터로 측정한다. 그리고 디지털 바로미터로 대기의 절대압력과 온도를 측정한다(Mclnnes
and Kampbell, 2000; Alter and Steiof, 2004). 펌프는 저속양수 펌프(bladder pump)와 정량 펌프가 좋다.
Electric submersible pump(ESP)는 자체적으로 수소를 발생할 오류가 있어 추천하지 않는다. 또한 EPS는 물 온도를 상승시켜
계산이 복잡해지기 때문에 사용하지 않는 것이 바람직하다(Heimann et al., 2003). Stripping 시간의 경우 스트리핑을 오래
할수록 수소 유출이 증가한다. 스트리핑 시간은 평형에 도달하는 데 필요한 시간과 관련이 깊다. 대개의 경우, 30분 경과했을 때 평형에 도달한다(Mclnnes
and Kampbell, 2000). 수소 가스 농도 분석 시 온도가 높을수록 손실이 크기 때문에 실내온도에 대한 고려가 필요하다(Mclnnes
and Kampbell, 2000).
유속 역시 Bubble Stripping을 이용한 수소 가스 농도 분석 시 고려해야 할 중요한 사항이다. 유속이 증가하면,
평형에 빨리 도달하고 이론값에 가까워진다. 또한 짧은 시간에 많은 샘플링이 가능해서 효율이 좋다. 하지만 실험 기구 틈새를 통해 유출이 증가한다는
단점이 있다(Heimann et al., 2003). 유속은 샘플링 장소에 따라 적절하게 설정한다. 어떤 지역은 빠르게 펌핑할 수 있겠지만, 어떤
지역은 어쩔 수 없이 저속으로 펌핑해야 한다. 지역 특성에 따라 가능한 유속에 한계가 존재하므로 상황에 따라 신중히 선택해야 한다. 저속 펌핑만
가능한 지역은 평형에 도달하는 데 매우 오래 걸려 비효율적이다. 하지만 튜브관과 headspace 크기를 조정하여 평형에 도달하는 시간을 단축시킴으로써
효율을 증가시킬 수 있다(Alter and Steiof, 2004).
수소 농도 분석 시 cell에 주입하는 공기 역시 고려해야 할 중요한 사항이 있다. Bubble Stripping 시,
headspace 부피를 유지하기 위해 배경 가스를 계속 주입해야 한다. 하지만 순수 질소, 헬륨 기체는 구하기 번거롭기 때문에 현장에서 사용하기 어려운
문제가 있다. 만약 측정하려는 지하수 수소 농도가 500 ppbv(0.4 nM) 이상이면 주위 공기를
주입하여 사용할 수 있다. 이때는 대기 중 수소가 지하수에 끼치는 영향이 적기 때문이다. 그러나 측정하려는 수소 농도가 500 ppbv 이하면 순수한 질소나
헬륨기체를 주입해야 한다(Alter and Steiof, 2004).
튜브관의 크기 역시 수소 농도 분석 시 고려해야 한다. 얇은 튜브관을 사용하면 평형에 도달하는 시간을 단축시킬 수 있다. 얇은 튜브홀이
평형에 빨리 도달하는 이유는, 압력이 급격히 높아지면서 많은 거품이 생겨 골고루 섞이기 때문이다. 하지만 튜브관이 얇아지면 사용 가능한
최대 유속은 감소하는데, 그 이유는 유속이 너무 빠르면 압력이 높아져 연결 부위를 고장 내기 때문이다. 예를 들면 0.6 mm 튜브관의 최대 유속은
140 ml/min이며 이는 아주 느린 유속에 속한다. 하지만 140 ml/min으로도 이론값에
충분히 도달할 수 있다(Alter and Steiof, 2004).
유리 용기의 headspace에 따라 수소농도 데이터의 정확도, 평형에 도달하는 시간이 달라질 수 있다. Headspace는 5, 10, 20 ml 중 10 ml 조건에서 가장 이론
값에 가까이 도달되는데, 5 ml는 가스와 용액 교환이 잘 일어나지 않고, 20 ml는 혼합이 잘 일어나지
않았다. 10 ml가 가장 적절했고, 이때 유속은 50~140 ml/min이 적당했다.
하지만 평형에 도달하는 속도는 headspace가 작을수록 빠르게 된다. 즉, 5 ml일 때가 가장 빠르며
정확도를 높이고, 샘플링 시간도 단축하려면, 10 ml headspace에
연결된 튜브관을 큰 것으로 교체할 필요가 있다. 그렇게 될 경우, 정확도는 유지하면서, 수소의 교환이 활발히 일어나 속도가 증가하게 되어, 샘플링 시간이
단축된다. 10 ml headspace 상태에서 200 ml/min 유속 조건의
경우, 평형에 도달하기까지 10~15분 밖에 걸리지 않았으며, 다양한 조건과 평형 시간에 대해
여러가지 보고된 바가 있다. 40 ml의 유리용기에서 4 ml headspace,
100 ml/min의 유속으로는 평형에 도달하기까지 20~25분 걸리고 5 ml headspace에
100 ml/min 유속으로는 10~15분 소요된다(Alter and Steiof, 2004).
현장에서 바로 분석하지 못하는 경우에는 샘플을 보관해서 실험실까지 옮겨야 하므로 보관 방법 역시 매우 중요하다. 수소 가스 샘플 보관을
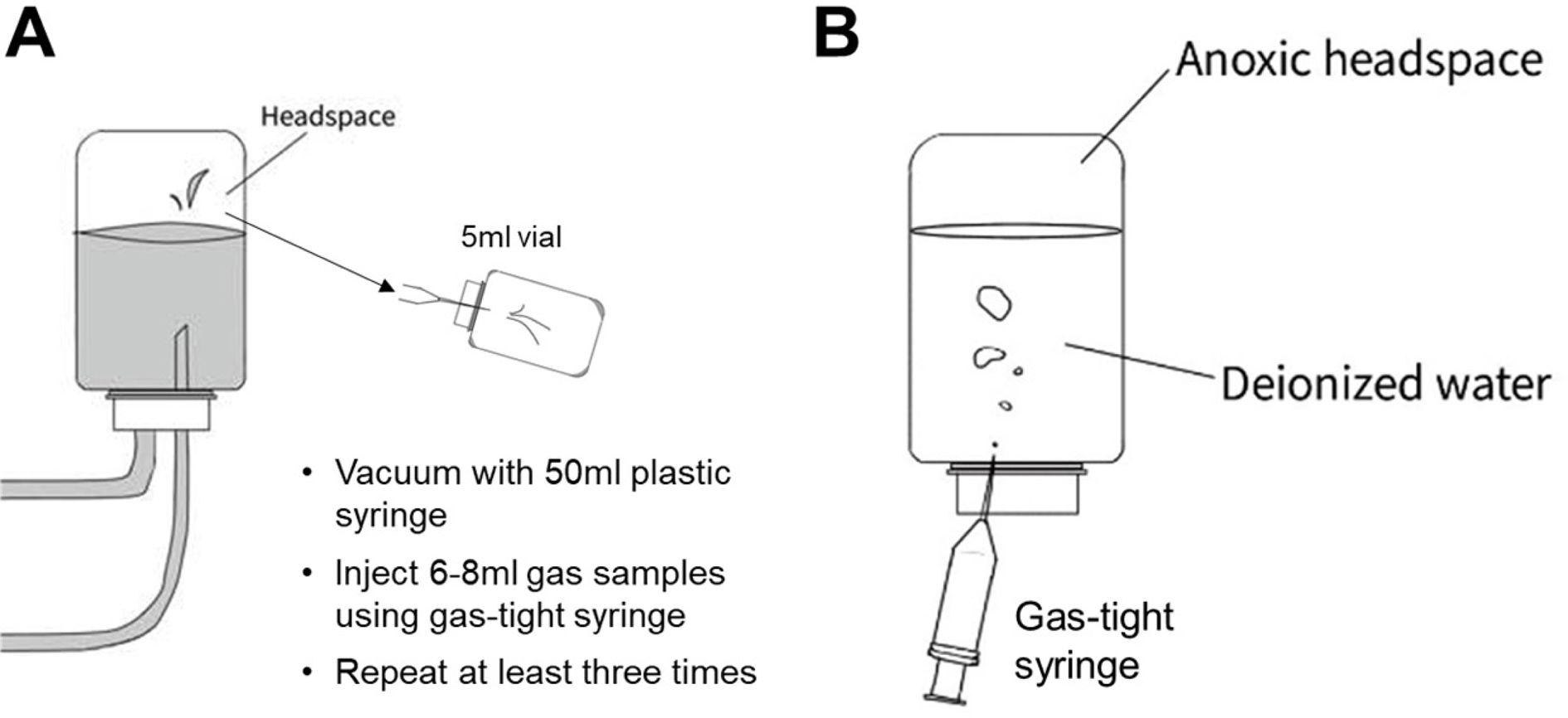
위해 다음의 두 가지 방법이 제안되었다. 첫 번째는 샘플링한 기체를 보관유리용기에 주입했다가 뽑는 과정을 세 번 반복하여(Fig. 3A), 유리용기
내부 잔류한 분자 성분이 차츰 샘플과 유사해지게 하는 방법이다. 완벽한 진공은 현실에서 불가능하기에, 유리용기 내부에 소량의
분자가 남아있을 수밖에 없다. 주입했다가 뽑는 과정을 세 번 반복하면 잔여 물질 성분 조성이 샘플에 100% 정도로 가까워진다(Heimann
et al., 2003).
1) 샘플링 전날, 5 ml 유리 용기를 진공펌프를 사용하여 진공상태로 만들고 PTFE로 코팅한 부틸 고무 스토퍼와
알루미늄 크림프캡(crimp cap)으로 밀봉한다.
2) 샘플링 당일, 현장에서 Bubble Stripping 방법을 이용한 Microseeps cell의 headspace로부터 6 ml를 gas-tight
주사기로 샘플링하여 5 ml 유리용기에 주입한다.
3) 일반 플라스틱 50 ml 주사기를 사용하여 유리용기를 진공상태로 다시 비운다.
4) 6 ml를 gas-tight 주사기로 샘플링하여 5 ml 유리용기에 한번 더
주입한 후 일반 플라스틱 50 ml 주사기를 사용하여 유리용기를 진공상태로 다시 비운다.
5) 최종적으로 8 ml를 gas-tight 주사기로 샘플링하여 5 ml 유리 용기에 주입한다.
유리 용기 내부는 압력이 높은 상태(대략 150~300 hPa)가 된다.
6) 유리 용기를 4oC 햇빛에 노출되지 않은 상태로 실험실로 옮겨 2일 이내에 분석한다.
7) 어둡고 서늘한(약 4oC) 장소에 보관하여 1~2일 내로 분석한다.
두번째 방법은 headspace 유리 용기를 이용하여 보관하는 방법이다. Headspace 유리 용기는 가스 누출을 방지하기 위해 거꾸로 세워 보관한다(Fig.
3B) (Alter and Steiof, 2004).
1) 유리 용기를 고무 septa로 막고 탈이온수로 가득 채운다.
2) 10 ml의 가스 샘플을 주사기를 통해 headspace 유리 용기에 주입한다.
3) 어둡고 서늘한(약 4oC) 장소에 거꾸로 세워 보관하고 1~2일 내로 분석한다.
4) 분석할 때는 1 ml의 초순수수를 주입하고, 1 ml 샘플을
gas-tight 주사기로 뽑아낸다. 이때 Headspace 유리용기 내부 압력이 대기압보다 높아야 한다.
위에서 소개한 두 방법을 적용하면 수소 가스 샘플을 보관할 수 있으며 이때 서늘하고(약 4oC) 어두운 환경에서 보관하는
것이 중요하다. 그러나, 정확한 분석을 위해서는 보관 후 1~2일 이내로 최대한 빨리 분석하는 것이 바람직하다(Heimann et al.,
2003; Alter and Steiof, 2004).
|
Fig. 2 Schematic diagrams of pump and jar in Microseeps cell (A) and pump and gas sample bulb in Chapelle cell (B) for gas sampling in groundwater. |
|
Fig. 3 Schematic diagrams showing how to store gas samples into an empty vial (A) and a headspace of the vial with deionized water (B) with syringes. |
|
Table 1 Stoichiometric ratio of electron acceptors required to biodegrade a unit mass of BTEX |
3.1. 화학성분 농도를 바탕을 한
TEAPs 분석
3.1.1. 호기성 호흡
호기성 호흡은 용존산소량(dissolved oxygen, DO)을 통해 직관적으로 판단할 수 있다. 지하수 DO 농도가 50 mM 이상이면, 그 지역 TEAPs는 호기성 호흡으로 간주할 수 있다. 용존산소 농도가 30 mM 이상이면 윙클러 적정 또는 산소 전극으로 분석하고, 30 μM 이하이면
Ampoulated Rhadazine-D procedure를 사용할 수 있다(Smith and Harris, 2007).
3.1.2. 탈질화 반응
질산염(NO3-)은 탈질화 반응을 일으켜 질소기체(N2)를 생성한다. 아질산염(NO2-)이
중간물질로 생성될 수 있어 지하수 내에 NO2-, N2가 NO3-와 공존하고 있다면, TEAPs를 탈질화 반응으로 판단할 수 있다. 만약 지하수 N2
농도가 대기 중 농도보다 높으면 확실히 탈질화 반응이다. 지하수 흐름 방향으로 조사하는 방법도 있다. 탈질화 반응이 일어나면 지하수 흐름을 따라
NO3- 가 감소하고, 동시에 N2 농도는 증가한다. 동위원소를 이용할 수도 있다. 생물학적 마이크로코즘 배양을 통해 탈질화 반응을
검사하는데, Acetylene blockage technique과 15N tracer를 사용한다(Smith and Harris, 2007).
3.1.3. 철 환원 반응
먼저 생물학적으로 이용 가능한(bioavailable) Fe3+와 철환원 미생물이 모두 존재하는지 확인한다. 이
두 가지를 우선 확인하고, 그 다음 Fe2+를 조사한다. 오로지 비정질, 덜 결정화된 Fe3+만이 호흡반응에
참여하기 때문에, 생물학적으로 이용 가능한 Fe3+만을 구분해서 분석해야 한다(Hwang et
al., 2014; Kwon et al, 2014). Fe3+는 0.5 M HCl과
Ti(3)-EDTA를 통해 측정한다. 마이크로코즘 배양에서 Fe2+가 생성되면 생물학적으로 이용 가능한 Fe3+와
철 환원 미생물이 모두 존재한다는 의미이다. 용해된 Fe2+는 ferrozine colorimetric 검정을 통해 분석한다(Stookey, 1970).
3.1.4. 황산염 환원 반응
황산염 이온(SO42-)과 HS-, H2S, FeS과 같은 황화물이 지하수에 함께 나타나면 황산염 환원 반응이
일어난다는 증거이다. SO42-의 존재 또는 농도만으로는 황산염 환원 반응의 존재유무를 확인할 수 없다. 해수가 침투한 지역에는
황산염 환원 반응이 일어나지 않아도 SO42- 가 풍부하기 때문이다. 따라서 다른 황화물이 공존하는지 확인하고 이에 더해, 수소 농도를 반드시
확인해야 한다. 그 이유는 황철석과 같은 황화광물이 풍부하면, 광물이 용해하여 황화물을 생성하기 때문이다. 황철석도 HS-,
H2S, FeS를 생성하기 때문에 황산염 환원 반응이 일어나지 않았는데도 혼동될 수 있다. 따라서 황산염 환원 반응을 확인하는데
수소 농도를 반드시 참고하도록 한다. 또한 동위원소 분석, 비색법을 활용하거나, 배양할 경우 [35S]와 식별용 방사성 동위원소
추적자를 사용할 수 있다. 또한, 미생물 개체수 측정법, 미생물 분리배양 방법을 사용할 수 있다(Smith and Harris, 2007).
3.1.5. 메탄 생성 반응
메탄은 지층 내 흔한 물질이다. 퇴적 분지, 광산, 석탄층에 풍부하여 어디서든 유입되기 때문에, 메탄이 있다는 이유로 섣불리
TEAPs를 메탄 생성 반응으로 확정하면 안 된다. 메탄은 수소 가스와 마찬가지로, Bubble Stripping과 가스크로마토그래피를 사용한다.
메탄에는 두 가지 종류가 있다. 열로 발생한 메탄(thermogenic)과 미생물이 생성한 메탄(biogenic)이다. TEAPs 조사에 필요한
것은 미생물이 생성한 메탄이다. 메탄 생성 반응이 진행 중인지 조사하기 위해 지하수 샘플의 두 메탄을 구분해야 한다. 두 메탄의 차이점은 탄소
동위원소 비율이다. 열로 발생한 메탄에는 13C가 더 풍부한데, 미생물 발생 메탄보다 13C가 58% 정도
더 많다. 메탄 농도를 잴 때는 core material을 혐기성 headspace가 있는 밀폐된 용기에 보관한다. 그러면 장기간 보관할 수 있다.
만약 지층에 유기 오염 물질이 너무 많을 경우, 메탄이 과도하게 생성될 수 있다. 그러면 지하수 메탄 농도가 너무 높아져 민감한 증감을 찾아내기
어려울 수 있다. 이럴 경우, Headspace를 조금 제거하여 농도를 줄이면 보다 정밀하게 측정할 수 있게되고, 메탄 생성 미생물의 존재 여부도
알아볼 수 있다(Smith and Harris, 2007).
3.2. 용존 수소 농도를 바탕을
한 TEAPs 분석
Bubble Stripping 방법으로 용존 수소 가스 샘플을 채취한 후 기체크로마토그래피(gas chromatograph, GC)와
reduction gas detector(RGD)를 사용하여 수소 농도를 측정할 수 있다. 한편, 수소 농도 값을 샘플링할 때마다 기록하고, 측정값이
안정해질 때까지 계속 샘플링 해야 한다. GC 컬럼은 5 Å, 1.5 m × 2 mm 사용하고, 실온에서
측정하며 이동상 기체는 헬륨을 사용한다. 측정한계(Limit of Detection)는 0.05 mM 이었다(Chapelle and McMahon, 1991). 헨리 법칙을 사용하여 기체
상태 데이터를 통해 용존 농도를 계산할 수 있다. 예를 들어 1기압 대기 농도가 0.8 ml/l일 때, 용존 수소
농도는 1.0 nM 이다.
4.1. 지하수 용존 성분을 바탕으로
한 TEAPs 평가
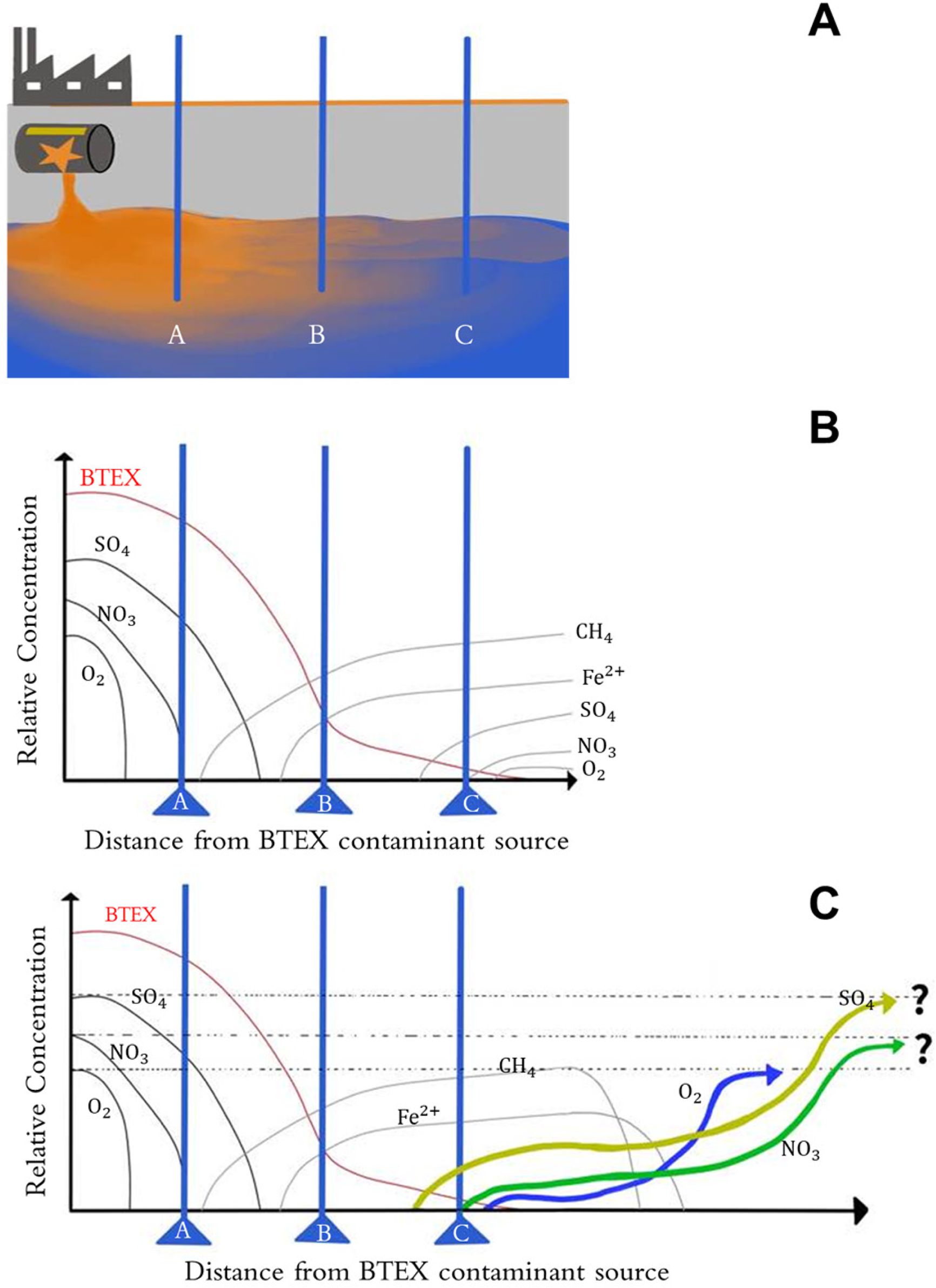
전자수용체, 또는 환원 반응의 생성물을 활용하여 TEAPs를 확인할 수 있다. 오염사고로 인해 BTEX가 유출되어 지하수를 따라 일정하게
흘러간다고 가정하고 몇 달에서 수 년 등 충분한 시간 지났을 때 관정 A, B, C에서 지하수를 샘플링하여 성분 조사를 한다고 가정하였다(Fig.
4A). 관정 A에서부터 B, C로 갈수록 BTEX 오염원으로부터 거리가 멀어진다. 유출 지점에서부터 지하수를 추적하여, 시간에 따른 성분 변화를
그래프로 나타냈다(Fig. 4B). 관정 A에서는, BTEX 농도와 다른 전자수용체 농도가 함께 감소하고 있다. 호흡 작용으로 BTEX가 분해됨과
동시에 전자수용체가 빠르게 소모된다. 산소가 가장 빠르게 고갈되고, 그다음 NO3가 고갈되었다. A에서의 TEAPs는 SO42- 가 가장 많으므로 황산염 환원 반응이 우세하리라 판단하기 쉽다. 그러나, A는 NO3- 농도가 0으로 수렴하고 있는 지점이자, SO42-도 감소하는 지점으로 탈질화 반응과 동시에 황산염환원 반응도 일어나고 있다. 즉, A는 황산염환원
반응과 탈질화 반응의 경계 부근에 위치한다. 관정 B에서는 다량의 CH4, Fe2+와 소량의 BTEX가
검출됐다. 그동안 메탄 생성 반응으로 CH4가 축적되어 농도가 높다. Fe2+도 축적 효과로 농도가 점진적으로
증가한다. 다른 전자수용체가 거의 없고 CH4가 가장 많으므로, B 지역의 TEAPs는 메탄 생성 반응이라고 판단할 수 있다.
관정 C는 BTEX 오염원으로부터 가장 멀다. 그동안 BTEX가 거의 다 분해되어서 농도가 희박하다. 관정 C에서는 다양한 이온이 검출된다. 다량의
CH4와 Fe2+, SO42-, 그리고 소량의 NO3-와 O2가
있다. CH4가 많으므로 TEAPs를 메탄 생성 반응으로 오인할 수 있는데, C에서는 메탄 생성 반응이 완만한 기울기로 진행되고
있다. 다시 말해, 매우 천천히 일어나는 중이다. 해당 지점에서 메탄 생성 반응이 TEAPs라고 하기에는 불확실하다. 아울러, NO3-, SO42- 가 검출됐다고 해서 탈질화 반응, 황산염 환원 반응이 진행한다고 평가할 수는 없다. 또한
Fe2+의 존재 자체는 철 이온 환원 반응이 일어나고 있거나, 그 전에 일어났음을 의미하지만, 현재 상황에 대한 명확한 정보를
제공하지는 않는다. 따라서 C의 경우에는 판단하는 과정에서 혼란이 올 수 있으므로 주의해야 한다.
C 지점에서 더 지하수 흐름 방향으로 진행하게 되면 O2, NO3-, SO42- 가 검출될 수 있는데 그 이유는 주변 지하수에 존재하는 O2, NO3-, SO42-와 평형을 이루기 때문이다(Fig. 4C). 즉, BTEX 오염물질은 C 지점 부근에서 대부분
분해되어 미생물에 의한 호흡반응이 미미해지고, 주변의 깨끗한 지하수와 혼합되어 평형을 이루게 된다. 이상의 예에서 보듯이 TEAPs는 간단해 보이지만
막상 평가할 때는 혼동을 빚을 수 있다. 지중환경은 복합적이고 지질학적, 수리지질학적 요인이 얽혀 있기 때문이다. 도식에 표시한 것처럼
화학 반응 구역의 범위가 명확하게 구분되지 않고 점진적인 전이가 일어나기 때문에 판단이 더 어려워진다. 따라서 NO3-와 SO42- 등 대표 성분만 가지고 판단하면 오류가 생길 수 있고, 환원
산물이 축적되어 경계 지역에서 심각한 착오를 일으킬 수 있다(EPA, 2017)
4.2. 자유면 대수층, 피압 대수층
오염에 따른 TEAPs 변화 평가
관정 A, B, C를 거쳐 지하수의 오염 물질 농도는 점점 감소하다 비오염지대에 진입하였을 때 비오염지대에 진입한 지하수 성분과
TEAPs 변화를 아래에 두 가지 시나리오에 기반하여 평가하였다. 첫 번째는 자유면 대수층의 환경, 두 번째는 피압 대수층의 환경이다(Fig.
5). 이러한 시나리오 평가는 수많은 사례 중 일부일 뿐이며 다양한 지중환경 사례에 응용될 수 있을 것이다.
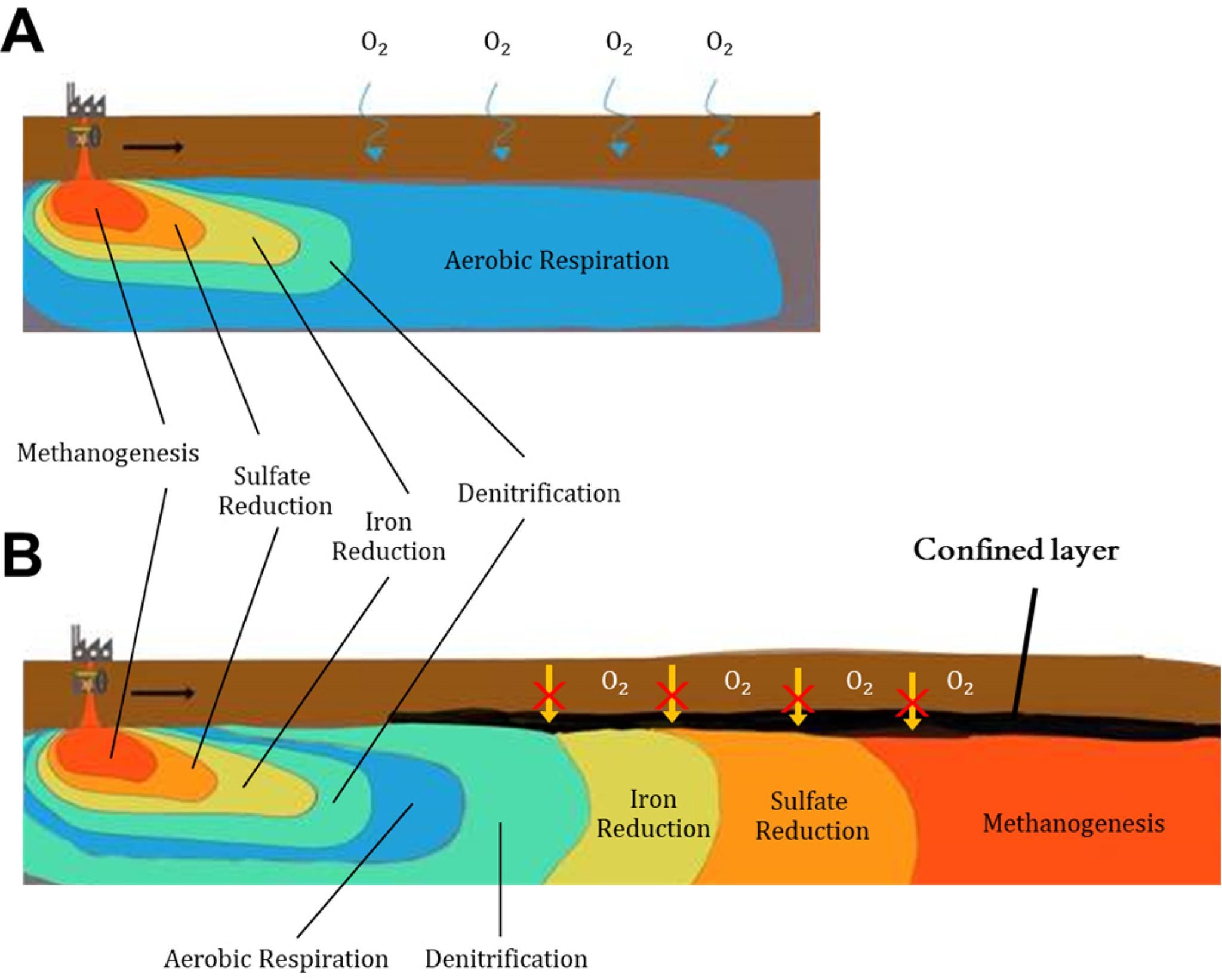
기존 환경이 자유면 대수층인 경우 자유면 층이 대수층 위에 존재하는데 자유면 층은 모래와 자갈 등 공극률이 큰 물질로 이루어져 투수성이
크다. 따라서 대기 중의 산소가 토양을 통해 지하수로 충분히 공급되어 지하수 내 용존산소 농도가 증가할 수 있다(Fig. 5A). 호기성 환경으로
변화하면서 메탄 생성 반응과 철 환원 반응이 비활성화되어 CH4, Fe2+ 농도가 급격하게 감소한다. 다른
성분들은 원래 수준으로 회복될 수도 있고, 그렇지 않을 수도 있는데, 이는 비오염지대 환경의 지하수에 따라 달라질 것이다. 산소가 지속적으로 공급되므로,
그 이후 지역은 모두 호기성 환경이다. 따라서 그 이후 지역에서는 호기성 호흡만 일어나고, 소량의 잔여 오염 물질을 모두 호기성 미생물이 분해한다.
Fig. 5B는 BTEX가 대량 유출된 시점부터 비오염지대 피압대수층까지 모든 시나리오를 나타낸 것이다. 오염 물질이 매우 희석된 시점(aerobic
respiration)을 기준으로 구역이 대칭적으로 나뉜다(Cozzarelli
and Weiss, 2007; Smith and Harris, 2007). 피압 지층이 대수층을 덮는 경우, 투수성이 낮은 점토층으로 인해 외부에서
산소가 대수층으로 유입되지 못한다. 따라서 산소의 농도는 상대적으로 낮고, 다른 화학 성분(NO3-, Fe3+, SO42- 등)들이 넓게 분포하는 환경이
조성된다. 물론 비오염지대 지하수에서도 소량의 산소를 이용한 일시적으로 호기성 호흡이 일어날 수 있지만 소량의 오염물질을 분해하면서, 산소가 빠르게
고갈되어 혐기성 환경이 조성된다. 다시 혐기성 호흡이 일어나고 탈질화 반응, 철 환원 반응, 황산염 환원 반응, 메탄 생성 반응을 거치면서
NO3-, Fe3+, SO42-, CO2가 순서대로 소모된다(Fig. 5B). 이로 인해 또다시 구역이 나뉘는데,
오염 유출 초기의 순서와는 반대이다. 비오염지대 유입 시점을 기준으로 탈질화 반응, 철 환원 반응, 황산염 환원 반응, 메탄 생성 반응의 순서로
TEAPs 구역이 나뉜다.
4.3. 산화환원전위에 의한 TEAPs
평가
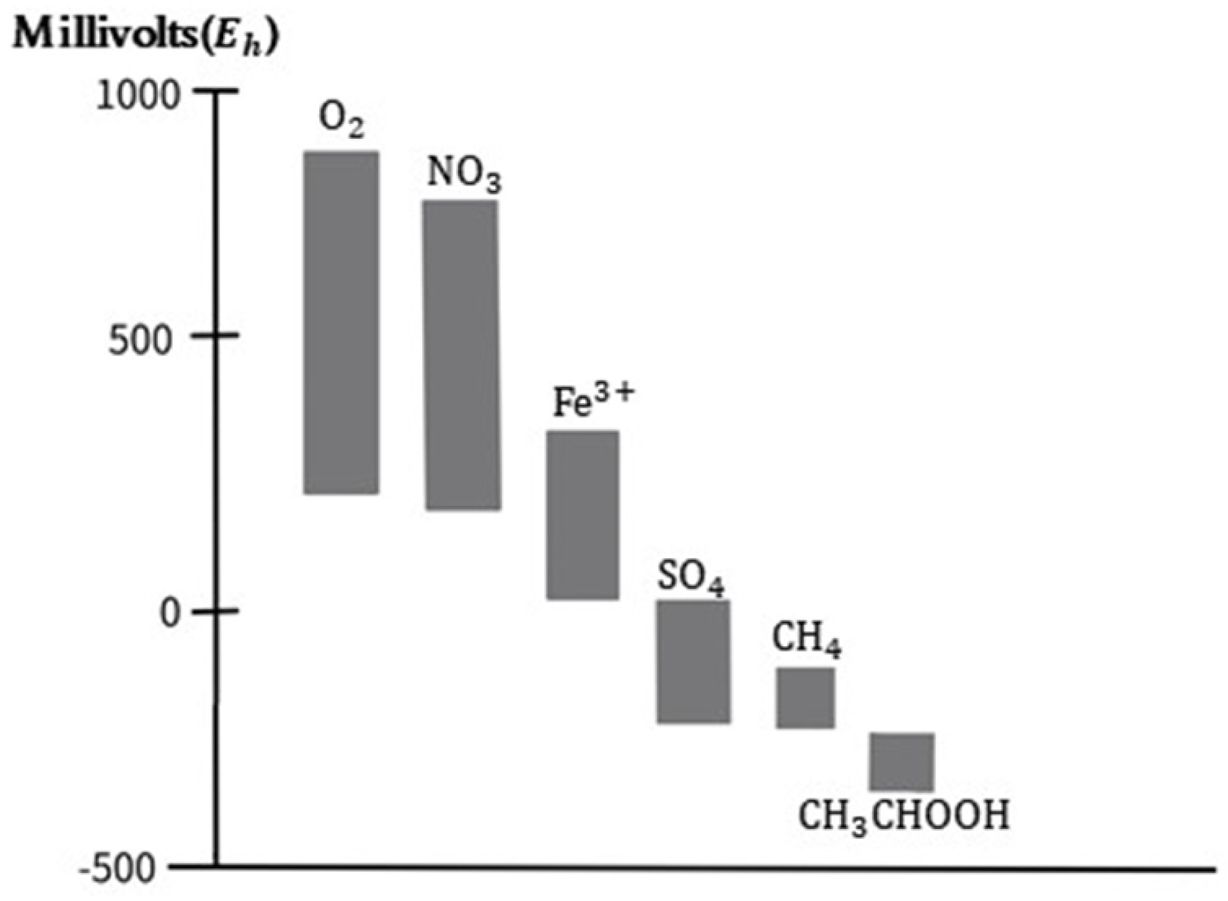
TEAPs를 판단할 때는 최대한 여러 가지 정보를 함께 사용해야 한다. 산화 환원 전위도 그중 하나인데 철 환원 반응과 황산염 환원
반응에서 차이가 두드러져, 구별하는 데 유용하다(Fig. 6). 하지만 호기성 호흡과 탈질화 반응의 경우 Eh 범위가 상당히 겹치기 때문에 주의가
필요하다. 산소와 질산이온에 의한 호흡이 가장 빈번히 일어나는 것을 감안하면, 산화환원전위(Eh)에만 의존하는 방법은 효율적이지 않기 때문에 이
외에 추가 정보와 함께 사용해야 한다(Smith and Harris, 2007).
4.4. 수소 농도에 의한 TEAPs
평가
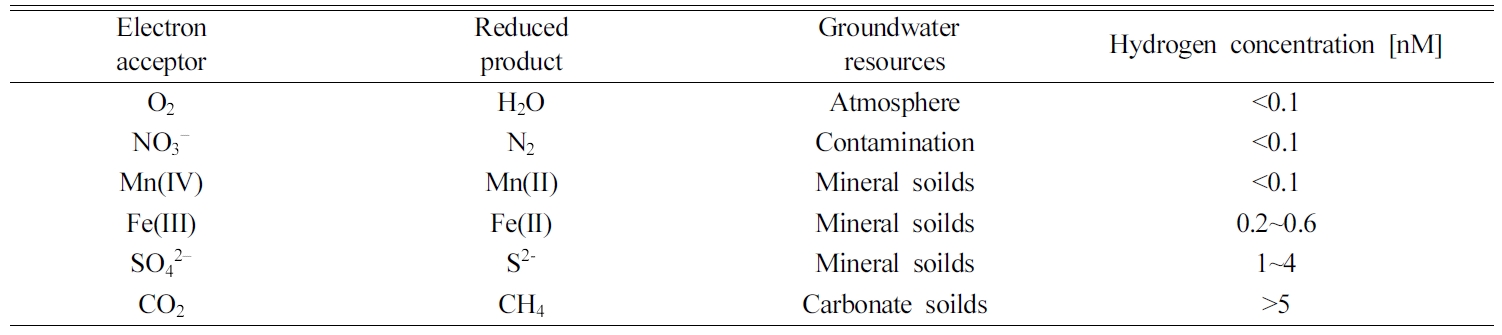
TEAPs를 알아보는 지표에는 용존 산소량, NO3, Fe3+,
SO42- 등 여러 화학 성분의 농도와 Eh 등이 있으며 각각 유용한 데이터를 제공하지만, 각 방법은
모호한 면도 함께 존재한다. 이때 수소 농도를 사용하면 TEAPs를 보다 정확하게 구별할 수 있다(Table 3). 수소 농도는 이론적 또한 실제 오염환경내에서 획득된 경험적 데이터를 통해 알려진 수치로, 수소 농도 범위에 따라 TEAPs를 정확하게 알 수 있다. 특히 황산염
환원 반응과 메탄 생성 반응을 구별하는 데 유용하다고 알려져 있다(Kwon
et al., 2006; Lovley and Goodwin, 1988;
Smith and Harris, 2007).
4.5. TEAPs 경계 지역 평가
대부분의 경우 수소 농도는 TEAPs를 구분할 수 있는 강력한 지표이다. 하지만 TEAPs 경계 또는 중복 지역(overlap)은 수소
농도로만 판단할 수 없다. 경계 부근에서는 특별한 주의가 필요하고, 한가지 지표만 보고 단순하게 확정하지 말아야 한다. 다양한 데이터를 수집하고
참고하여 통합하고 유연하게 생각해야 한다(Alter and Steiof, 2004). 다양한 지표들과 분석법을 Table 4에 정리하였다.
|
Fig. 4 Groundwater contamination with benzene, toluene, ethylbenzene and xylene (BTEX) leaked from underground storage tanks (UST) (A), variation of key chemical components in groundwater with decrease in BTEX concentrations (B), and variation of key chemical components after complete removal of BTEX (C). |
|
Fig. 5 Zoning of terminal electron accepting processes (TEAPs) after release of benzene, toluene, ethylbenzene and xylene (BTEX) in unconfined aquifer (A) and in confined aquifer (B). |
|
Fig. 6 Redox potentials of various biodegradation reactions by terminal electron accepting processes (TEAPs). |
|
Table 3 Dissolved hydrogen concentration in groundwater used as an indicator for predominant TEAPs (Chapelle et al., 1995) |
오염 유출 시, 지중환경 TEAPs는 오염원으로부터 순서대로 메탄 생성 반응, 황산염 환원 반응, 철 환원 반응, 탈질화 반응, 호기성
호흡이 나타난다. 오염이 충분히 희석되어 비오염지대에 진입 시, 자유면 대수층일 경우, 이후 지중환경에서는 호기성 호흡이 일어나고, 피압 대수층일
경우, 배열 순서가 반대를 이루며 TEAPs가 전개된다.
수소 농도를 비롯하여 용존 산소량, NO3-, Fe3+, SO42-, CH4
농도 등 발현되는 여러 가지 특징을 고려하여 해당 지역의 TEAPs을 확인할 수 있다. 그중에서도
용존수소 농도를 이용한 TEAPs 평가가 효과적이며, 특히 황산염 환원 반응과 메탄 생성반응을 구분하는 데 유용하다고 알려져 있다.
Bubble Stripping 방법을 이용한 수소 가스 샘플링 시, Microseeps cell과 저속양수 펌프와 정량펌프가 효율적이었다. 더불어
튜브관과 headspace 크기를 조절하여 stripping 시간을 단축해 샘플링 효율을 높일 수 있다. 수소 가스 샘플을 보관할 경우, 약
4oC의 서늘하고 어두운 곳에서 이틀까지 보관할 수 있었다.
지중환경은 복잡성, 다양성, 불균질성을 포함하고 있으므로 TEAPs 평가 시 어느 한 가지 지표가 아닌 다양한 지표 들을 고려해야 한다.
또한, 경계 지역에서 TEAPs가 중복될 수 있으므로 지중환경내 오염 확산과 지역적 분포특성을 고려하여 분석에 특별히 신중해야 한다. 따라서 대표 화학성분 농도와 수소 농도에
추가하여, 산화환원전위, 유기 탄소 농도 등 최대한 많은 데이터를 종합하여 해석 평가해야 한다.
TEAPs를 부지 특성화의 주요 항목으로 보고, 지중환경 조사를 시행하면 더 정확한 복원 계획을 수립할 수 있을 것이고, 이를 통해
오염 정화 성공률에 기여할 것으로 예상된다. 또한, 지하수 수질 변화로 인한 지하수공 막힘, 부식, 유해 가스 발생 원인을 규명하고 이를 방지하는
데 중요한 단서로 활용될 수 있을 것이다. 따라서 TEAPs에 대한 기초 연구와 분석법 개발을 진행하여 가이드라인을 확립하고, 오염부지를 포함한
국내 지중환경에 대한 TEAPs 데이터 베이스 작성을 위한 기반 마련이 필수적이라고 판단된다.
본 연구는 환경부 재원으로 환경산업기술원의 지중환경오염위해관리기술개발사업의 지원을 받아 연구되었습니다(과제번호:
2018002440002).
- 1. 박용하, 1988, 심층 지하미생물 탐색 현황, 미생물과 산업(The microorganisms and industry), 14(2), 11-12.
- 2. AFCEE (Air Force Center for Engineering and the Environment), NFESC (Naval Facilities Engineering Service Center), ESTCP (Environmental Security Technology Certification Program), 2004, Principles and practices of enhanced anaerobic bioremediation of chlorinated solvents. Prepared by Parson Infrastructure & Technology Group, Inc., Denver, CO, USA. TR-2250-ENV.
- 3. Alter, M.D. and Steiof, M., 2004, Optimized method for dissolved hydrogen sampling in groundwater, Journal of Contaminant Hy-drology, 78(1-2), 71-86.
-

- 4. Azadpour-Keeley, A., 1999, Ground Water Issue: Microbial Processes Affecting Monitored Natural Attenuation of Contaminants in the Subsurface, US Environmental Protection Agency.
- 5. Chapelle, F.H., 2001, Ground-water microbiology and geochemistry. 2nd ed. New York (N.Y.): Wiley.
-

- 6. Chapelle, F.H. and McMahon, P.B., 1991, Geochemistry of dissolved inorganic carbon in a Coastal Plain aquifer, Journal of Hy-drology, 127(1-4), 85-108.
-

- 7. Chapelle, F.H., McMahon, P.B., Dubrovsky, N.M., Fujii, R.F., Oaksford, E.T., and Vroblesky, D.A., 1995, Deucing the distribution of terminal electron-accepting processes in hydroglogically diverse groundwater systems, Water Resources Research, 31(2), 359-371.
- 8. Cozzarelli, I. and Weiss, J., 2007, Biogeochemistry of Aquifer Systems, p 843-859. In Hurst C, Crawford R, Garland J, Lipson D, Mills A, Stetzenbach L (ed), Manual of Environmental Microbiology, Third Edition. ASM Press, Washington, DC.
- 9. EPA, 2017, How To Evaluate Alternative Cleanup Technologies For Underground Storage Tank Sites, EPA 510-B-17-003.
- 10. Finneran, K.T., 2019, Using Information to Your Advantage: Data Analyses and Interpretation to Design Engineered and Passive Remediation Strategies, 12th Asian Regional Conference of IAEG, Jeju, Republic of Korea.
- 11. Flynn, T.M., Sanford, R.A., and Bethke, C.M., 2008, Attached and suspended microbial communities in a pristine confined aquifer, Water Resources Research, 44(7).
-

- 12. Geological Survey of Denmark and Greenland, 2019, Groundwater Maps and Data. https://eng.geus.dk/products-services-facilities/data-and-maps/groundwater-maps-and-data/
- 13. Hwang, Y.H., Shim, M., Oh, D.H., Yang, J., and Kwon, M.J., 2014, Effects of Extracellular Electron Shuttles on Microbial Iron Reduction and Heavy Metals Release from Contaminated Soils, Journal of Soil and Groundwater Environment, 19(2), 16-24.
-

- 14. Heimann, A., Marczinek, S., Kloos, K., and Peiffer, S., 2003, Optimization of the Sampling Technique for the Determination of Dis-solved Hydrogen in Groundwater, Acta Hydrochimica Et Hydrobiological, 31(6), 491-500.
-

- 15. Kwon, M.J., O¡¯Loughlin, E.J., Antonopoulos, D., and Finneran, K.T., 2011, Geochemical and Microbiological processes contrib-uting to the transformation of Hexahydro-1,3,5-trinitro -1,3,5-triazine (RDX) in Aquifer Sediment, Chemosphere, 84(9), 1223-1230.
-

- 16. Kwon, M.J., O¡¯Loughlin, E., Ham, B., Hwang, Y.H., Shim, M., and Lee, S., 2018, Application of an in-situ soil sampler for as-sessing subsurface biogeochemical dynamics in a diesel-contaminated coastal site during soil flushing operations, Journal of Envi-ronmental Management, 206, 938-948.
-

- 17. Kwon, M.J., Sanford, R.A., Park, J., Kirk, M.F., and Bethke, C.M., 2008. Microbiological Response to Well Pumping, Ground Wa-ter, 46(2), 286-294.
-

- 18. Kwon, M.J., Yang, J., Shim, M., Lee, S., Boyanov, M., Kemner, K., and O¡¯Loughlin, E., 2014, Biotic and abiotic reduction of goe-thite (a-FeOOH) by subsurface microorganisms in the presence of electron donor and sulfate, Journal of Soil and Groundwater En-vironment, 19(1), 54-62.
-

- 19. Lovley, D.R., Chapelle, F.H., and Woodward, J.C., 1994, Use of dissolved H2 concentrations to determine distribution of microbially catalyzed reactions in anoxic groundwater, Environmental Science and Technology, 28(7), 1205-1210.
-

- 20. Lovley, D.R. and Goodwin, S., 1988, Hydrogen concentrations as an indicator of the predominant terminal electron-accepting reac-tions in aquatic sediments, Geochimica et Cosmochimica Acta, 52(12), 2993-3003.
-

- 21. Mclnnes, D.M. and Kampbell, D., 2000, Bubble Stripping Method for Determining Dissolved Hydrogen(H2) in Well Water, Field Analytical Chemistry and Technology, 4(6), 283-296.
-

- 22. Raynaud, X. and Nunan, N., 2014, Spatial ecology of bacteria at the microscale in soil, PLoS ONE, 9(1), e87217.
-

- 23. Smith, R. and Harris, Jr. S., 2007, Determining the Terminal Electron-Accepting Reaction in the Saturated Subsurface, p 860-871. In Hurst C, Crawford R, Garland J, Lipson D, Mills A, Stetzenbach L (ed), Manual of Environmental Microbiology, Third Edition. ASM Press, Washington, p 860-871.
- 24. Stookey, L.L., 1970, Ferrozine - a new spectrophotometric reagent for iron, Analytical Chemistry, 42(7), 779-781.
-

- 25. Torsvik, V. and ¨ªvreås, L., 2002, Microbial diversity and function in soil: From genes to ecosystems, Curr. Opin. Microbiol., 5(3), 240-245.
-

- 26. Van Der Heijden, M.G., Bardgett, R.D., and Van Straalen, N.M., 2008, The unseen majority: soil microbes as drivers of plant diver-sity and productivity in terrestrial ecosystems, Ecology letters, 11(3), 296-310.
-

 This Article
This Article
-
2020; 25(S1): 1-15
Published on Jun 30, 2020
- 10.7857/JSGE.2020.25.s1.001
- Received on Apr 11, 2020
- Revised on May 7, 2020
- Accepted on May 21, 2020
 Services
Services
- Abstract
1.지중환경 내teaps의 중요성과 활용성
2. teaps분석 지표 및 샘플링 기법
3.teaps분석 방법
4. teaps평가방법
5.결 론
- 사사
- References
- Full Text PDF
Shared
 Correspondence to
Correspondence to
- Man Jae Kwon
-
Department of Earth and Environment Sciences, Korea University, Seoul 02841, Korea
- E-mail: manjaekwon@korea.ac.kr







