- Removal of PCBs in Aqueous Phase in Ultraviolet (UV), Ultrasonic (US), and UV/US Processes
Dukyoung Lee1,2·Younggyu Son1,2*
1Department of Environmental Engineering, Kumoh National Institute of Technology
2Department of Energy Engineering Convergence, Kumoh National Institute of Technology- 자외선 및 초음파 공정에 의한 수용액 상의 PCBs 분해
이덕영1,2·손영규1,2*
1금오공과대학교 환경공학과
2금오공과대학교 에너지공학융합전공This article is an open access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/4.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
The removal of PCBs (Polychlorinated biphenyls) in aqueous phase was investigated in the ultraviolet (UV) process, ultrasonics (US) process and ultraviolet/ultrasonic (UV/US) process using PCB No.7 and Aroclor 1260. For PCB No.7 relatively high removal efficiency over 90% was obtained during 20 min in the UV process and UV/US process. On the other hand, lower removal efficiency of 50 – 70% was achieved for it consisted of individual congeners of PCBs containing 3~8 of chlorine atom. It was found that the dechlorination reaction (the photolytic cleavage of C-Cl bond) was considered as a main removal mechanism in the UV process while PCBs were removed by cavitation-induced radical reaction in the US process. No significant dechlorination occurred in the US process. Consequently, it was suggested that the UV process or UV/US process was applicable for the removal of PCBs in aqueous phase in terms of the removal efficiency and operation time. In addition, the application of saturating gas such as Ar and Air could be considered to control redox condition and enhance the severity of acoustic cavitation for the removal of PCBs
Keywords: PCBs (Polychlorinated biphenyls), Ultraviolet, Ultrasound, Dechlorination, Cavitation
최근 환경부에서 발간된 “잔류성유기오염물질 환경 모니터링 백서”에 따르면 2008년부터 스톡홀름협약의 이행을 위한 POPs(Persistent Organic Pollutants) 모니터링 목적의 대기, 수질, 토양, 퇴적물 등의 측정망을 설치·운영하였는데, 국내 잔류성유기오염물질의 농도가 정도의 차이는 있으나 지속적으로 감소한 것으로 나타났다(MOE, 2021). 그러나 반환 미군기지 부지에서의 다이옥신(Dioxins) 오염토양 확인, 일부 농경지에서의 살충제 DDT(Dichloro-Diphenyl-Trichloroethane) 오염 확인, PCBs (Polychlorinated Biphenyls) 포함 폐변압기의 관리 부실 등이 지속적으로 보고되고 있어 지속적인 모니터링과 처리방안 마련이 필요한 실정이다(MOE, 2021).
PCBs는 두 개의 벤젠고리에 염소가 결합되어 있는 화합물로 사용금지 이전에는 난연제 및 변압기, 콘덴서 등의 절연유로 폭넓게 사용되었다(Tang et al., 2018). 벤젠고리에 있는 총 10개의 자리에 염소가 1개에서 10개까지 다양하게 포함할 수 있어 총 209개의 이성체(Congeners)가 존재한다. 네 개 이상의 염소를 포함하는 PCBs 중 두 개의 ortho 자리에 염소가 모두 없거나 하나만 없는 12종의 PCBs가 다이옥신과 같은 독성이 있어 이를 dioxin-like PCBs(DL-PCBs)로 명하고 이를 특별 관리하고 있다(IARC, 2016; MOE, 2021). 염소를 여러 개 포함하는 일반 PCBs가 분해반응에 의해 탈염소 반응이 일어날 경우 DL-PCBs가 생성되기도 한다(Chang et al., 2003).
PCBs를 효율적으로 분해하기 위해 0가 철 반응, 광분해, 소각, 생물학적 분해, 초음파 캐비테이션 기술 등의 다양한 방법이 제안되었는데, 유기 용매 등의 액상 내 PCBs 처리를 위해서는 자외선 광분해 기술이 일반적으로 연구되었다(Zhang and Hua, 2000; Tang et al., 2018). UVC 등의 자외선을 액상에 조사할 경우 PCBs의 벤젠고리와 결합한 염소가 분리되는 탈염소(Dechlorination) 반응이 일어나게 되는데, 이때 전자효과(electronic effect) 및 입체효과(steric effect) 등의 이유로 ortho, meta, para 자리 순으로 탈염소 반응 및 분해 반응이 일어나는 것으로 보고되고 있다(Miao et al., 1999; Chang et al., 2003; Tang et al., 2018). 또한, 전자친화도의 증가로 인해 염소가 많은 PCB의 분해 시간이 상대적으로 더 많이 소요된다는 것도 보고되었다(Miao et al., 1999; Chang et al., 2003).
PCBs는 상대적으로 낮은 용해도로 인하여 수계에서 발견될 가능성이 매우 낮아 기존 연구도 거의 대부분 유기용매 상에서의 PCBs 처리기술 개발에 집중하였다. 그러나 국내 모니터링 결과를 통해 향후 수질환경분야에서의 PCBs 모니터링이 지속적으로 필요함을 강조하였고(MOE, 2021), 이와 함께 수용액 상에서의 PCBs 분해기술 개발 및 분해 기작 규명 등의 연구가 필요할 것으로 예상되었다. 그러므로 본 연구에서는 액상에 존재하는 PCBs의 처리기술 개발을 위하여 단일 물질인 PCB No.7과 복합 물질인 Aroclor 1260의 분해 수준을 다양한 조건에서 확인하였다. UVC를 이용한 자외선 공정 및 20 kHz 초음파 공정을 공기 및 아르곤 포화 조건에서 단독 및 혼합 공정으로 적용하여, 분해 수준 및 탈염소 수준을 정량적으로 비교분석 하였다. 또한, 기존 연구결과 등을 활용하여 자외선 공정 및 초음파 공정의 PCBs 분해 기작을 규명하고자 하였다.
2.1. PCB 수용액 제조
대상 PCB는 염소를 2개 포함하는 PCB No.7(2,4-Dichlorbiphenyl, C12H8Cl2)와 4-8개의 염소를 포함하는 다양한 종류의 PCB를 포함하는 혼합물인 Aroclor 1260(1,000 mg/L: C12H6Cl4 1%, C12H5Cl5 12%, C12H4Cl6 38%, C12H3Cl7 41%, C12H2Cl8 8%)을 이용하였다. 두 화학약품 모두 Dr. Ehrenstorfer 제품을 이용하였다. 실험을 위한 PCB 수용액은 PCB No.7의 경우 우선 250 mg/L의 메탄올 용매의 용액을 제조한 후 이를 물과 1:300의 비율로 혼합하여 준비하였다. Aroclor 1260의 경우 메탄올 용매의 300 mg/L 용액을 제조 후 이를 물과 1:300의 비율로 혼합하여 실험에 이용하였다. PCB No.7 및 Aroclor 1260의 수용액 상 초기농도는 각각 0.83 및 1.0 mg/L였다.
2.2. PCB 분해 실험
자외선 및 초음파에 의한 PCB 분해 실험을 수행하기 위해 냉각시스템이 연결된 500 mL 부피의 원형 이중 Pyrex 반응기를 이용하였다. 제조된 PCB 수용액 300 mL를 대상으로 자외선 단독 공정, 초음파 단독 공정, 자외선/초음파 혼합 공정을 적용하였다. 자외선 공정의 경우 235 nm 파장의 UVC 램프(TUV 6W, Philips) 1개를 반응기 내부에 최대한 잠기도록 위치시켜 실험을 진행하였고, 초음파 공정의 경우 20 kHz probe 형태의 초음파 장비(VCX 750, Sonics & Materials)를 100W로 유지하여 tip 끝이 반응기 바닥면에서 1 cm 떨어지게 위치시켜 실험을 진행하였다. 자외선/초음파 혼합 공정은 자외선 램프와 초음파 probe를 동시에 반응기에 설치하여 실험을 진행하였다. PCB 분해 실험은 1시간 동안 진행하였으며, 온도는 20±2oC로 유지하였다. 산화 조건 및 환원 조건의 조성을 위해 수용액은 공기 혹은 아르곤 가스로 실험 전 포화시켜 적용하였다.
2.3. PCB 농도 측정
단독 및 혼합 공정에서 시간에 따른 PCB 분해 수준을 분석하기 위해 0, 1, 3, 5, 10, 20분 간격으로 PCB 수용액을 1 mL 샘플링하였다. 샘플링된 시료는 80oC 조건에서 질소농축기(MG-2200, Eyela)를 이용하여 물을 모두 휘발시킨 후 헥산으로 용해시켠 1 mL 부피를 만들어 ECD(Electron Capture Detector)가 장착된 GC(NL/450 GC, Varian)로 분석하였다. 추가적으로 PCB의 탈염기 반응에 의해 발생되는 염소 이온을 측정하기 위하여 시간대별로 시료 5 mL를 샘플링한 후 IC(ICS-2100, Dionex)를 이용하여 분석하였다. PCB congeners는 IUPAC No. 18, 28, 31, 44, 52, 101, 118, 138, 149, 153, 170, 180, 194인 피크를 피크패턴법을 이용하여 정량하였다.
2.4. SCL 이미지 분석
초음파 캐비테이션 현상에 의한 반응기 내부의 활성화 영역을 확인하기 위하여 암실 조건에서 루미놀 용액(luminol 0.1 g/L, NaOH 1.0 g/L)과 노출 기능이 있는 디지털카메라(DSC-RX100M7, Sony)를 이용하여 초음파화학발광(SCL, sonochemiluminescence) 이미지를 촬영하여 분석하였다. 카메라의 노출시간은 20초 였으며, 메탄올의 농도 비율(0 - 2.0%)을 변화시켜 촬영하였다.
3.1. PCB 분해
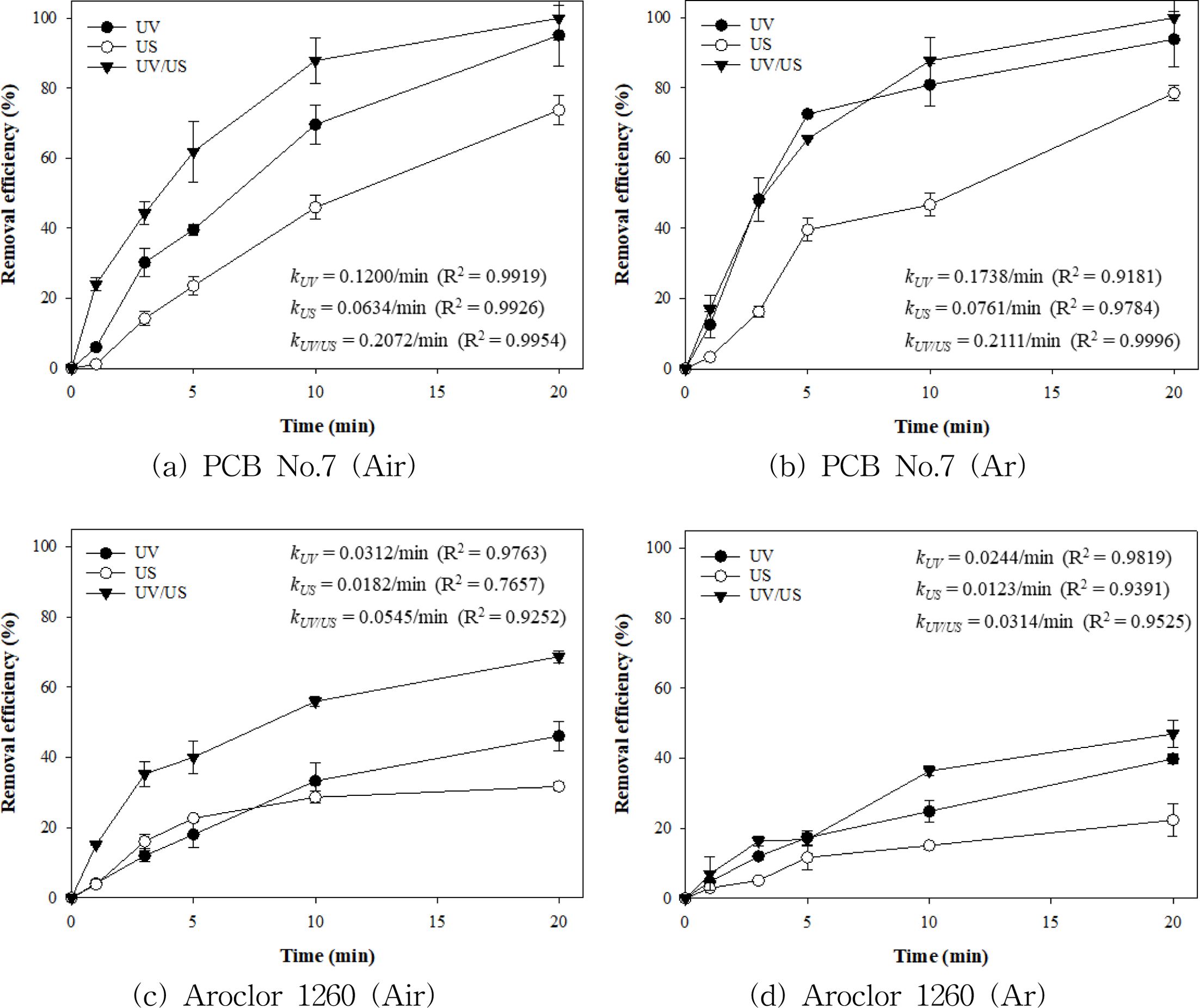
자외선 및 초음파 기술에 의한 수용액상에서의 PCB 분해 수준을 확인하기 위하여 PCB 단일 물질(PCB No.7) 및 혼합 물질(Aroclor 1260)을 대상으로 자외선 단독 공정, 초음파 단독 공정, 자외선/초음파 혼합 공정을 적용하였다. 산화 혹은 환원 조건에서의 분해 경향을 확인하기 위하여 공기 및 아르곤 가스 조건을 적용하였다. Fig. 1에 나타낸 바와 같이 단일 PCB 조건인 PCB No.7(염소 2개 포함)의 경우 자외선 혹은 자외선/초음파 공정을 적용하는 경우 20분 이내에 약 90% 이상의 분해효율을 얻을 수 있었다. 초음파 공정의 경우 다소 낮은 약 70% 수준의 분해효율이 확인되었는데, 이는 자외선 공정에 의한 PCB 분해와 초음파 공정에 의한 PCB 분해의 기작이 다르기 때문인 것으로 판단되었다. PCB 혼합물질인 Aroclor 1260(염소 3-8개 포함)의 경우 상대적으로 낮은 처리효율을 나타내었는데, 공기 조건에서 자외선/초음파 혼합 공정을 적용하는 경우 약 70% 수준의 처리효율을, 아르곤 조건에서 혼합 공정 적용 시 약 50% 수준의 처리효율이 측정되었다.
자외선 공정에서 PCB가 분해되는 기작은 주로 광반응에 의한 탈염소(Dechlorination) 반응으로, 기존 연구에 따르면 ortho 자리에 있는 염소가 가장 쉽게 떨어지며, 이후 meta, para 자리 순으로 염소가 떨어질 수 있는 것으로 알려져 있다(Miao et al., 1999; Chang et al., 2003; Tang et al., 2018). 또한, PCB 내 염소의 개수가 많을수록 1차 분해 반응에 대한 반감기가 크게 증가하는 것으로 보고되기도 하였다. 본 연구에서 적용한 PCB No.7은 염소를 2개 포함하는 PCB로 한 개의 염소가 ortho 자리에 다른 한 개의 염소가 para 자리에 있어 탈염기 반응에 의한 PCB 분해 반응이 원활하게 일어날 수 있는 PCB로 판단된다. Tang et al.(2018)은 자외선에 의해 PCB No.7이 빠르게 분해되고, 그에 대한 분해산물로 PCB No.3(para 자리에 염소 1개 포함)가 일부 생성되는 것을 보고하기도 하였다. 그러나 Aroclor 1260에 포함된 PCB는 염소를 4개에서 8개까지 포함하는 PCB로 상대적으로 덜 활발한 탈염소 반응이 일어날 것으로 고려되었다. 이는 탈염기 반응이 일어난다 하더라도 염소를 적게 포함하는 새로운 PCB가 반응 부산물로 생성될 가능성이 PCB No.7과 같이 염소를 적게 포함하는 PCB 보다 상대적으로 높기 때문이다(Chang et al., 2003; Tang et al., 2018). 결과적으로 Fig. 1의 결과와 같이 Aroclor 1260을 대상으로 한 분해실험에서 자외선에 의한 상대적으로 낮은 광분해 반응 정도가 확인되었다. 자외선 단독 공정에서 PCB No. 7의 경우 90% 수준의 처리효율이었으나, Aroclor 1260의 경우 40% 수준으로 절반 수준에 미치지 못하는 낮은 처리효율을 얻을 수 있었다. Fig. 2에 공기 조건에서의 GC-ECD에서의 PCB 종류별 시간에 따른 저감 수준을 나타내었다. 자외선 단독 공정에서 PCB No. 7의 경우 90% 수준의 처리효율이었으나, Aroclor 1260의 경우 40% 수준으로 절반 수준에 미치지 못하는 낮은 처리효율을 얻을 수 있었다. Fig. 2에 공기 조건에서의 GC-ECD에서의 PCB 종류별 시간에 따른 저감 수준을 나타내었다.
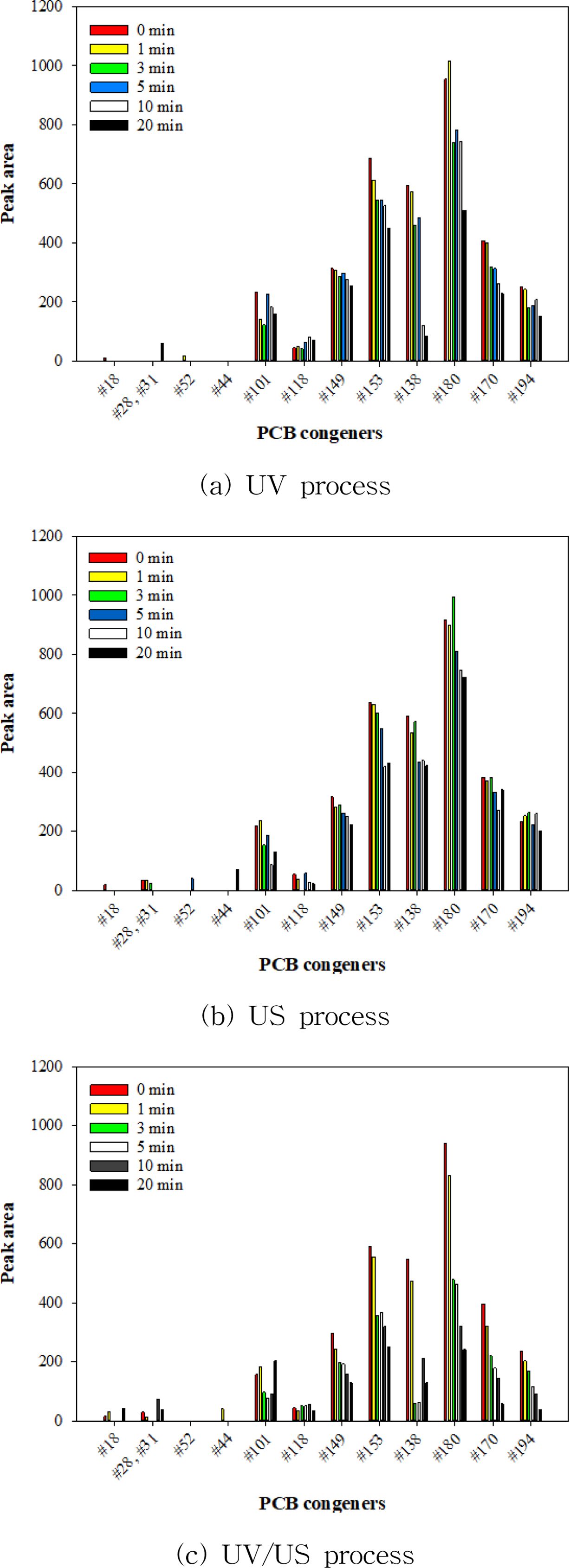
Fig. 2는 x축의 PCB congeners 순서대로 #18, #28, #31은 염소 3개를, #52, #44은 염소 4개를, #101, #118은 염소 5개를, #149, #153은 염소 6개를, #180, #170은 염소 7개를, #194는 염소 8개를 포함하는 PCB의 농도를 의미한다. 결과를 살펴보면, 염소를 상대적으로 적게 포함하는 PCB의 농도가 염소를 많이 포함하는 PCB의 분해반응 진행으로 인해 초기 농도보다 증가하는 것이 일부 확인되었다. 또한, 일부 PCB의 분해되는 정도 혹은 분해 속도가 상대적으로 염소를 더 많이 포함하는 PCB 보다 적거나 느린 것으로 나타났다.
각각의 단독 공정 및 혼합 공정을 반응속도론(Reaction kinetics)으로 분석한 결과 대부분의 경우에 높은 R2 값을 갖는 1차 분해 반응으로 확인되었다. 이는 오염물질의 시간에 따른 분해가 오염물질 자체의 농도에만 영향을 받는다는 의미이며, 오염 반응을 일으키는 빛 에너지 및 초음파 반응에 의한 생성 라디칼 등의 수준 및 농도가 반응 시간 동안 일정하게 유지되었기 때문이다. 구해진 1차 반응상수에 의한 반감기는 단독 및 혼합공정에서 PCB No.7의 경우 3분에서 11분 수준 정도였으며, Aroclor 1260의 경우 13분에서 56분 수준으로 확인되었다. 기존 연구에서 염소가 2개 이하인 PCB의 분해 반감기는 수 분에서 20분 수준이었으나, 3개 이상의 염소를 갖는 PCB에서는 반감기가 수십 분에서 900분 이상까지 확인되기도 하였다(Chang et al., 2003).
초음파에 의한 오염물질 분해 기작은 캐비테이션 현상을 기반으로 이루어지는데, 일반적으로 캐비테이션 버블 내부로 오염물질이 물질이동 되어 극한 조건에서 열분해(Pyrolysis)되는 기작과 캐비테이션 버블 내부에서 생성된 라디칼이 버블 폭발 시 외부로 전달되어 발생하는 라디칼에 의한 분해 기작으로 구분할 수 있다. 본 연구에서 초음파 단독 공정에 의한 분해가 자외선 단독 및 혼합 공정보다 상대적으로 낮은 처리효율을 나타내었는데, 이는 PCB 자체의 특성 때문일 것으로 판단되었다. 적용한 PCB의 낮은 휘발성으로 인해 캐비테이션 버블 내부로의 유입이 거의 일어나지 않았을 것이다. 또한, 캐비테이션 버블에서 생성되는 라디칼에 의한 분해 반응 역시 라디칼의 매우 짧은 존재 시간으로 인해 효율적으로 일어난다고 보기 어렵다. 이는 염소를 많이 포함하고 있지 않아 상대적으로 휘발성이 높은 PCB No.7가 염소를 많이 포함하는 Aroclor 1260 보다 더 높은 분해효율을 나타내는 이유가 될 것이다. 오염물질의 휘발성이 높다면 캐비테이션 버블 쪽에 보다 가까이 존재할 수 있어 라디칼에 의한 영향을 보다 크게 받을 수 있기 때문이다. 평균적으로 염소 2개를 포함하는 PCB의 증기압은 0.24 Pa 수준이며, 염소를 더 포함할수록 증기압이 낮아져 염소 4개 포함 PCB의 증기압은 0.012 Pa, 6개 포함 PCB의 증기압은 5.8×10-4 Pa 수준이 된다. 기존 연구에서 휘발성의 차이가 있는 chlorobenzene과 4-chlorophenol이 수용액 상에 같이 존재할 경우 초음파 분해를 일으키게 되면, 휘발성이 상대적으로 높은 chlorobenzene이 모두 분해된 후에 4-chlorophenol이 분해되기 시작하는 것을 보고하기도 하였다(Pétrier et al., 2007).
수용액 상에서의 초음파 캐비테이션 현상에 의한 PCB 분해를 연구한 Zhang and Hua(2000) 연구를 살펴보면, PCB No.1 와 PCB No.3 각각의 분해에 따라 phenyl 라디칼이 생성되었는데 이는 biphenyl의 C-C 결합이 열적(thermolytic)으로 분열(cleavage)되었기 때문인 것으로 보고하였다. 이러한 열적 반응은 캐비테이션 버블 내부 혹은 액상과 기상(캐비테이션 버블)의 계면에서 일어날 수 있으며, 액상에서는 일어날 수 없는 것으로 확인하였다. 이는 PCB No.1 및 PCB No.3가 모두 염소를 1개만 갖고 있어 휘발성이 상대적으로 높기 때문에 가능한 것으로 판단되었다. 염소를 3개 포함하는 PCB No.29에 대한 실험에서는 phenyl 라디칼이 확인되지 않았는데, 이는 상대적으로 휘발성이 낮은 PCB가 캐비테이션 현상에 노출되었기 때문일 것이다. 결과적으로 앞서 언급한 바와 같이 염소 개수가 적은 PCB는 캐비테이션 버블 내부 혹은 계면에 존재할 수 있어 열적 반응에 의한 분해가 일어날 가능성이 높으며, 상대적으로 염소 개수가 많은 PCB는 생성 라디칼에 의한 분해가 일어날 것으로 예상되었다.
자외선 및 초음파 혼합 공정은 기존의 다양한 오염물질 분해에 대한 연구에서 높은 시너지 효과를 얻을 수 있는 공정으로 보고되고 있다(Xu et al., 2013; Ghafoori et al., 2015; Rao et al., 2016; Matafonova and Batoev, 2019). 시너지 효과의 원인으로는 초음파 캐비테이션 현상에 의한 라디칼 반응의 부산물로 수용액상에 축적되는 과산화수소가 자외선에 의해 활성화되어 다시 라디칼 반응을 일으키기 때문인 것으로 보고되고 있다(Xu et al., 2013). 본 연구에서도 초음파 공정에서 일정 수준의 과산화수소가 생성 및 축적되는 것을 확인하였고, 이를 통해 자외선 공정과 초음파 공정을 혼합하여 적용할 경우 각각의 단독 공정보다 높은 처리효율을 얻을 수 있는 것으로 확인되었다. 그러나 이러한 증진이 시너지 효과 수준까지 미치지 못하는 것으로 확인되었다. 식 (1) 및 본 연구에서 얻어진 각 조건의 1차 분해반응 상수를 이용하여 시너지 수준을 계산해보면, 공기 조건에서 PCB No.7 및 Aroclor 1260은 각각 1.13 및 1.10이, 아르곤 조건에서는 각각 0.84 및 0.86이 산정되었다.

여기서 kUV+US는 혼합공정에서의 1차 분해반응 상수, kUV 및 kUS는 자외선 및 초음파 단독 공정에서의 1차 분해반응 상수를 의미한다(Xu et al., 2013). 결과적으로 본 연구에서의 혼합 공정 적용은 특정 처리효율을 달성하기 위한 전체 공정 시간을 단축한다는 측면에서 의미가 있는 것으로 판단되었다.
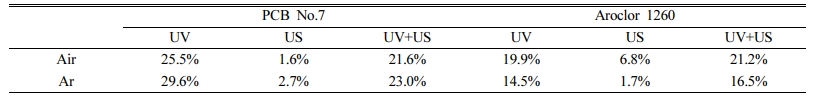
산화 조건 및 환원 조건 조성을 위한 공기 및 아르곤의 주입에 대한 결과를 살펴보면, PCB No.7의 경우 환원 조건인 아르곤 포화 조건에서 상대적으로 높은 분해 수준이 확인되었다. 그러나 Aroclor 1260의 경우에는 공기로 포화된 조건에서 더 높은 수준의 분해가 확인되었다. Table 1은 PCB No.7 및 Aroclor 1260이 최초 포함하고 있는 염소 대비 탈염소 반응 후 액상에 존재하는 염소이온의 비율을 나타내었다. 탈염소 수준을 살펴보면 PCB No.7의 경우 공기 조건보다 아르곤 조건에서 보다 높은 탈염소 반응이 일어났으나, Aroclor 1260의 경우 공기 조건에서 보다 높은 탈염소 반응이 일어났다. 결과적으로 염소를 적게 포함하는 PCB No.7의 경우 환원 조건을 조성하는 것이 분해 및 탈염소 반응에 유리하며, Aroclor 1260의 경우 산화 조건을 조성하는 것이 유리한 것으로 확인되었다. 이는 Aroclor 1260이 다양한 종류의 PCB를 포함하고 있어 다양한 산화/환원 반응에 의해 PCB가 분해되고, 탈염소 반응이 일어나기 때문인 것으로 판단되었다. 이에 대한 정확한 이해를 위해 추가 연구가 필요할 것으로 판단되었다. 추가적으로 아르곤은 초음파 캐비테이션 반응에서 캐비테이션 버블 내부의 높은 온도 및 압력 조건을 보다 극한 조건으로 만들 수 있는 기체로 알려져 있어 캐비테이션 현상 자체 및 열분해 등의 반응에 유리한 것으로 보고되고 있다(Beckett and Hua, 2001; Choi et al., 2021). 그러나 라디칼 반응에는 적합하지 않은 것으로 보고되고 있어, 이는 아르곤 조건에서 상대적으로 휘발성이 높은 PCB No.7의 분해가 초음파 반응에 의해 증진되고, 휘발성이 낮은 Aroclor 1260의 분해는 저감되는 것에 대한 설명이 될 수 있을 것이다.
초음파 공정에서 탈염소 반응이 거의 일어나지 않는 것으로 확인되었으며, 자외선 및 초음파 혼합 공정에서의 탈염소 수준이 자외선 단독 공정과 비슷하거나 오히려 낮은 수준으로 나타났다. 이는 초음파에 의한 PCB 분해 공정이 자외선 공정과는 다르게 탈염소 반응이 주를 이루는 것이 아님을 의미한다. Zhang and Hua(2000)은 염소를 3개 포함하는 2,4,5-PCB를 초음파 공정에 적용한 결과 염소 3개를 모두 포함하고 있는 trichlorophenol이 생성되는 것을 보고하기도 하였다.
본 연구에서의 대상 수용액에는 PCB 용해를 위한 메탄올이 포함되어 있는데, 이 메탄올로 인한 분해 반응의 저해 혹은 증진이 일어났을 것으로 예상되었다. 일반적으로 메탄올은 OH 라디칼과 같은 산화 라디칼에 대한 scavenger 역할을 하는 것으로 알려져 있어, 메탄올의 존재로 인한 오염물질의 분해가 저해됨은 여러 연구자에 의해 보고되었다(Nasseri et al., 2017; Li et al., 2013). 특히 본 연구에서의 초음파 반응의 경우 라디칼 반응을 주요 분해 반응으로 고려하고 있기 때문에 메탄올의 존재는 전체 반응 정도를 크게 저해했을 것이다. 이를 확인하기 위해 초음파 캐비테이션 현상에 의한 라디칼 산화 반응을 시각적으로 확인할 수 있는 루미놀 시험을 Fig. 3과 같이 수행하였다. 순수한 루미놀 수용액 대비 메탄올의 존재 비율이 0.1%에서 2%까지 증가함에 따라 캐비테이션 반응의 정도 및 범위가 다소 감소하는 것을 확인할 수 있었으며, 이를 통해 메탄올로 인한 초음파 공정의 효율 저해가 PCB 분해 시에도 의미 있는 수준으로 있었을 것으로 판단하였다. 본 연구에서의 메탄올 존재 비율은 약 0.3% 수준이었다.
자외선 반응의 경우 메탄올의 존재로 인하여 오염물질의 분해가 증진된 경우도 보고되었는데, 더 이상의 산화가 진행될 수 없는 사염화탄소(CCl4)를 대상으로 자외선 및 과산화수소 공정을 적용한 결과, 사염화탄소의 분해가 일어나지 않았다. 그러나 메탄올을 0.01%에서 0.5%까지 메탄올 농도를 증가시킴에 따라서 분해 정도가 크게 증진되는 것이 확인되었다. 이는 자외선/과산화수소 공정에서 발생한 OH 라디칼과 메탄올이 반응하여 hydroxymethyl 라디칼(∙CH2OH)이 생성되고, 이후 사염화탄소의 C-Cl 결합을 끊는 환원 반응을 유도하여 오염물질의 분해를 일으킨다(Gonzalez et al., 2007). 본 연구에서는 자외선 반응에 과산화수소를 주입하지는 않았으나, 초음파 반응과의 혼합 공정 시 초음파 캐비테이션 반응에 의해 생성되는 OH 라디칼 및 과산화수소 등에 의해 위와 같은 분해 증진 효과가 일어나 염소를 상대적으로 많이 포함하여 산화정도가 높은 PCB의 분해를 증진시키는 효과가 있을 것으로 예상되었다.
|
Fig. 1 Removal efficiency of PCB No. 7 and Aroclor 1260 in UV, US, and UV/US processes under air or Ar condition. |
|
Fig. 2 Variation of each congener’s peak area of Aroclor 1260 in the UV, US, and UV/US process under the air condition. |

|
Fig. 3 SCL (Sonochemiluminescence) images obtained under various methanol concentrations |
|
Table 1 Dechlorination ratio of PCB No. 7 and Aroclor 1260 in the UV, US, and UV/US process under air or Ar condition |
본 연구에서는 수용액 상의 PCBs 분해기술 개발을 목적으로 자외선에 의한 광분해 공정과 초음파에 의한 캐비테이션 공정을 평가하였다. 단독 물질인 PCB No.7의 경우 20분 수준의 처리시간 내 자외선 단독 공정 및 자외선/초음파 혼합 공정에서 90% 수준의 처리효율을 얻을 수 있었다. 그러나 여러 종류의 PCB를 포함하고 있는 Aroclor 1260의 경우 많은 염소를 포함하는 특성 등으로 인하여 혼합 공정에서의 처리효율이 50-70% 수준으로 나타나 추가적인 분해 기술 적용 혹은 더 긴 처리시간이 요구되었다. 자외선 공정의 분해 기작은 기존 유기용매 상에서의 연구에서와 같이 빛에너지에 의한 C-Cl 결합을 끊는 탈염소 반응이었다. 그러나 초음파 공정의 경우 캐비테이션 현상에 의한 라디칼 반응 및 그로 인한 연쇄반응이 주요 분해 기작으로 고려되었으며, 이로 인해 매우 낮은 수준의 탈염소 반응이 확인되었다. 결과적으로 수용액 상에 존재하는 PCBs를 처리하기 위한 방안으로 자외선 공정 단독 혹은 자외선/초음파 혼합 공정이 효율적인 공정으로 제시되었으며, 대상 오염물질에 따라 포화 가스를 변화시키는 등의 추가 기법을 적용할 수 있을 것으로 판단되었다.
본 연구는 환경부 지중환경오염위해관리기술개발사업(No. 2021002470001)에 의해 지원받은 과제입니다. 본 성과물은 중소벤처기업부에서 지원하는 2020년도 산학협력 거점형 플랫폼(R&D) (S3012072)의 연구수행으로 인한 결과물임을 밝힙니다.
- 1. Beckett, M.A. and Hua, I., 2001, Impact of ultrasonic frequency on aqueous sonoluminescence and sonochemistry, J. Phys. Chem. A, 105(15), 3796-3802.
-

- 2. Chang, F.C., Chiu, T.C., Yen, J.H., and Wang, Y.S., 2003, Dechlorination pathways of ortho-substituted PCBs by UV irradiation in n-hexane and their correlation to the charge distribution on carbon atom, Chemosphere, 51(8), 775-784.
-

- 3. Choi, J., Lee, H., and Son, Y., 2021, Effects of gas sparging and mechanical mixing on sonochemical oxidation activity, Ultrason. Sonochem., 70, 105334.
-

- 4. Ghafoori, S., Mowla, A., Jahani, R., Mehrvar, M., and Chan, P.K., 2015, Sonophotolytic degradation of synthetic pharmaceutical wastewater: Statistical experimental design and modeling, J. Environ. Manage., 150, 128-137.
-

- 5. Gonzalez, M.C., Le Roux, G.C., Rosso, J.A., and Braun, A.M., 2007, Mineralization of CCl4 by the UVC-photolysis of hydrogen peroxide in the presence of methanol, Chemosphere, 69(8), 1238-1244.
-

- 6. International Agency for Research on Cancer (IARC), 2016, Polychlorinated Biphenyls and Plybrominated Biphenyls.
- 7. Li, B., Li, L., Lin, K., Zhang, W., Lu, S., and Luo, Q., 2013, Removal of 1,1,1-trichloroethane from aqueous solution by a sono-activated persulfate process, Ultrason. Sonochem., 20(3), 855-863.
-

- 8. Matafonova, G. and Batoev, V., 2019, Review on low- and high-frequency sonolytic, sonophotolytic and sonophotochemical processes for inactivating pathogenic microorganisms in aqueous media, Water Res., 166, 115085.
-

- 9. Miao, X.S., Chu, S.G., and Xu, X.B., 1999, Degradation pathways of PCBs upon UV irradiation in hexane, Chemosphere, 39(10), 1639-1650.
-

- 10. Ministry of Environment (MOE), 2021, White Book of Environmental Monitoring Report on Persistent Organic Pollutants (POPs)
- 11. Nasseri, S., Mahvi, A.H., Seyedsalehi, M., Yaghmaeian, K., Nabizadeh, R., Alimohammadi, M., and Safari, G.H., 2017, Degradation kinetics of tetracycline in aqueous solutions using peroxydisulfate activated by ultrasound irradiation: Effect of radical scavenger and water matrix, J. Mol. Liq., 241, 704-714.
-

- 12. Pétrier, C., Combet, E., and Mason, T., 2007, Oxygen-induced concurrent ultrasonic degradation of volatile and non-volatile aromatic compounds, Ultrason. Sonochem., 14(2), 117-121.
-

- 13. Rao, Y., Yang, H., Xue, D., Guo, Y., Qi, F., and Ma, Y., 2016, Sonolytic and sonophotolytic degradation of Carbamazepine: Kinetic and mechanisms, Ultrason. Sonochem., 32, 371-379.
-

- 14. Tang, T., Zheng, Z., Wang, R., Huang, K., Li, H., Tao, X., Dang, Z., Yin, H., and Lu, G., 2018, Photodegradation behaviors of polychlorinated biphenyls in methanol by UV-irradiation: Solvent adducts and sigmatropic arrangement, Chemosphere, 193, 861-868.
- 15. Xu, L.J., Chu, W., and Graham, N., 2013, Sonophotolytic degradation of dimethyl phthalate without catalyst: Analysis of the synergistic effect and modeling, Water Res., 47(6), 1996-2004.
-

- 16. Zhang, G. and Hua, I., 2000, Cavitation Chemistry of Polychlorinated Biphenyls: Decomposition Mechanisms and Rates, Environ. Sci. Technol., 34(8), 1529-1534.
-

 This Article
This Article
-
2021; 26(4): 1-7
Published on Aug 31, 2021
- 10.7857/JSGE.2021.26.4.001
- Received on Jul 8, 2021
- Revised on Jul 12, 2021
- Accepted on Jul 23, 2021
 Services
Services
Shared
 Correspondence to
Correspondence to
- Younggyu Son
-
1Department of Environmental Engineering, Kumoh National Institute of Technology
2Department of Energy Engineering Convergence, Kumoh National Institute of Technology - E-mail: yson@kumoh.ac.kr





