- The Potential Application of Passive Sampling Techniques in Contaminated Soil and Groundwater
Pil-Gon Kim1·Joungho Park2·JaeKyoung Moon2·Jung-Hwan Kwon1·Jihee Kim3·Seunghee Han3·Yongseok Hong2*
1Division of Environmental Science and Ecological Engineering, Korea University
2College of Science and Technology, Korea University Sejong Campus
3School of Earth Sciences and Environmental Engineering, GIST- 오염 토양 및 지하수에서 수동샘플러 적용 방안 연구
김필곤1·박중호2·문재경2·권정환1·김지희3·한승희3·홍용석2*
1고려대학교 환경생태공학부
2고려대학교 환경시스템공학과
3광주과기원 환경공학부This article is an open access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/4.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Passive samplers are environmental monitoring devices that are accumulating pollutants in adsorbing medium by diffusion. They are distinguished from active samplers which are generally required electric power to create artificial and advective movements facilitating mass transport from environment to samplers’ adsorbing parts. Passive samplers have been applied to various environmental media such as air, water, sediment, groundwater, and soil with different but could be sometimes similar purposes. They have been primarily used to measure concentrations of pollutants in both homogeneous and heterogeneous environments with high resolution in space, i.e., millimeters. They also have been used to quantify time weighted average concentrations without multiple sampling efforts at different times. Human and ecological risk assessments are also a representative example for the application of passive samplers. However, it is hard to find a case study in Korea that passive samplers have ever applied in soil and groundwater with any of those purposes. In this research, extensive literatures are reviewed to identify the utility of passive sampler application on various environmental media and diverse pollutants including VOCs, HOCs, heavy metals, and etc. Finally, the potential uses of passive sampling techniques to the area of soil and groundwater science and engineering are critically evaluated
Keywords: Passive sampler,Soil, Groundwater, Heavy metals, Organic pollutants
현재 우리나라에서 유기오염물질 및 중금속과 같은 무기오염물질에 대한 토양 위해성평가는 주로 토양 내 오염물질의 총 농도를 기반으로 이뤄지고 있다(환경부, 2015). 하지만 토양의 총 농도를 바탕으로 한 위해성평가는 인간이나 다른 여러 생물을 대상으로 한 오염물질의 생물이용도를 잘 반영하지 못하는 단점이 있다(한국지하수토양환경학회, 2008). 토양 내의 유무기오염물질 중 일부는 토양입자나 토양유기물질과 강하게 결합하고 있기 때문에 생물체내로 확산에 의해 잘 흡수되지 않으며 토양 공극이나 공극수에 자유롭게 용해된 물질이 생물이용가능(bioavailable)한 것으로 간주된다(NRC, 2003). 그렇기 때문에 토양의 총 농도를 바탕으로 한 위해성평가는 종종 토양오염물질에 의한 위해도를 과대평가하게 되는 경향이 있다(USEPA, 2007). 이러한 문제점을 반영하고, 오염물질의 생물이용도를 고려한 위해성평가 및 관리를 위해서 여러 가지 방법들이 고안되고 거론되고 있다.
예를 들면 유기오염물질의 생물이용도가 토양 속 총 유기탄소가 늘어날수록 감소한다는 측면을 이용해 토양 속 총 농도에 토양 속 총 유기탄소율을 적용하여 공극수내 농도를 예측하는 방법이 있다. 하지만 유기오염물질 분배계수의 불확실성으로 인해 실제로 오염된 토양에서 유기오염물질의 생물이용도(bioavailability)를 판단하기에는 부족하다고 알려져 있다(Arp et al., 2014). 또 다른 방법으로는 토양 침출 방법(leaching test)이 있는데 이 방법은 유기오염물질의 생물이용도 측정보다는 유기오염물질의 토양 속 거동이나 입자상, 중 생물에 접촉이 가능하거나 생물에 전달이 가능한(bioaccessibility) 오염물질을 분석할 때 더 적합하다는 평가가 있다(Enell et al., 2016). 여러 연구에서 수동샘플러를 이용해 토양 공극수에 자유롭게 녹아 있는(freely dissolved) 유기오염물질의 농도를 측정하고 이를 물질의 생물이용도 평가에 적용해야 한다고 주장하고 있다.
중금속의 경우도 이와 유사하게 토양내 총 농도 보다는 이용성 농도(labile concentration) 또는 자유이온농도(free ion activity)에 의존하므로 이 두 가지의 농도를 측정하는 방법이 오랜 기간 동안 연구되어 왔다. 이용성 농도를 산정하는 방법 중 화학평형모델이 있지만, 리간드 농도를 파악하기 어려운 문제점으로 자연수의 적용에 제한성이 있다. 즉 다수의 중금속이 용존 유기물과 반응하여 착화합물을 형성하나 용존 유기물의 조성을 파악하기 어려우므로 여러 가지의 가설이 개입되고 이러한 가설은 모델의 신뢰성을 낮추게 된다. 따라서 모델의 사용은 실험을 통한 보정 과정을 필요로 하는데 실험적으로 자연수의 이용성 중금속 농도를 수동샘플러로 직접 측정하는 것이 더 신뢰성이 있다고 주장하고 있다.
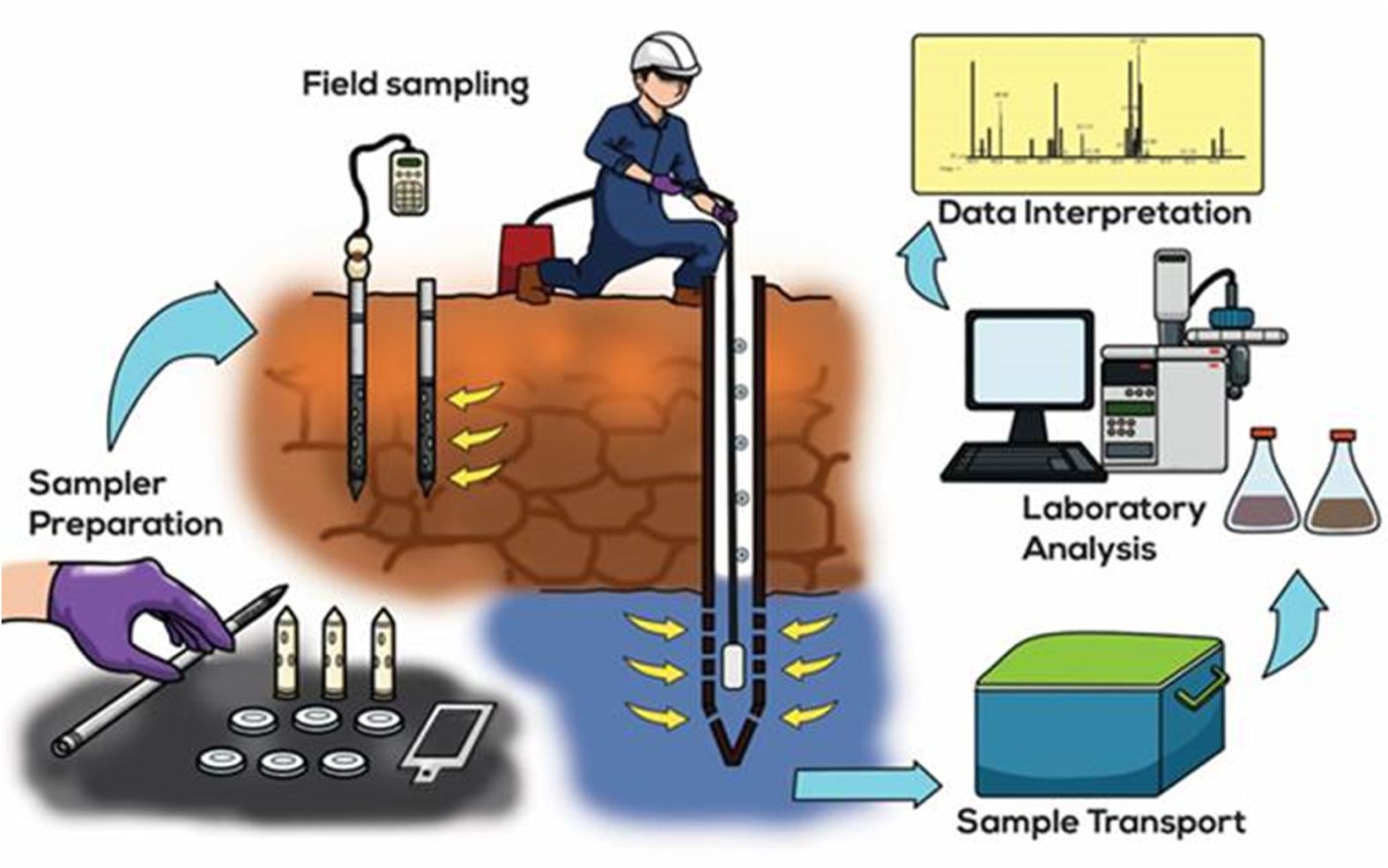
수동샘플러란 특별한 동력 없이 화학포텐셜 차이에 의한 오염물질 확산현상에 의해 오염물질을 농축하는 시료채취 방법으로 정의되며(Górecki and Namienik, 2002), 현장의 특성을 반영하여 다양한 형태로 제작이 가능하며 확산 및 흡착 또는 흡수 기작에 기반을 하므로, 적절한 흡착제나 흡수제만 있다면 거의 모든 오염물질에 적용이 가능하다(Kot et al., 2000; Górecki and Namienik, 2002; Vrana et al., 2005; Greenwood; et al., 2007; Kot-Wasik et al., 2007; Seethapathy et al., 2008). Fig. 1은 토양 및 지하수에 수동샘플러를 적용하는 과정을 보여준다. 이러한 수동샘플러는 폐수, 물환경, 대기, 토양 및 퇴적물 등 거의 모든 환경에 적용되어왔으며 중금속, 잔류성유기오염물, 휘발성유기오염물 등 다양한 유무기 환경 오염물질에 적용이 되어 왔다(Seethapathy et al., 2008). 최근에는 환경 호르몬물질이나 의약물질 등 신종오염물질들을 수동샘플러로 포집하는 연구들이 다양하게 진행되고 있다(Ort et al., 2010; Kaserzon et al., 2012; Challis et al., 2016; Fauvelle et al., 2017).
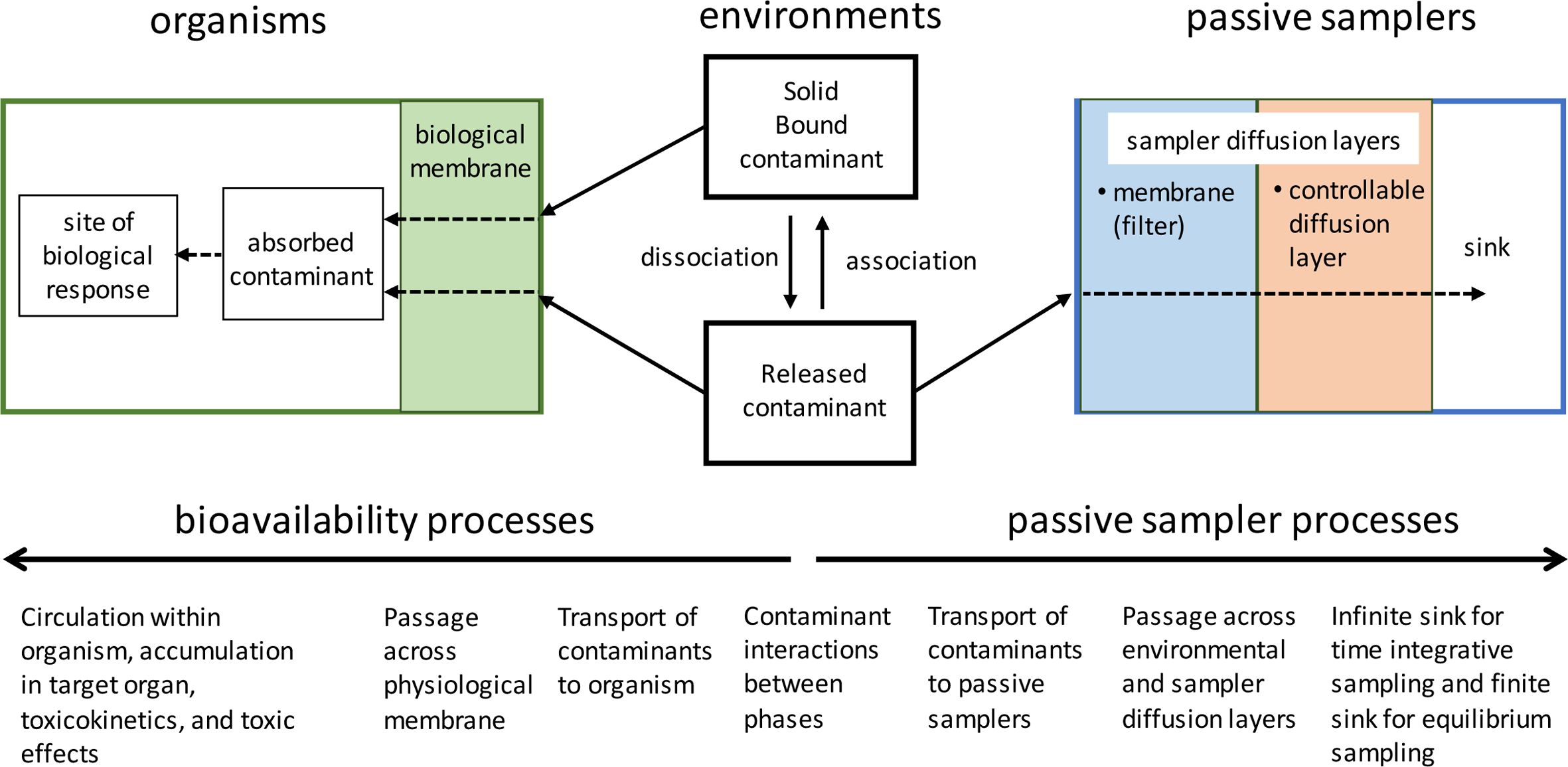
수동샘플러는 Fig. 2와 같이 생물이 오염물질을 흡수하는 과정과 유사하게 작동한다고 알려져 있다. 다양한 형태의 수동샘플러가 존재하지만 일반적으로 오염물질이 확산할 수 있는 확산층(diffusion layer)을 가지고 있고, 그 뒤에 확산에 의해 샘플러 안으로 들어온 오염물질을 강하게 흡착하거나 흡수하는 층을 가지고 있다. 환경에 설치되면 종종 샘플러 바깥에 확산경계층(diffusive boundary layer)에 의해 추가적인 확산층이 생성되기도 한다. 흡수/흡착층이 설치기간동안 지속적으로 오염물질을 흡수/흡착한다면(infinite sink) 확산층에 농도구배(concentration gradient)에 의해 지속적인 물질 플럭스가 발생하여 시간에 따라 선형적인 오염물질 농축이 가능하다. PDMS (Polydimethylsiloxane)나 POM(polyoxymethylene)과 같은 폴리머계열의 샘플러는 확산층이 따로 존재하지 않고, 오염물질을 흡수하는 층만 존재하며, 이는 확산 및 흡수가 동시에 일어나는 샘플러 매질만이 존재한다. 이런 경우 기본적으로 환경내 오염물질과 샘플러간에 평형이 일어나기를 기대하고 평형분배계수를 이용하여 환경내 오염물질의 농도를 측정하며, PRCs(performance reference compounds)를 이용하여 평형이 되기 전에 샘플링을 중단해도 환경내 오염물질의 농도를 측정할 수 있게 한다. 이러한 환경내에서 오염물질의 생물체내 농축과 샘플러내 농축의 유사성으로 인해, 수동샘플러는 오염물질의 생물이용 가능성 예측성과 관련되어 많은 연구가 진행되었다.
이 외에도 수동샘플러는 용존상태의 오염물질의 농도를 예측하는데 사용되는 것이라 할 수 있다. 토양 또는 퇴적물의 공극수 농도를 측정할 때 수동샘플러를 적용하면, 현장시료를 채취해와서 분석하는 grab sampling시 발생하는 원심분리 및 필터링 그리고 농축과 같은 복잡한 과정이나, 그동안 일어 날수 있는 생지화학 반응에 의한 농도의 변화와 같은 불확실성을 줄일 수 있는 장점이 있다. 수동샘플러는 주로 물환경 및 대기에 응용되어 왔으며, 토양의 경우 주로 공극수의 오염물질 농도를 측정하거나 생물이용도를 예측하기 위해 사용되었으며, 지하수의 경우 grab sampling이 가진 단점을 극복하기 위해 사용되어왔으나, 대체적으로 두 환경 매체에 대한 적용은 다른 환경 매체에 비해서는 비교적 제한적이었다. 본 연구에서는 주로 토양 및 지하수 분야에 사용되었던 수동샘플러를 오염물질별 및 매체별로 구분하여 정리하고, 그 목적 및 특성을 기술하였다. 오염물질의 경우 우리나라 토양지하수에서 관리되는 오염물질 중 중금속, 잔류성유기오염물(PAHs, PCBs), 및 휘발성유기오염물 위주로 정리하였다.
|
Fig. 1 General passive sampler application practice in soil and groundwater |
|
Fig. 2 comparison of bioavailability and passive sampler processes. Modified from (NRC, 2003) |
2.1. 토양에 적용된 수동샘플러
토양내 중금속, 잔류성유기오염물, 및 휘발성유기화합물은 Table 1과 같이 다양한 형태의 수동샘플러로 시료채취 되었다. 단순히 농도를 예측하는 것부터 위해성평가까지 다양한 목적으로 활용되어 왔다. 자세한 내용은 아래와 같다.
2.1.1. 토양 중금속 수동샘플러
토양내 중금속의 생물이용가능성 평가를 위해 또는 토양공극수내 중금속 농도를 측정하기 위해 주로 DGT(diffusive gradient in thin film probe)나 DET (diffusive equilibrium in thin film probe)와 같은 샘플러들이 주로 이용되었다(Yong Seok, H., 2013). DGT는 다양한 목적에 이용 가능한데 식물 뿌리에 의해 유도되는 토양 중금속 또는 영양염의 흡수를 정량적으로 설명하기 위한 거동 모사에 이용되기도 한다. 예를 들어 서로 다른 조성을 가진 토양에 DGT 장치를 설치 측정한 후 DIFS (DGT-induced fluxes in soils) 모델을 이용하여 이용성 Zn, Cd, Ni의 분배계수(Kdl)와 입자에서 토양수로의 재공급 반응시간(Tc)을 구한 보고가 있다(Ernstberger et al., 2005). 같은 논문에서 DGT에 의하여 유도된 중금속의 재공급 플럭스는 토양 내 이용성 중금속 종의 농도, 그리고 이들의 흡탈착 동역학에 의존하는 것으로 확인되었다. 공극 크기를 조절한 분산젤을 이용하여 분자량이 작은 이용성 금속 농도를 측정하고 토양 공극수 고갈과 재공급 속도상수를 산정한 예시도 있다(Doèekalová et al., 2012).
최근에 들어서는 DGT가 토양 중금속의 생물이용도(bioavailability) 측정 및 예측에 많이 이용되고 있다. 모든 연구에서 DGT는 BCR, NIST에서 제시한 다단계 추출과정 중 한 과정으로 사용되는 순차추출법(sequential extraction)이나 공극수 추출법에 비하여 매우 낮은 이용성 중금속 농도를 얻었다. 한 예로 오염토와 일반토에서 용해성 Cu의 농도는 토양 총농도에 0.2% 이하로, DGT로 측정한 생물이용성 농도는 토양 총 농도의 0.06% 이하로 측정되어서 DGT 농도/공극수 농도의 비는 0.2-0.8로 산정되었다(Cattani et al., 2006). 토양슬러리를 제조하여 DGT로 생물이용성 중금속 농도를 측정한 결과 DGT 농도가 화학추출법 농도보다 1000-10000배 정도 적은 결과를 보여주기도 하였다(Doèekalová et al., 2012). Table 1의 연구 중 일부는 DGT가 화학추출법 또는 순차추출법과 비교하여 생물시료의 중금속 농도를 더 잘 예측하는 결과를 보여주었다(Vandenhove et al., 2007; Yao et al., 2017). 일례로 야생벼를 이용하여 Cd의 생물이용도를 측정한 결과 DGT로 산정한 공극수 Cd 농도는(CDGT) 재래적 화학추출법(EDTA, HAc, CaCl2)으로 측정한 농도에 비하여 식물의 Cd 농도와 더욱 높은 상관성을 보였다(Yao et al., 2017). 또 다른 예로 서로 다른 수준의 U 오염 토양에 독보리의 씨를 심고 수주 후에 뿌리와 그 윗부분을 수확한 후 각 부분의 총 U 농도를 측정하고 이를 DGT 및 화학추출법과 비교한 결과, DGT는 재래적 화학추출법에 비하여 식물 U 농도와 더욱 높은 상관성을 보였다(Vandenhove et al., 2007). DGT를 이용한 생물이용성 예측을 주제로 한 대부분의 논문이 식물의 이용성에 중점에 두고 있는데 이는 DGT에 의한 중금속 흡수 후 공극수 농도의 고갈이라는 기본 메커니즘이 식물 뿌리의 작용과 매우 유사하기 때문이다. 최근에는 DGT를 이용하여 동물에 의한 토양 중금속 이용성을 평가한 연구 결과가 보고되었다(Bade et al., 2012). 이 연구는 지렁이, Eisenia foetida,의 Pb, Zn, Cu 축적을 DGT 측정으로 설명하고자 하였는데 DGT로 측정한 농도는 지렁이(Eisenia foetida) 조직 농도 및 순차추출의 생물이용성 농도(I+II of the standard measurements and testing, SM&T I+II), 생리적추출 농도(PBET, stomach+intestine)와 매우 좋은 연관성을 보였다(Bade et al., 2012).
많은 논문에서 생물이용성의 예측을 위하여 레진젤 내 중금속 질량을 측정한 후 분산계수를 이용하여 레진의 경계면 공극수의 중금속 농도(CDGT)를 재산출하는 방법을 사용하였는데, 이 농도 보다는 레진으로의 중금속 플럭스가 생물이용성 예측에 더욱 효과적임이 최근의 논문에서 제시되었다(Simpson et al., 2012; Amato et al., 2015; Amato et al., 2016). 이는 혼합분산계수가 이용성 화학종의 조성에 의존하나, 공극수 내의 중금속 화학종을 파악하기 어렵고 각 화학종마다 분산계수가 정확히 알려져 있지 않은 이유에 기인한다.
DGT를 이용한 퇴적물 중금속의 생물이용성과 독성 평가에 대한 연구 또한 꾸준히 보고되고 있다(Roulier et al., 2008; Simpson et al., 2012; Amato et al., 2015; Amato et al., 2016). 퇴적물의 경우는 대상 생물로써 새우류, 조개류, 달팽이류 둥의 저서무척추 동물이 주로 실험되었고, DGT 생물이용성 결과는 순차추출법, 산휘발성황화물 동시추출법(acid volatile sulfide-simultaneously extracted metals, AVS-SEM) 뿐 아니라 생존률, 번식률 등의 급성 독성 평가법과도 비교되었다(Simpson et al., 2012; Yin et al., 2014; Amato et al., 2015; Amato et al., 2016). 일례로 DGT와 쌍각류 조개 Tellina deltoidalis를 Cu 성분의 부착방지 페인트로 오염된 여러 조성의 퇴적물에 설치하고 DGT플럭스를 상등수와 퇴적물 깊이별로 측정한 연구 보고가 있다(Simpson et al., 2012). 이 연구는 Tellina deltoidalis 생존률로 측정한 생물 독성도를 상등수의 DGT Cu 플럭스와 연관하였을 때 매우 좋은 노출-반응 관련성을 보여서 DGT가 독성의 평가에도 유용한 도구임을 입증하였다(Simpson et al., 2012).
토양과 마찬가지로 퇴적물에 대한 여러 문헌에서도 전반적으로 DGT 방법이 순차추출법이나 산휘발성황화물 동시추출법 보다 좋은 결과를 보였다(Roulier et al., 2008; Simpson et al., 2012; Amato et al., 2015; Amato et al., 2016). 이는 화학추출법이나 순차추출법이 특정 용매에 반응하는 중금속 농도를 순간적으로 측정하는 원리임에 비하여, DGT검출법은 공극수 내 중금속을 소모하고 다시 입자에서 반응성 중금속을 재공급하는 역학적 과정을 기본으로 하므로 토양입자가 가진 생물이용성을 보다 정교하게 그리고 긴 시간에 걸쳐 측정하기 때문으로 생각된다. 그러나 DGT를 이용한 생물이용성과 독성 측정 결과는 토양, 중금속, 그리고 생물의 종류에 따라 서로 다른 특징을 보이므로, DGT 적용에 앞서서 특정 중금속과 생물을 대상으로 면밀한 조사가 선행되어야 한다. 그 예로 독보리에 농축된 U 농도와 토양수 농도, 아세테이트 암모늄으로 추출한 농도, DGT 농도를 비교한 결과 식물의 U흡수는 DGT 보다는 토양수나 아세테이트 암모늄 추출 농도로 더욱 잘 예측되었고(Duquène et al., 2010), 퇴적물에 설치한 DGT 연구의 경우 달팽이 조직에 농축된 Cr, Ni, Cu, Pb 농도는 DGT로 예측 가능하였으나 Zn, Cd의 경우는 좋은 연관성을 보이지 않았다(Yin et al., 2014).
위에서 설명한 DGT와 비슷한 기술인 DET는 레진젤이 없이 하이드로젤과 자연수 사이에 평형을 형성하여 중금속 농도를 측정하는 원리이다(Fones et al., 2001; Leermakers et al., 2005). 이 기술은 투석과 매우 비슷하지만 샘플링 매체가 투석막에서 하이드로젤로 대체되면서 막의 공극 크기에 따른 화합종 선택성이 없이 총 농도만을 측정하고 분산젤의 얇은 막이 상대적으로 짧은 시간 내 평형에 이르는 것을 가능하게 한다(Davison and Grime, 1991). 아직까지 DET는 젤의 바탕농도, 농축의 부재, 분석 전 희석의 필요성, 실험과정의 오염 등의 문제로 인하여 분석 가능한 중금속과 시료의 종류가 제한적이다. 예로 하천 퇴적물에 DET 장치를 설치하여 여러 중금속을 측정했을 때 Cd, Pb, Zn, Ni, Cu는 신뢰성 있는 농도를 얻지 못하였고 Fe, Mn, Co, As의 경우는 분석의 신뢰성이 높았다(Leermakers et al., 2005).
DET의 이용사례를 살펴보면 일부 원소의 경우 DET 측정 농도가 원심분리하여 측정한 공극수농도에 비하여 높게 측정된다(Leermakers et al., 2005; Gao et al., 2006; Garnier et al., 2015). 논토양 공극수의 As을 토양 깊이 별로 측정한 경우 DET 측정 농도는 공극수 농도보다 높게 측정되었는데 이는 DET 표면의 수산화철 침전의 결과로 설명되었다(Garnier et al., 2015). 강 퇴적물에서도 동일한 이유로 Fe의 DET 농도가 공극수 농도보다 높은 값을 보였다(Gao et al., 2006). 이러한 문제점에도 불구하고 DET 기술은 대체적으로 원심분리를 이용한 공극수 채취방법에 비하여 높은 해상도를 가진 정교한 프로파일을 제공한다.
2.1.2 토양 잔류성유기오염물 수동샘플러
토양내 잔류성 유기오염물(persistent organic pollutants, POPs)의 생물이용가능성을 예측/평가하기 위해서, LDPE (light density polyethylene), POM, PDMS 등과 같은 폴리머 계열의 시료채취기가 이용되었다. 기존 문헌을 살펴보면 수동샘플러(POM)를 이용해 토양 공극수에 자유롭게 용해된 유기오염물질(PAHs, oxy-PAHs, N-PACs)의 농도를 측정했고 이 농도가 Enchytraeus crypticus를 이용한 독성평가와 생물농축성 평가에 적용해 본 결과 매우 적합하다는 결론을 얻었다(Arp et al., 2014). 그리고 토양 위해성평가를 할 때 수동샘플러를 이용해 측정한 공극수의 농도를 기반으로 물질의 생물이용도를 평가해야 한다고 주장하며 논문을 결론지었다. 또한 토양 속 물질(PAHs, oxy-PAHs, N-PACs)의 생물이용도를 측정하는 방법 중 수동샘플러(POM)와 토양 침출 방법을 비교 분석했고 실험 결과 수동샘플러는 공극수 농도를 측정해 생물이용도를 평가하는데 적합하고 토양 침출 방법은 공극수 속 유기오염물질의 총 농도를 측정해 물질의 거동 측정에 적합하다는 결론을 내렸다(Enell et al., 2016). PAHs를 대상으로 토양 속 물질의 생물이용도를 측정하는 방법 중 수동샘플러(POM)와 exhaustive mild solvent 추출법, cyclodextrin 추출법을 지렁이와 잡초의 PAHs 생물축적 실험을 이용해 비교 분석했고 실험 결과 수동샘플러를 이용해 측정한 공극수의 농도가 가장 적합하다는 결론을 얻었다(Gomez-Eyles et al., 2012). 한 리뷰논문은 수동샘플러(LDPE, PDMS, POM)를 이용해 측정한 물에서의 물질(PCBs, DDTs, CECs, PAHs)의 농도와 여러 다른 연구에서 얻은 다모류, 지렁이류, 쌍각류 조개류, 수생 곤충류, 복족류의 유기오염물질 축적농도를 비교한 결과 수동샘플러가 물질의 생물이용도 측정에 적합하다는 결론을 얻는다(Joyce et al., 2016). 특히 측정농도와 생물 농축농도와의 상관성을 R2 값으로 샘플러 재질마다 비교한 결과 PDMS를 사용할 때 0.76 값으로 가장 높은 연관성을 가졌고 LDPE가 0.68, POM이 0.58의 값을 가졌다.
또한 수동샘플러를 이용해 퇴적물의 공극수 속 유기오염물질의 농도 측정이 가능하고 이를 이용해 물질의 거동과 운송에 대해 예측, 모델링이 가능하며 생물축적과 생물독성에 적용할 수 있고 이는 곧 퇴적물의 위해성평가와 관리로 이어질 수 있다(Mayer et al., 2014). 수중에서 서식하는 지렁이를 이용해 생물축적실험을 진행한 결과와 수동샘플러(POM)를 이용해 측정한 물에 자유롭게 용해된 물질의 농도를 PAHs로 오염된 현장과 실험실조건에서 비교하였고 두 상황 모두 적합했다(Muijs and Jonker, 2012). 마지막으로 다모류 속의 PAHs 농도와 수동샘플러(PE)를 이용해 측정한 퇴적물의 공극수 속 PAHs 농도를 비교 분석해본 결과 선형관계를 나타냈고 이를 통해 수동샘플러가 퇴적물에서 물질의 생물이용도를 측정할 수 있었다(Vinturella et al., 2004). 이처럼 많은 연구에서 수동샘플러를 이용해 토양이나 퇴적물의 공극수, 또는 물에 자유롭게 녹아 있는 유기오염물질의 농도를 측정가능 하고 이를 위해성평가 시 물질의 생물이용도 평가에 적용해야 한다고 주장하고 있다.
이 외에도 많은 연구에서 여러 가지 목적을 위해 수동샘플러를 퇴적물의 공극수 속 자유롭게 용해된 유기오염물질의 농도를 측정하는데 사용했다. 퇴적물(Baltic sea, Newport bay 등)에 수동샘플러를 이용해서 공극수 속 자유롭게 용해된 유기오염물질의 농도를 측정했다(Maruya et al., 2009; Burgess et al., 2015), (Lang et al., 2015). 수동샘플러를 이용해 퇴적물의 공극수 속 유기오염물질의 농도를 측정했고 이를 performance reference compound 검정의 적합성 평가에 이용했다(Apell and Gschwend, 2014; Bao et al., 2016). 수동샘플러를 사용해 퇴적물의 공극수 속 물질의 농도를 측정했고 이를 이용해 퇴적물과 물 사이에서 물질의 흐름, 거동을 평가하는데 사용했다(Fernandez et al., 2014).
또한 많은 연구에서 여러 가지 목적을 위해 수동샘플러를 토양의 공극수 속 자유롭게 용해된 유기오염물질의 농도를 측정하는데 사용했다. 오염된 토양에서 PAHs를 분리해내기 위해 활성탄소를 사용하는 방법의 효율성, 적합성을 확인하기 위해 수동샘플러를 토양에 적용시켰다(Hale et al., 2012). Oil-soot(lampblack)처리한 토양에서 수동샘플러를 이용해 토양과 물 사이 PAHs의 평형분배계수를 측정했다(Hong and Luthy, 2008). 또한 수동샘플러를 이용해 토양 개량이 토양 속 공극수 유기오염물질 농도변화와 식물에게 주는 영향에 대해 분석했다(Marchal et al., 2014). Canola oil이 PAHs의 생물이용도와 생분해에 미치는 영향을 수동샘플러를 이용해 관찰했다(Scherr et al., 2009). 바이오차의 토양 교정효과를 수동샘플러를 이용해 측정한 공극수 유기오염물질의 변화를 비교해가며 분석했고 또한 공극수 농도의 변화와 Folsomia candida, Lepidium sativum, Allivibrio fischeri의 독성평가와 연관지어 설명했다(Stefaniuk and Oleszczuk, 2016). 토양의 공극수 유기오염물질의 농도를 측정하기 위해 수동샘플러를 이용하였다(Ter Laak et al., 2006).
2.1.3. 토양 휘발성유기오염물 수동샘플러
일반적으로 능동샘플링은 대기중 VOCs 샘플링과 유사하게 토양공기를 약 100 mL/min 보다 낮은 공기유량으로 흡입하여 적절한 sample container를 이용하여 샘플링하는 방법이 이용된다. 해외에서는 Dedicated Vapor Probes 또는 GeoProbe PRT system을 이용하여 샘플러를 지반에 설치하고 정량펌프를 이용하여 토양가스를 Tedlar bag이나 스테인리스 스틸 재질의 canister 에 0.5 L/min의 유량으로 샘플링하여 약 2-5 ppbv의 VOCs들을 분석하였다(DiGiulio et al., 2006). 이러한 방법은 공기를 인위적으로 흡입하기 때문에 토양 공극내 VOCs의 농도를 희석하거나 화학적 평형을 교란시켜 부정확한 농도를 제시할 수 있다. 또한 토양의 심도에 따른 조사가 가능하도록 다공성 튜브를 이용해 poly-use multi-level sampling system (PMLS)를 개발해 샘플링한 사례도 있다(Nauer et al., 2013).
이와 같은 능동샘플링 방법 외에 수동샘플링 방법들도 이용되어 왔다. 휘발성 유기오염물로 오염된 부지나 지하수 위에 건설된 건물 지하실에는 종종 휘발성유기오염물(VOCs, sVOCs, Hg, H2S, CH4, Rd, and etc) 침투로 인한 위해성이 발견되기도 한다(USEPA, 2015). 이때 토양증기침투경로(soil vapor intrusion pathway)를 파악하는 것이 위해성을 낮추는데 중요한 역할을 하는데, 토양 공극내 휘발성유기오염물의 농도를 측정하기 위해 수동샘플러가 이용되기도 한다(ITRC, 2007a). 토양 공극내 VOCs의 농도는 토양 총 농도로부터 평형분배를 가정하고 측정하기도 하나 토양 시료 채취시 VOCs 휘발을 최소화 하기위해 메탄올에 안정화시키거나(이런 경우 과대예측함) 상분배 계수 등을 가정해야 함으로 그 예측값에 불확실성이 높다. 직접 측정된 토양 공극내 VOCs의 농도(ug/m3)를 위해성 평가에 직접 사용되기도 한다.
일반적인 적용은 토양에 흡착물질을 가지고 있는 흡착제를 묻어놓고 오염물질 확산에 의해 흡착되는 것을 이용하는 방법이다. 토양 공기를 인위적으로 빼내지 않기 때문에, 토양에서 VOCs의 평형분배 상태를 교란시키지 않는 장점이 있고, time-integrative한 샘플링이 가능하기 때문에 시간에 따른 영향을 최소화할 수 있는 장점도 있다. 토양이 아닌 공기에서 수동샘플링 방법은 ASTM에서(ASTM, 2013, 2016) 그 적용방법에 대해 설명해 놓았으나, 캘리브레이션이 되어 있지 않아 정량적인 농도(ug/m3)로 변환이 어려워, 단순히 샘플러에 농축된 농도 ug으로 결과를 보고하고 있다.
2.2. 지하수에 적용된 수동샘플러
지하수에서 수동샘플링 방법들은 Table 2에 정리하였으며, 다양하게 시도되었다(ITRC, 2007b; Johnson and Hajcak, 2007). 지하수의 경우 토양과 유사하게 지하수 섭취에 의한 위해성을 평가할 때 총농도를 기준으로 하나, 실제 물환경에서도 중금속이나 유기오염물의 경우 일부만 생물이용가능하다는 연구가 많이 있다. 또한 grab sampling이 불가능한 지역에 수동샘플러가 이용되기도 한다. 일반적으로 지하수 관측공에서 지하수 시료를 채취하기 위해 두 가지 일반적인 접근 방법이 사용되고 있다. 첫번째는 소위 말하는 uphole sampling으로 지하수 관측공 아래에서 지하수 시료를 지상으로 펌프를 이용하여 끌어 올려 지상에서 채취하는 방법이며, 두번째는 Fig. 3과 같이 downhole sampling으로 시료채취용 용기를 지하수관측공 아래로 내려 원위치에서 채취하는 방법이 있다(Britt et al., 2010). 현재 우리나라에서는 대부분 첫번째 방법인 지상시료채취 방법을 이용하고 있으며, 이는 시료채취 지하수관측공에 정체된 물이 지하수 수질을 대표하지 못한다는 가정하에 지하수관측공 부피의 3-5배를 제거한 후에 새롭게 고인 지하수를 채취하고 있다(USEPA, 2002; Barcelona et al., 2005). 그러나 여려 연구에 따르면 관측공의 지하수는 정체되어 있지 않고 지하수 펌핑에 따라 대수층에 수문 교란을 일으키고 지상으로 끌어 올리면서 대표성 있는 농도를 분석하지 못할 가능성이 제기되었다(Barcelona and Helfrich, 1986). 또한 일부 지하수 흐름이 느린 지역에서는 지하수 펌핑이 거의 불가능하여 시료채취에 어려움이 있을 수 있다. 일반적으로 지하수는 모니터링 웰을 설치하고 purge and sample 방법으로 샘플링 하여 왔다(USEPA, 2002). 지하수의 경우 투수성이 낮아 지하수 purging 이 불가능한 지역에서 수동샘플러가 적용이 되어 왔다(Britt et al., 2010).
2.2.1. 지하수 중금속 수동샘플러
지하수의 중금속 농도 측정에는 주로 grab sampling이 사용되어 왔으나 오염이 쉽고 검출한계가 높은 단점을 가지므로 이를 극복하기 위한 DGT의 적용이 보고되고 있다(Lucas et al., 2014). DGT 검출기를 지하수에 설치할 경우, pH, 온도, 이온강도, 설치시간 등을 고려해야 하는데 결합층 레진의 종류에 따라 DGT의 적용가능 pH 범위가 결정된다. Chelex-100의 경우 pH 5에서 8.3 사이에서 가능하다. DGT의 설치 시에는 반드시 현장 온도를 측정하여 확산계수에 대한 온도보정을 실시해야 하고(Zhang and Davison, 1995), 이온강도의 경우 0.01-1 M 범위의 이온강도는 중금속 확산에 미치는 영향이 미미한 것으로 보고되었다(Zhang et al., 2014).
지하수의 중금속 검출을 위하여 DGT를 사용한 사례들을 살펴보면 DGT를 플라스틱 재질의 그물망에 설치한 후 이 그물망을 시추공에 삽입하는 방식으로 수심 별 중금속 농도를 측정하였다(Fig. 1) (Lucas et al., 2014). Au의 검출 감도를 높이기 위하여 분산젤 없이 0.13 mm의 필터를 통과한 후 바로 레진층 활성탄에 Au이 흡착 되도록 구성 하였다(Lucas et al., 2014). 활성탄 DGT를 이용하여 측정한 Au의 농도는 모두 검출한계 이상이었고 이를 grab 농도와 비교했을 때 대부분의 시료에서 DGT 농도가 grab 농도 보다 높았는데 최대 5배 까지의 차이를 보였다. 상대적으로 흐름이 느린 지하수의 조건, 극미량 Au 농도 등을 고려할 때 이 정도의 검출은 의미가 있는 결과로 해석되었고, 논문의 저자는 지하수에서 DGT를 이용하기 위해서는 분산층의 효율 그리고 pH, 이온강도, 리간드, 용존유기탄소, 용존산소의 영향에 대한 면밀한 조사의 필요성을 제기하였다(Lucas et al., 2014).
수동형 샘플러의 하나로 자연수의 자유이온 측정이 가능한 도난막기술(Donnan membrane technique, DMT)이 있다. 이 방법은 이온 교환수지를 이용한 자유이온의 수송역학에 기초한 도난막평형(Donnan membrane equilibrium)을 기본원리로 하는데, 이온교환 막을 사이에 두고 한쪽의 용액에만 일정 화학종의 농도가 높으면 삼투압에 기인한 전기적 포텐셜을 발생하여 반대의 전하를 가진 이온의 흐름이 발생하는 원리이다(Temminghoff et al., 2000; Weng et al., 2010). 초기의 DMT 기술은 셀 내부의 공여(donor)용액과 수용(acceptor)용액을 이동시키기 위해 연동펌프를 사용하여 전기의 공급이 가능한 곳으로 현장 채취가 제한되었지만, 이후에 펌프의 사용이 필요 없는 field DMT가 개발되었다(Kalis et al., 2006). 이 기술은 공여용액으로 현장시료를 사용하고 수용용액으로는 시료와 비슷한 이온강도를 가진 Ca(NO3)2 용액을 사용하는데 여기에 EDTA, NTA 등의 인위적 리간드와 휴믹산, 펄빅산의 자연적 리간드를 주입하여 금속의 검출한계를 낮추었다. DMT 검출기를 강이나 호수에 담그면 인위적 펌핑이 없이 자연적 흐름에 의하여 공여와 수용 용액 사이에 양이온 교환이 일어나므로 일정 시간 후에 장치를 수거하고 수용용액을 분리하여 금속 농도를 정량한다. 아직까지 지하수에 적용한 사례는 보고되지 않았다. 유럽 여러 지역의 하천수에 DMT를 테스트 한 결과 Cu의 경우는 자유이온 농도는 Cu의 경우는 총 농도의(0.06 nM) 0.15%, Zn의 경우는 총농도의(237 nM) 13%로 측정되었다(Kalis et al., 2006). 다른 예시에서는 제련소 인근에서 수거한 토양에 물을 주입하여 70%MWHC를 24시간 유지한 후 토양수를 추출하고 DMT를 적용하였다. 총농도에 대한 자유이온의 비율이 Cd은 3–52%, Zn는 11–72%로 측정되어서 Cu(0.2-30%)와 Pb(0.6-10%)에 비하여 높은 비율을 보였다(Kwon-Rae and Owens, 2009).
2.2.3. 지하수 휘발성유기오염물 수동샘플러
지하수에서 VOCs를 수동성 샘플링하는 경우 Fig. 4과 같이 다양한 종류의 샘플러가 사용되었다. 30-60 cm 길이의 저밀도 폴리에틸렌백에 초순수를 채워 VOCs 모니터링을 하였다(Vroblesky, 2001a, b). 이 샘플러는 지하수내 VOCs와 수동샘플러간의 평형분배를 이용하는 샘플러이고 오염물질 및 온도에 따라 48-166 hr의 시간이 필요하였으며 약 2주 정도면 거의 모든 오염물질 및 다양한 지하수 환경조건에서 샘플링이 가능하였다. Needle type의 수동샘플러도 개발되어 지표수나 기상에 존재하는 휘발성유기오염물을 측정하는데 이용되고 있다(Asl-Hariri et al., 2014; Go and Eom, 2014). 지하수 관측공에 양끝단이 열려있는 샘플링 바틀을 원하는 위치까지 내리고, 일정시간 시료채취 후 양끝단에 달려있는 뚜껑을 닫아 샘플링하는 방법이 시도 되었다(Britt et al., 2010). 지하수에 녹아있는 VOCs를 샘플링하기 위해, 속이 비어있는 바이알 입구를 LDPE로 싸매고, 지하수에 설치하여, VOCs 확산에 의해 바이알 안으로 샘플링하는 방법이 시도되었다(Divine and McCray, 2004). POM의 경우 물환경(지표수 및 퇴적물 공극수)에 적용하여 TCE나 PCE와 같은 VOCs를 equilibrium passive sampling 하는 목적으로 사용되었다(Endo et al., 2011). 세라믹재질의 튜브안에 VOCs를 강하게 흡착하는 물질을 채워, 지하수에 녹아있는 VOCs를 수동샘플링하였고, grab sampling 과 비교하였다(Martin et al., 2003).
2.2.2. 지하수 잔류성유기오염물 수동샘플러
지하수에서 잔류성유기오염물을 수동샘플링하기 위해 다양한 형태의 샘플러가 사용되었다. 두께 0.15 cm, 표면적 8.5 cm2의 세라믹 튜브에 흡착제로 사용한 Amberlite IRA-743 1.5 g을 채우고 테플론으로 만들어진 뚜껑을 이용해 밀봉한 뒤 스테인리스 스틸로 된 틀에 넣어 PAHs 모니터링을 하였다(Bopp et al., 2005). 이 샘플러는 물질 흡착 속도를 이용해 지하수의 농도를 측정하였으며 1년 동안 현장에 설치되었고 장기간 동안 시간가중평균 농도 측정이 가능하였다. 91 cm 길이의 Low-density polyethylene (LDPE) 튜브에 lipid-triolein을 주입한 semipermeable membrane device sys tem(SPMD) 형태의 수동샘플러도 PAHs, OCP 등 다양한 잔류성 유기오염물질의 농도를 측정하는데 사용되었다(Koèí et al., 2009). 마찬가지로 물질 흡착속도를 이용해 지하수의 농도를 측정하였다. 활성탄소 또한 수동샘플러의 재질로 사용되어 pesticides, halogenated solvents, nonhalogenated solvents, domestic and personal, plasticizers, additives를 포함한 유기오염물질의 지하수 농도를 측정했다(Mali et al., 2017). 3 g의 활성탄소를 스테인리스 스틸로 제작한 틀에 넣어 사용했다. Perfluoroalkyl sulfonates(PFSAs), perfluoroalkyl car- boxylates(PFCAs), perfluorooctane sulfo-namides(FOSAMs), fluorotelomer sulfonates(FTS) 등의 지하수내 잔류성 유기오염물질 측정을 위해 폴리에틸렌을 이용해 제작한 수동샘플러가 사용되었고 평형분배 현상을 이용했다(Kaserzon et al., 2019). 83일 동안 현장에 설치되었고 grab sampling과 높은 상관성을 보여 수동성 샘플링의 정확성을 확인했다.
2.2.3. 지하수 휘발성유기오염물 수동샘플러
지하수에서 VOCs를 수동성 샘플링하는 경우 Fig. 4과 같이 다양한 종류의 샘플러가 사용되었다. 30-60 cm 길이의 저밀도 폴리에틸렌백에 초순수를 채워 VOCs 모니터링을 하였다(Vroblesky, 2001a, b). 이 샘플러는 지하수내 VOCs와 수동샘플러간의 평형분배를 이용하는 샘플러이고 오염물질 및 온도에 따라 48-166 hr의 시간이 필요하였으며 약 2주 정도면 거의 모든 오염물질 및 다양한 지하수 환경조건에서 샘플링이 가능하였다. Needle type의 수동샘플러도 개발되어 지표수나 기상에 존재하는 휘발성유기오염물을 측정하는데 이용되고 있다(Asl-Hariri et al., 2014; Go and Eom, 2014). 지하수 관측공에 양끝단이 열려있는 샘플링 바틀을 원하는 위치까지 내리고, 일정시간 시료채취 후 양끝단에 달려있는 뚜껑을 닫아 샘플링하는 방법이 시도 되었다(Britt et al., 2010). 지하수에 녹아있는 VOCs를 샘플링하기 위해, 속이 비어있는 바이알 입구를 LDPE로 싸매고, 지하수에 설치하여, VOCs 확산에 의해 바이알 안으로 샘플링하는 방법이 시도되었다(Divine and McCray, 2004). POM의 경우 물환경(지표수 및 퇴적물 공극수)에 적용하여 TCE나 PCE와 같은 VOCs를 equilibrium passive sampling 하는 목적으로 사용되었다(Endo et al., 2011). 세라믹재질의 튜브안에 VOCs를 강하게 흡착하는 물질을 채워, 지하수에 녹아있는 VOCs를 수동샘플링하였고, grab sampling 과 비교하였다(Martin et al., 2003).

|
Fig. 3 Deployment of passive samplers to groundwater
monitoring well. |

|
Fig. 4 Various types of passive sampler for VOCs (by turns, Gore Module, Hydrasleeve, Snap sampler, regenerated cellulose dialysis membrane sampler (ITRC, 2007b), syringe-silicone tubing samplers (Spalding and Watson, 2006)). |
본 연구에서는 수동샘플러를 중금속, 잔류성유기오염물, 휘발성유기오염물로 오염된 지하수, 토양에 적용한 다수의 해외 연구 및 논문을 목적 및 특성에 따라 정리했다. 중금속의 경우 토양내 생물이용가능성 평가를 위해 또는 토양공극수내 농도를 측정하기 위해 주로 DGT나 DET를 사용했으며 많은 연구에서 수동샘플러가 생물이용농도 및 독성 예측에 적합하다는 결론을 제시했고 이는 퇴적물에도 적용되었다. 잔류성유기오염물의 경우 토양내 생물이용가능성을 예측/평가하기 위해서, LDPE, POM, PDMS 등과 같은 폴리머 계열의 시료채취기가 보편적으로 이용되었다. 중금속과 마찬가지로 많은 연구에서 다양한 생물의 축적농도와 비교해 생물이용농도 예측 적합성을 보여주었고 퇴적물에서도 같은 결과를 나타냈다. 휘발성유기오염물의 경우 능동샘플링와 비교하여 토양 공기를 인위적으로 빼내지 않기 때문에, 토양에서 VOCs의 평형분배 상태를 교란시키지 않는 장점이 있고, time-integrative한 샘플링이 가능하기 때문에 시간에 따른 영향을 최소화할 수 있는 장점도 있다. 하지만 토양 총 농도로부터 평형분배를 가정하고 측정하거나 상분배 계수 등을 가정해야 하는 등 불확실성의 가능성이 있다. 지하수의 경우 uphole sampling, downhole sampling을 포함한 grab sampling이 주로 사용되지만 여려 연구에 따르면 관측공의 지하수는 정체되어 있지 않고 지하수 펌핑에 따라 대수층에 수문 교란을 일으키고 지상으로 끌어 올리면서 대표성 있는 농도를 분석하지 못할 가능성이 제기되었고 지하수 흐름이 느린 지역에서는 지하수 펌핑이 거의 불가능하여 시료채취에 어려움이 있을 수 있어 수동샘플러가 사용되기도 한다. 중금속은 오염이 쉽고 검출한계가 높은 grab sampling의 단점을 극복하기 위해 DGT, DMT가 주로 사용된다. 잔류성 및 휘발성유기오염물은 LDPE 등의 폴리머가 주로 사용되며 grab sampling 결과와 높은 상관성 및 정확성을 보여주었다.
그러나 국내 토양 지하수 분야에서 수동샘플러를 적용한 사례를 찾기는 어렵다. 국내 적용을 고려해 봤을 때 수동샘플러가 1차적으로 사용될 수 있는 부분은 오염 지하수 및 토양현장에서 시행되는 기초/개황/정밀조사 단계나 그 이전에 screening 단계에서 오염지역에 적용하여 수직 및 수평오염 분포 파악하는데 사용될 수 있다. 이는 오염 현장을 공간적으로 촘촘하게 샘플링하게 하여 Fig. 5와 같이 보다 입체적이고 보다 정확한 conceptual site model(CSM)을 구축하게 하여 효과적인 위해성 평가를 통한 합리적인 오염정화 공법 및 전략선정, 그리고 정화 목표 산정에 기초 자료로 사용될 수 있다. 또한 오염부지에 대해 오염 총농도를 낮추는 정화공법이 아닌, 위해성을 낮추는 안정화 또는 고형화 공법 적용 이후, 그 효과를 평가하는데도 유용하게 사용할 수 있다.
그리고 위해성 평가 분야에도 이용이 가능하다. 국내 환경부 예규 383호 “토양오염 위해성평가지침을 살펴보면 현재 우리나라 위해성 평가는 주로 발암 비발암 인간겅강위해성만을 평가하도록 되어 있으며 농작물 섭취, 지하수 섭취, 토양섭취, 토양접촉, 비산먼지흡입, 휘발물질흡입을 주요 노출경로로 고려하고 있다. 이때 유무기 오염물의 토양, 지하수, 및 농작물의 농도가 주요 노출농도로 사용되고 있고, 섭취흡수계수(FI)를 이용하여(생물이용가능성과 유사) 토양노출농도 중 실제 인체에 흡수되는 농도를 보정하도록 되어 있다. 그러나 이와 같은 계수는 현장 토양 및 지하수의 생지화학적 특성에 따라 변할 수 있으므로, FI=1로 추천하고 있고 실제 FI 측정법에 대해 표준화된 방법이 존재하고 있지 않다. 특히 휘발성 유기오염물의 경우 휘발되어 공기중 흡입이 가능한데, 이때 토양내 휘발가능한 휘발성유기오염물의 농도를 정량적으로 측정하기는 매우 어렵다. 이렇게 위해성 평가 시 필요한 환경 매체 별 오염물질의 농도는 매체내 총농도를 주로 이용하지만, 대부분의 경우 섭취 한 화학 물질의 독성은 부분적으로 위장관에서 신체로 흡수되는 정도에 따라 다르다. 인간건강 위해성 평가 시 구강을 통한 섭취한계량(oral reference doses, RfDs)과 암 기울기 계수(cancer slope factor, CSFs)는 다양한 노출경로를 통한 섭취량을 통하여 섭취 선량으로 일반적으로 표현되기 때문에 여러 노출 매체 사이의 흡수의 잠재적 차이를 고려하는 것이 부지 위해성 평가에 중요 할 수 있다(USEPA, 1989, 2007). 또한 수동샘플러를 이용하면 현재 위해성 평가에서는 고려하고 있지 않은 생태위해성평가로의 확장도 가능하다. 본 연구에서 정리한 문헌들의 목적을 포함한 다양한 용도로 국내 토양 및 지하수 연구에 수동샘플러를 적용 가능할 것으로 예상된다.
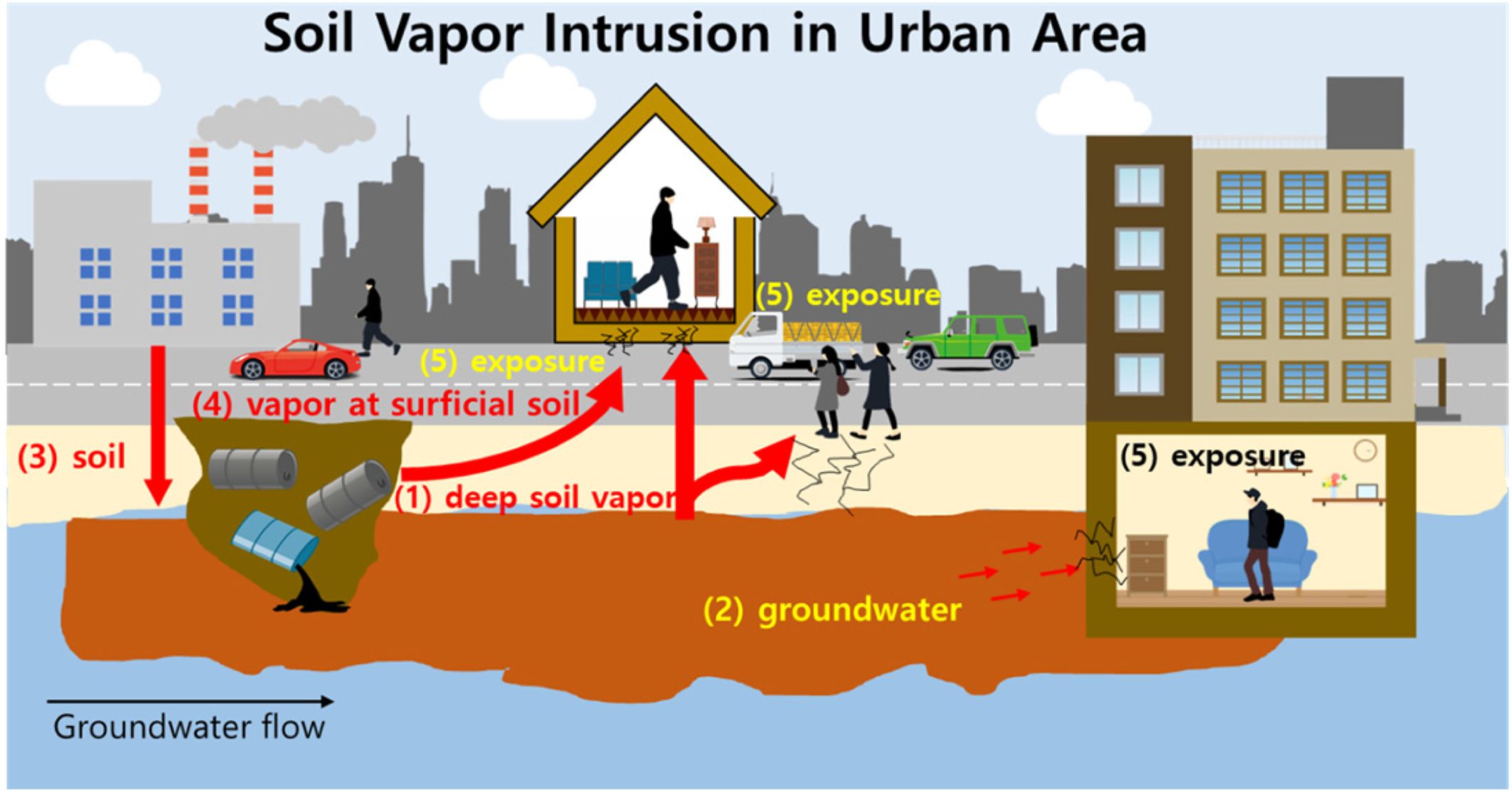
|
Fig. 5 Potential application of passive samplers in soil and groundwater pollution. (1) VOCs sampling in deep soil vapor, (2) groundwater monitoring, (3) monitoring of pollutants in soil, (4) vapor phase VOCs in surficial soil, and (5) determining exposure concentrations to organisms. |
본 연구는 환경산업기술원 지중환경오염위해관리기술개발사업에서 지원하는 지중환경내 휘발성유기오염물질 조사 및 노출 평가 기법 개발(2020R2011681)연구에서 지원받아 수행되었습니다.
- 1. Adamson, D.T., McHugh, T.E., Rysz, M.W., Landazuri, R., and Newell, C.J., 2012, Field Investigation of Vapor-phase-based Groundwater Monitoring, Ground Water Monit Remediat, 32(1), 59-72.
-

- 2. Amato, E.D., Simpson, S.L., Belzunce-Segarra, M.J., Jarolimek, C.V., and Jolley, D.F., 2015, Metal Fluxes from Porewaters and Labile Sediment Phases for Predicting Metal Exposure and Bioaccumulation in Benthic Invertebrates, Environ. Sci. Technol., 49(24), 14204-14212.
-

- 3. Amato, E.D., Simpson, S.L., Remaili, T.M., Spadaro, D.A., Jarolimek, C.V., and Jolley, D.F., 2016, Assessing the Effects of Bioturbation on Metal Bioavailability in Contaminated Sediments by Diffusive Gradients in Thin Films (DGT), Environ. Sci. Technol., 50(6), 3055-3064.
-

- 4. Apell, J.N. and Gschwend, P.M., 2014, Validating the Use of Performance Reference Compounds in Passive Samplers to Assess Porewater Concentrations in Sediment Beds, Environ. Sci. Technol., 48(17), 10301-10307.
-

- 5. Arp, H.P.H., Lundstedt, S., Josefsson, S., Cornelissen, G., Enell, A., Allard, A.-S., and Kleja, D.B., 2014, Native Oxy-PAHs, N-PACs, and PAHs in Historically Contaminated Soils from Sweden, Belgium, and France: Their Soil-Porewater Partitioning Behavior, Bioaccumulation in Enchytraeus crypticus, and Bioavailability, Environ. Sci. Technol., 48(19), 11187-11195.
-

- 6. Asl-Hariri, S., Gómez-Ríos, G.A., Gionfriddo, E., Dawes, P., and Pawliszyn, J., 2014, Development of Needle Trap Technology for On-Site Determinations: Active and Passive Sampling, Anal. Chem., 86(12), 5889-5897.
-

- 7. ASTM, 2013, D6246-08(2013)e1, Standard Practice for Evaluating the Performance of Diffusive Samplers, ASTM International, West Conshohocken, PA, 2013.
- 8. ASTM, 2016, ASTM D7758 - 11(2016) Standard Practice for Passive Soil Gas Sampling in the Vadose Zone for Source Identification, Spatial Variability Assessment, Monitoring, and Vapor Intrusion Evaluations.
- 9. Bade, R., Oh, S., and Shin, W.S., 2012, Diffusive gradients in thin films (DGT) for the prediction of bioavailability of heavy metals in contaminated soils to earthworm (Eisenia foetida) and oral bioavailable concentrations, Sci. Total Environ., 416, 127-136.
-

- 10. Bao, L.J., Wu, X., Jia, F., Zeng, E.Y., and Gan, J., 2016, Isotopic exchange on solid-phase micro extraction fiber in sediment under stagnant conditions: Implications for field application of performance reference compound calibration, Environ. Toxicol. Chem., 35(8), 1978-1985.
-

- 11. Barcelona, M.J. and Helfrich, J.A., 1986, Well construction and purging effects on ground-water samples, Environ. Sci. Technol., 20(11), 1179-1184.
-

- 12. Barcelona, M.J., Varljen, M.D., Puls, R.W., and Kaminski, D., 2005, Ground water purging and sampling methods: History vs. hysteria, Ground Water Monit Remediat, 25(1), 52-62.
-

- 13. Bopp, S., Wei©¬, H., and Schirmer, K., 2005, Time-integrated monitoring of polycyclic aromatic hydrocarbons (PAHs) in groundwater using the Ceramic Dosimeter passive sampling device. J. CHROMATOGR. A, 1072(1), 137-147.
-

- 14. Bopp, S.K., McLachlan, M.S., and Schirmer, K., 2007, Passive Sampler for Combined Chemical and Toxicological Long-Term Monitoring of Groundwater: The Ceramic Toximeter, Environ. Sci. Technol., 41(19), 6868-6876.
-

- 15. Britt, S.L., Parker, B.L., and Cherry, J.A., 2010, A Downhole Passive Sampling System To Avoid Bias and Error from Groundwater Sample Handling, Environ. Sci. Technol., 44(13), 4917-4923.
-

- 16. Burgess, R.M., Lohmann, R., Schubauer-Berigan, J.P., Reitsma, P., Perron, M.M., Lefkovitz, L., and Cantwell, M.G., 2015, Application of passive sampling for measuring dissolved concentrations of organic contaminants in the water column at three marine superfund sites, Environ. Toxicol. Chem., 34(8), 1720-1733.
-

- 17. Cattani, I., Fragoulis, G., Boccelli, R., and Capri, E., 2006, Copper bioavailability in the rhizosphere of maize (Zea mays L.) grown in two Italian soils, Chemosphere, 64(11), 1972-1979.
-

- 18. Challis, J.K., Hanson, M.L., and Wong, C.S., 2016, Development and Calibration of an Organic-Diffusive Gradients in Thin Films Aquatic Passive Sampler for a Diverse Suite of Polar Organic Contaminants, Anal. Chem., 88(21), 10583-10591.
-

- 19. Davison, W., Grime, G.W., Morgan, J.A.W., and Clarke, K., 1991, Distribution of dissolved iron in sediment pore waters at submillimetre resolution, Nature, 352, 323-325.
-

- 20. de Jonge, H. and Rothenberg, G., 2005, New Device and Method for Flux-Proportional Sampling of Mobile Solutes in Soil and Groundwater, Environ. Sci. Technol., 39(1), 274-282.
-

- 21. DeSutter, T.M., Sauer, T.J., and Parkin, T.B., 2006, Porous tubing for use in monitoring soil CO2 concentrations, Soil Biol. Biochem., 38(9), 2676-2681.
-

- 22. DiGiulio, D., Paul, C., Cody, R., Willey, R., Clifford, S., Mosley, R., Lee, A., and Christensen, K., 2006, Comparison of Geoprobe¢ç PRT and AMS GVP Soil-Gas Sampling Systems with Dedicated Vapor Probes in Sandy Soils at the Raymark Superfund Site, U.S. Environmental Protection Agency Office Of Research And Development National Risk Management Research Laboratory Cincinnati, OH 45268.
- 23. Divine, C.E. and McCray, J.E., 2004, Estimation of Membrane Diffusion Coefficients and Equilibration Times for Low-Density Polyethylene Passive Diffusion Samplers, Environ. Sci. Technol., 38(6), 1849-1857.
-

- 24. Dočekalová, H., Kovaříková, V., and Dočekal, B., 2012, Mobility and bioaccessibility of trace metals in soils assessed by conventional extraction procedures and passive diffusive samplers, Chem. Speciat. Bioavailab., 24(4), 261-265.
-

- 25. Duquène, L., Vandenhove, H., Tack, F., Van Hees, M., and Wannijn, J., 2010, Diffusive gradient in thin FILMS (DGT) compared with soil solution and labile uranium fraction for predicting uranium bioavailability to ryegrass, J Environ Radioact, 101(2), 140-147.
-

- 26. Endo, S., Hale, S.E., Goss, K.-U., and Arp, H.P.H., 2011, Equilibrium Partition Coefficients of Diverse Polar and Nonpolar Organic Compounds to Polyoxymethylene (POM) Passive Sampling Devices, Environ. Sci. Technol., 45(23), 10124-10132.
-

- 27. Enell, A., Lundstedt, S., Arp, H.P.H., Josefsson, S., Cornelissen, G., Wik, O., and Berggren Kleja, D., 2016, Combining Leaching and Passive Sampling To Measure the Mobility and Distribution between Porewater, DOC, and Colloids of Native Oxy-PAHs, N-PACs, and PAHs in Historically Contaminated Soil, Environ. Sci. Technol., 50(21), 11797-11805.
-

- 28. Ernstberger, H., Zhang, H., Tye, A., Young, S., and Davison, W., 2005, Desorption kinetics of Cd, Zn, and Ni measured in soils by DGT, Environ. Sci. Technol., 39(6), 1591-1597.
-

- 29. Fauvelle, V., Kaserzon, S.L., Montero, N., Lissalde, S., Allan, I.J., Mills, G., Mazzella, N., Mueller, J.F., and Booij, K., 2017, Dealing with Flow Effects on the Uptake of Polar Compounds by Passive Samplers, Environ. Sci. Technol., 51(5), 2536-2537.
-

- 30. Fernandez, L.A., Lao, W., Maruya, K.A., and Burgess, R.M., 2014, Calculating the Diffusive Flux of Persistent Organic Pollutants between Sediments and the Water Column on the Palos Verdes Shelf Superfund Site Using Polymeric Passive Samplers, Environ. Sci. Technol., 48(7), 3925-3934.
-

- 31. Fones, G.R., Davison, W., Holby, O., Jorgensen, B.B., and Thamdrup, B., 2001, High‐resolution metal gradients measured by in situ DGT/DET deployment in Black Sea sediments using an autonomous benthic lander, Limnol. Oceanogr. 46(4), 982-988.
-

- 32. Freedman, Y.E., Ronen, D., and Long, G.L., 1996, Determination of Cu and Cd Content of Groundwater Colloids by Solid Sampling Graphite Furnace Atomic Absorption Spectrometry, Environ. Sci. Technol., 30(7), 2270-2277.
-

- 33. Gao, Y., Leermakers, M., Gabelle, C., Divis, P., Billon, G., Ouddane, B., Fischer, J.-C., Wartel, M., and Baeyens, W., 2006, High-resolution profiles of trace metals in the pore waters of riverine sediment assessed by DET and DGT, Sci. Total Environ., 362(1-3), 266-277.
-

- 34. Garnier, J.-M., Garnier, J., Jézéquel, D., and Angeletti, B., 2015, Using DET and DGT probes (ferrihydrite and titanium dioxide) to investigate arsenic concentrations in soil porewater of an arsenic-contaminated paddy field in Bangladesh, Sci. Total Environ., 536, 306-315.
-

- 35. Go, U.J. and Eom, I.-Y., 2014, Development of syringe pump assisted headspace sampler, J. Chromatogr. A, 1361, 88-94.
-

- 36. Gomez-Eyles, J.L., Jonker, M.T.O., Hodson, M.E., and Collins, C.D., 2012, Passive Samplers Provide a Better Prediction of PAH Bioaccumulation in Earthworms and Plant Roots than Exhaustive, Mild Solvent, and Cyclodextrin Extractions, Environ. Sci. Technol., 46(2), 962-969.
-

- 37. Górecki, T. and Namieśnik, J., 2002, Passive sampling. Trends. Analyt. Chem., 21(4), 276-291.
-

- 38. Greenwood, R., Mills, G., and Vrana, B., 2007, Passive Sampling Techniques in Environmental Monitoring, Volume 48, 1st Edition,Comprehensive Analytical Chemistry, Elsevier Science.
- 39. Gut, A., Blatter, A., Fahrni, M., Lehmann, B.E., Neftel, A., and Staffelbach, T., 1998, A new membrane tube technique (METT) for continuous gas measurements in soils, Plant Soil, 198(1), 79-88.
-

- 40. Hale, S.E., Elmquist, M., Brandli, R., Hartnik, T., Jakob, L., Henriksen, T., Werner, D., and Cornelissen, G., 2012, Activated carbon amendment to sequester PAHs in contaminated soil: a lysimeter field trial, Chemosphere, 87(2), 177-184.
-

- 41. Hong, L. and Luthy, R.G., 2008, Uptake of PAHs into polyoxymethylene and application to oil-soot (lampblack)-impacted soil samples, Chemosphere, 72(2), 272-281.
-

- 42. ITRC, 2007a, (Interstate Technology & Regulatory Council) Vapor Intrusion Pathway: A Practical Guideline. VI-1. Washington, D.C.: Interstate Technology & Regulatory Council, Vapor Intrusion Team. www.itrcweb.org.
- 43. ITRC, 2007b, Protocol for Use of Five Passive Samplers to Sample for a Variety of Contaminants in Groundwater (The Interstate Technology & Regulatory Council), Document DSP5.
- 44. Jacinthe, P.A., Dick, W.A., 1996, Use of silicone tubing to sample nitrous oxide in the soil atmosphere. Soil Biol. Biochem., 28(6), 721-726.
-

- 45. Johnson, R.E. and Hajcak, C.A., 2007, Passive Diffusion Groundwater Samplers: A New Way to Sample Groundwater, Environ. Claims J., 19(1-2), 88-96.
-

- 46. Joyce, A.S., Portis, L.M., Parks, A.N., and Burgess, R.M., 2016, Evaluating the Relationship between Equilibrium Passive Sampler Uptake and Aquatic Organism Bioaccumulation, Environ. Sci. Technol., 50(21), 11437-11451.
-

- 47. Kalis, E.J., Weng, L., Dousma, F., Temminghoff, E.J., and Van Riemsdijk, W.H., 2006, Measuring free metal ion concentrations in situ in natural waters using the Donnan membrane technique, Environ. Sci. Technol., 40(3), 955-961.
-

- 48. Kaserzon, S.L., Kennedy, K., Hawker, D.W., Thompson, J., Carter, S., Roach, A.C., Booij, K., and Mueller, J.F., 2012, Development and Calibration of a Passive Sampler for Perfluorinated Alkyl Carboxylates and Sulfonates in Water, Environ. Sci. Technol., 46(9), 4985-4993.
-

- 49. Kaserzon, S.L., Vijayasarathy, S., Bräunig, J., Mueller, L., Hawker, D.W., Thomas, K.V., and Mueller, J.F., 2019, Calibration and validation of a novel passive sampling device for the time integrative monitoring of per-and polyfluoroalkyl substances (PFASs) and precursors in contaminated groundwater, J. Hazard. Mater., 366, 423-431.
-

- 50. Kočí, V., Ocelka, T., and Grabic, R., 2009, Background level of POPs in ground water assessed on chemical and toxicity analysis of exposed semipermeable membrane devices, Air, Soil Water Res. 2, ASWR. S2128.
-

- 51. Kot-Wasik, A., Zabiega©©a, B., Urbanowicz, M., Dominiak, E., Wasik, A., and Namieśnik, J., 2007, Advances in passive sampling in environmental studies, Anal. Chim. Acta, 602(2), 141-163.
-

- 52. Kot, A., Zabiega©©a, B., and Namieśnik, J., 2000, Passive sampling for long-term monitoring of organic pollutants in water, Trends Analyt Chem, 19(7), 446-459.
-

- 53. Kwon-Rae, K., and Owens, G., 2009, Chemodynamics of heavy metals in long-term contaminated soils: Metal speciation in soil solution, J Environ Sci (China), 21(11), 1532-1540.
-

- 54. Louise, P., Willey, R., Mchale, T., Major, W., Hall, T., Bailey, R., Gagnon, K., and Gooch, G., 2014, Demonstration of the AGI Universal Samplers (F.K.A. the GORE¢ç Modules) for Passive Sampling of Groundwater, Environmental Security Technology Certification Program (ESTCP), Project ER-200921.
- 55. Laemmel, T., Maier, M., Schack-Kirchner, H., and Lang, F., 2017, An in situ method for real-time measurement of gas transport in soil, Eur. J. Soil. Sci., 68(2), 156-166.
-

- 56. Lang, S.-C., Hursthouse, A., Mayer, P., Kötke, D., Hand, I., Schulz-Bull, D., and Witt, G., 2015, Equilibrium passive sampling as a tool to study polycyclic aromatic hydrocarbons in Baltic Sea sediment pore-water systems, Mar. Pollut. Bull., 101(1), 296-303.
-

- 57. Laor, Y., Ronen, D., and Graber, E.R., 2003, Using a Passive Multilayer Sampler for Measuring Detailed Profiles of Gas-Phase VOCs in the Unsaturated Zone, Environ. Sci. Technol., 37(2), 352-360.
-

- 58. Leermakers, M., Gao, Y., Gabelle, C., Lojen, S., Ouddane, B., Wartel, M., and Baeyens, W., 2005, Determination of High Resolution Pore Water Profiles of Trace Metals in Sediments of the Rupel River (Belgium) using Det (Diffusive Equilibrium in Thin Films) and DGT (Diffusive Gradients in Thin Films) Techniques, Water Air Soil Pollut., 166(1-4), 265-286.
-

- 59. Lucas, A.R., Reid, N., Salmon, S.U., and Rate, A.W., 2014, Quantitative assessment of the distribution of dissolved Au, As and Sb in groundwater using the diffusive gradients in thin films technique, Environ. Sci. Technol., 48(20), 12141-12149.
-

- 60. Magnusson, T., 1989, A method for equilibration chamber sampling and gas chromatographic analysis of the soil atmosphere, Plant Soil, 120(1), 39-47.
-

- 61. Mali, N., Cerar, S., Koroša, A., and Auersperger, P., 2017, Passive sampling as a tool for identifying micro-organic compounds in groundwater. Sci. Total Environ., 593-594, 722-734.
-

- 62. Marchal, G., Smith, K.E., Mayer, P., Wollesen de Jonge, L., and Karlson, U.G., 2014, Impact of soil amendments and the plant rhizosphere on PAH behaviour in soil, Environ. Pollut. (Barking, Essex : 1987), 188, 124-131.
-

- 63. Martin, H., Patterson, B.M., Davis, G.B., and Grathwohl, P., 2003, Field Trial of Contaminant Groundwater Monitoring: Comparing Time-Integrating Ceramic Dosimeters and Conventional Water Sampling, Environ. Sci. Technol., 37(7), 1360-1364.
-

- 64. Maruya, K.A., Zeng, E.Y., Tsukada, D., and Bay, S.M., 2009, A passive sampler based on solid-phase microextraction for quantifying hydrophobic organic contaminants in sediment pore water, Environ. Toxicol. Chem., 28(4), 733-740.
-

- 65. Mayer, P., Parkerton, T.F., Adams, R.G., Cargill, J.G., Gan, J., Gouin, T., Gschwend, P.M., Hawthorne, S.B., Helm, P., Witt, G., You, J., and Escher, B.I., 2014, Passive sampling methods for contaminated sediments: scientific rationale supporting use of freely dissolved concentrations, Integr. Environ. Assess. Manag., 10(2), 197-209.
-

- 66. McLeish, K., Ryan, M.C., and Chu, A., 2007, Integrated Sampling and Analytical Approach for Common Groundwater Dissolved Gases, Environ. Sci. Technol., 41(24), 8388-8393.
-

- 67. Muhammad, I., Puschenreiter, M., and Wenzel, W.W., 2012, Cadmium and Zn availability as affected by pH manipulation and its assessment by soil extraction, DGT and indicator plants, Sci. Total Environ., 416, 490-500.
-

- 68. Muijs, B. and Jonker, M.T., 2012, Does equilibrium passive sampling reflect actual in situ bioaccumulation of PAHs and petroleum hydrocarbon mixtures in aquatic worms?, Environ. Sci. Technol., 46(2), 937-944.
-

- 69. Nauer, P.A., Chiri, E., and Schroth, M.H., 2013, Poly-Use Multi-Level Sampling System for Soil-Gas Transport Analysis in the Vadose Zone, Environ. Sci. Technol., 47(19), 11122-11130.
-

- 70. NRC, 2003, Bioavailability of Contaminants in Soils and Sediments: Processes, Tools, and Applications, Committee on Bioavailability of Contaminants in Soils and Sediments, National Research Council.
- 71. Ort, C., Lawrence, M.G., Rieckermann, J., and Joss, A., 2010, Sampling for Pharmaceuticals and Personal Care Products (PPCPs) and Illicit Drugs in Wastewater Systems: Are Your Conclusions Valid? A Critical Review, Environ. Sci. Technol., 44(16), 6024-6035.
-

- 72. Panikov, N.S., Mastepanov, M.A., and Christensen, T.R., 2007, Membrane probe array: Technique development and observation of CO2 and CH4 diurnal oscillations in peat profile, Soil Biol. Biochem., 39(7), 1712-1723.
-

- 73. Papastefanou, C., 2002, An overview of instrumentantion for measuring radon in soil gas and groundwaters, J Environ Radioact, 63(3), 271-283.
-

- 74. Peng, Q., Wang, M., Cui, Z., Huang, J., Chen, C., Guo, L., and Liang, D., 2017, Assessment of bioavailability of selenium in different plant-soil systems by diffusive gradients in thin-films (DGT), Environ. Pollut., 225, 637-643.
-

- 75. Petersen, S.O., 2014, Diffusion probe for gas sampling in undisturbed soil, Eur J Soil Sci, 65(5), 663-671.
-

- 76. Roulier, J.L., Tusseau-Vuillemin, M.H., Coquery, M., Geffard, O., and Garric, J., 2008, Measurement of dynamic mobilization of trace metals in sediments using DGT and comparison with bioaccumulation in Chironomus riparius: First results of an experimental study, Chemosphere, 70(5), 925-932.
-

- 77. Scherr, K.E., Hasinger, M., Mayer, P., and Loibner, A.P., 2009, Effect of vegetable oil addition on bioaccessibility and biodegradation of polycyclic aromatic hydrocarbons in historically contaminated soils, J. Chem. Technol. Biotechnol., 84(6), 827-835.
-

- 78. Seethapathy, S., Górecki, T., and Li, X., 2008, Passive sampling in environmental analysis. J. Chromatogr. A, 1184(1-2), 234-253.
-

- 79. Senila, M., 2014, Real and simulated bioavailability of lead in contaminated and uncontaminated soils, J. Environ. Health Sci. Eng., 12, 108.
-

- 80. Senila, M., Levei, E.A., and Senila, L.R., 2012, Assessment of metals bioavailability to vegetables under field conditions using DGT, single extractions and multivariate statistics, Chem. Cent. J., 6(1), 119.
-

- 81. Simpson, S.L., Yverneau, H., Cremazy, A., Jarolimek, C.V., Price, H.L., and Jolley, D.F., 2012, DGT-Induced Copper Flux Predicts Bioaccumulation and Toxicity to Bivalves in Sediments with Varying Properties, Environ. Sci. Technol., 46(16), 9038-9046.
-

- 82. Spalding, B.P. and Watson, D.B., 2006, Measurement of Dissolved H2, O2, and CO2 in Groundwater Using Passive Samplers for Gas Chromatographic Analyses, Environ. Sci. Technol., 40(24), 7861-7867.
-

- 83. Stefaniuk, M. and Oleszczuk, P., 2016, Addition of biochar to sewage sludge decreases freely dissolved PAHs content and toxicity of sewage sludge-amended soil, Environ. Pollut. (Barking, Essex : 1987), 218, 242-251.
-

- 84. Temminghoff, E.J., Plette, A.C., Van Eck, R., and Van Riemsdijk, W.H., 2000, Determination of the chemical speciation of trace metals in aqueous systems by the Wageningen Donnan Membrane Technique, Anal. Chim. Acta, 417(2), 149-157.
-

- 85. Ter Laak, T.L., Agbo, S.O., Barendregt, A., and Hermens, J.L., 2006, Freely dissolved concentrations of PAHs in soil pore water: measurements via solid-phase extraction and consequences for soil tests, Environ. Sci. Technol., 40(4), 1307-1313.
-

- 86. USEPA, 1989, Risk Assessment Guidance for Superfund. Volume I. Human Health Evaluation Manual (Part A). EPA/540/1-89/002.
- 87. USEPA, 2002, Ground-Water Sampling Guidelines for Superfund and RCRA Project Managers, Office of Solid Waste and Emergency Response, EPA 542-S-02-001.
- 88. USEPA, 2007, Guidance for Evaluating the Oral Bioavailability of Metals in Soils for Use in Human Health Risk Assessment, OSWER 9285.7-80.
- 89. USEPA, 2015, Assessing and Mitigating the Vapor Intrusion Pathway from Subsurface Vapor Sources to Indoor Air, U.S. Environmental Protection Agency, Office of Solid Waste and Emergency Response, June 2015.
- 90. Vandenhove, H., Antunes, K., Wannijn, J., Duquène, L., and Van Hees, M., 2007, Method of diffusive gradients in thin films (DGT) compared with other soil testing methods to predict uranium phytoavailability. Sci. Total Environ., 373(2-3), 542-555.
-

- 91. Vinturella, A.E., Burgess, R.M., Coull, B.A., Thompson, K.M., and Shine, J.P., 2004, Use of Passive Samplers To Mimic Uptake of Polycyclic Aromatic Hydrocarbons by Benthic Polychaetes, Environ. Sci. Technol., 38(4), 1154-1160.
-

- 92. Vrana, B., Allan, I.J., Greenwood, R., Mills, G.A., Dominiak, E., Svensson, K., Knutsson, J., and Morrison, G., 2005, Passive sampling techniques for monitoring pollutants in water, Trends Analyt Chem, 24(10), 845-868.
-

- 93. Vroblesky, D., 2001a, User's Guide for Polyethylene-Based Passive Diffusion Bag Samplers to Obtain Volatile Organic Compound Concentrations in Wells, Part 1: Deployment, Recovery, Data Interpretation, and Quality Control and Assurance; U.S. Geological Survey Water-Resources Investigations Report 01-4060, 18 pp.
-

- 94. Vroblesky, D., 2001b, User's Guide for Polyethylene-Based Passive Diffusion Bag Samplers to Obtain Volatile Organic Compound Concentrations in Wells, Part 2: Field Tests; U.S. Geological Survey Water-Resources Investigations Report 01-4061.
-

- 95. Weisbrod, N., Ronen, D., and Nativ, R., 1996, New Method for Sampling Groundwater Colloids under Natural Gradient Flow Conditions, Environ. Sci. Technol., 30(10), 3094-3101.
-

- 96. Weng, L., Van Riemsdijk, W.H., and Temminghoff, E.J., 2010, Effects of lability of metal complex on free ion measurement using DMT, Environ. Sci. Technol., 44(7), 2529-2534.
-

- 97. Yao, Y., Wang, P.-F., Wang, C., Hou, J., and Miao, L.-Z., 2017, The Evaluation on the Cadmium Net Concentration for Soil Ecosystems, Int. J. Environ. Res. Public Health, 14(3), 297.
-

- 98. Yin, H., Cai, Y., Duan, H., Gao, J., and Fan, C., 2014, Use of DGT and conventional methods to predict sediment metal bioavailability to a field inhabitant freshwater snail (Bellamya aeruginosa) from Chinese eutrophic lakes, J. Hazard. Mater., 264, 184-194.
-

- 99. Zarrouk, S., Bermond, A., Benzina, N.K., Sappin-Didier, V., and Denaix, L., 2014, Diffusive gradient in thin-film (DGT) models Cd and Pb uptake by plants growing on soils amended with sewage sludge and urban compost, Environ Chem Lett, 12(1), 191-199.
-

- 100. Zhang, C., Ding, S., Xu, D., Tang, Y., and Wong, M.H., 2014, Bioavailability assessment of phosphorus and metals in soils and sediments: a review of diffusive gradients in thin films (DGT), Environ. Monit. Assess., 186(11), 7367-7378.
-

- 101. Zhang, H. and Davison, W., 1995, Performance characteristics of diffusion gradients in thin films for the in situ measurement of trace metals in aqueous solution, Anal. Chem., 67(19), 3391-3400.
-

- 102. 한국지하수토양환경학회, 2008, 토양위해성평가, 동화기술.
- 103. Yong Seok, H., 2013, 종설 : 박막분산탐침(diffusive gradient in thin film probe)의 수중 생물학적 이용가능한 중금속 측정 적용, 한국물환경학회지, 29(5), 691-702.
- 104. 환경부, 2015, 토양오염물질 위해성평가 지침.
 This Article
This Article
-
2021; 26(2): 1-16
Published on Apr 30, 2021
- 10.7857/JSGE.2021.26.2.001
- Received on Apr 13, 2021
- Revised on Apr 16, 2021
- Accepted on Apr 20, 2021
 Services
Services
Shared
 Correspondence to
Correspondence to
- Yongseok Hong
-
College of Science and Technology, Korea University Sejong Campus
- E-mail: yongseokhong@korea.ac.kr